2.3: Families en Periodes van het Periodiek Systeem
Families van het Periodiek Systeem
Houd in gedachten dat Mendelejev het periodiek systeem zo schikte dat elementen met de meest gelijkende eigenschappen in dezelfde groep werden geplaatst. Een groep is een verticale kolom van het periodiek systeem. Alle 1A-elementen hebben één valentie-elektron. Daardoor reageren deze elementen op dezelfde manier als de andere leden van de familie. De elementen in 1A zijn allemaal zeer reactief en vormen verbindingen in dezelfde verhoudingen met vergelijkbare eigenschappen met andere elementen. Omwille van hun gelijkenissen in hun chemische eigenschappen, plaatste Mendelejev deze elementen in dezelfde groep. Groep 1A is ook bekend als de alkalimetalen. Hoewel de meeste metalen de neiging hebben zeer hard te zijn, zijn deze metalen eigenlijk zacht en kunnen gemakkelijk worden gesneden.
Groep 2A wordt ook wel de alkalische aardmetalen genoemd. Nogmaals, door hun overeenkomsten in elektronenconfiguraties hebben deze elementen soortgelijke eigenschappen als elkaar. Hetzelfde patroon is waar voor andere groepen in het periodiek systeem. Onthoud dat Mendelejev de tabel zo heeft ingedeeld dat elementen met de meest vergelijkbare eigenschappen in dezelfde groep van het periodiek systeem zaten.
Het is belangrijk om een paar andere belangrijke groepen op het periodiek systeem te herkennen aan hun groepsnaam. Groep 7A (of 17) elementen worden ook wel halogenen genoemd. Deze groep bevat zeer reactieve niet-metaalelementen.
De edelgassen zitten in groep 8A. Ook deze elementen hebben gelijksoortige eigenschappen, met als belangrijkste eigenschap dat ze uiterst onreactief zijn en zelden verbindingen vormen. De reden hiervoor zullen we later leren, wanneer we bespreken hoe verbindingen worden gevormd. De elementen in deze groep zijn ook gassen bij kamertemperatuur.
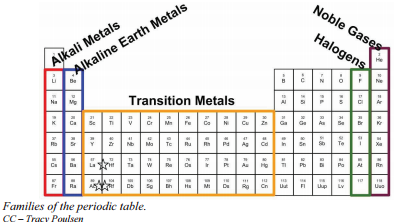
Een alternatief nummeringssysteem nummert alle blokelementen van 1-18. In dit nummeringsysteem worden de blokelementen van groep 1A, 1A, 1A en D van 1-18 genummerd. In dit nummeringsysteem is groep 1A groep 1; groep 2A is groep 2; de halogenen (7A) zijn groep 17; en de edelgassen (8A) zijn groep 18. Je zult periodieke tabellen tegenkomen met beide nummersystemen. Het is belangrijk om te weten welk nummeringssysteem wordt gebruikt en om het aantal valentie-elektronen in de hoofdblokelementen te kunnen vinden, ongeacht welk nummeringssysteem wordt gebruikt.