Alles over baarmoederhalskanker
Wat is de baarmoederhals?
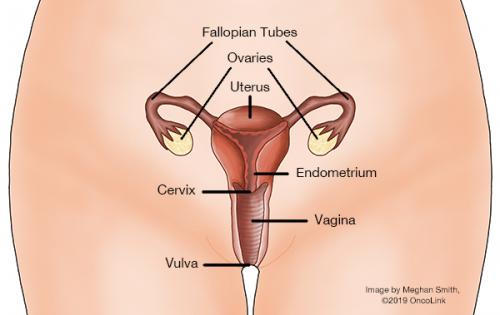
De baarmoederhals is de naam voor het onderste deel van de baarmoeder. Alleen vrouwen hebben een baarmoeder. De baarmoeder is de plaats waar een baby groeit en zich ontwikkelt als een vrouw zwanger is. Tijdens de zwangerschap wordt de baarmoeder veel groter. Als een vrouw niet zwanger is, is de baarmoeder een klein, peervormig orgaan dat tussen de endeldarm en de blaas van de vrouw zit. De baarmoederhals verbindt de baarmoeder met het geboortekanaal (de vagina). Uw zorgverlener kan uw baarmoederhals bekijken en een monster van de cellen nemen (pap-test) tijdens een routine bekkenonderzoek.
Wat is baarmoederhalskanker?
Baarmoederhalskanker ontwikkelt zich wanneer cellen in de baarmoederhals uit de hand beginnen te groeien. Deze cellen kunnen ook naburige weefsels binnendringen of zich over het hele lichaam verspreiden. Grote verzamelingen cellen die abnormaal groeien, worden tumoren genoemd. Gewoonlijk groeit baarmoederhalskanker zeer langzaam. In bepaalde omstandigheden kan het echter snel groeien en zich snel verspreiden.
Cankers worden gekenmerkt door de cellen waaruit ze oorspronkelijk zijn ontstaan. De meest voorkomende vorm van baarmoederhalskanker wordt plaveiselcelcarcinoom genoemd. Het ontstaat uit cellen die aan de oppervlakte van de baarmoederhals liggen, de zogenaamde plaveiselcellen. Plaveiselcel baarmoederhalskanker maakt ongeveer 80% van alle baarmoederhalskankers uit. De tweede meest voorkomende vorm is adenocarcinoom. Deze is afkomstig van cellen die klieren in de baarmoederhals vormen. Het percentage baarmoederhalskankers dat een adenocarcinoom is, is sinds de jaren zeventig gestegen, maar niemand weet precies waarom. Ongeveer 3% tot 5% van de baarmoederhalskankers vertonen kenmerken van zowel plaveisel- als adenocarcinomen en worden adenosquameuze carcinomen genoemd. Er zijn nog een paar andere zeer zeldzame typen, zoals kleincellig en neuro-endocrien carcinoom, maar die zijn uiterst zeldzaam.
Wat veroorzaakt baarmoederhalskanker en loop ik risico?
Baarmoederhalskanker komt in ontwikkelingslanden veel vaker voor dan in ontwikkelde landen. Baarmoederhalskanker is de op één na meest voorkomende doodsoorzaak door kanker in ontwikkelingslanden. 84% van alle gevallen van baarmoederhalskanker doet zich voor in onderontwikkelde gebieden in Afrika, Latijns-Amerika en het Caribisch gebied. In de Verenigde Staten is het vrij zeldzaam. Elk jaar worden in de Verenigde Staten naar schatting 13.800 gevallen van baarmoederhalskanker gediagnosticeerd. In de ontwikkelde landen is het aantal sterfgevallen als gevolg van baarmoederhalskanker in de afgelopen 50 jaar met 75% gedaald. Het grootste deel van deze daling wordt toegeschreven aan de effectieve instelling van screeningprogramma’s voor baarmoederhalskanker (HPV-tests en/of Pap-tests) in ontwikkelde landen.
Een van de belangrijkste risicofactoren voor baarmoederhalskanker is infectie met een virus dat HPV (humaan papillomavirus) wordt genoemd. Benadrukt moet worden dat slechts een zeer klein percentage van de vrouwen die HPV hebben, baarmoederhalskanker zullen krijgen. Het feit dat je HPV hebt, betekent niet dat je kanker zult krijgen. Bij bijna alle gevallen van baarmoederhalskanker zijn echter sporen van het HPV-virus gevonden, dus HPV-infectie is een belangrijke risicofactor voor het krijgen van baarmoederhalskanker. HPV is een seksueel overdraagbare aandoening (soa) die ongelooflijk veel voorkomt onder de bevolking. In feite zijn de meeste mannen en vrouwen van middelbare leeftijd blootgesteld aan HPV.
HPV is het virus dat genitale wratten veroorzaakt, maar het hebben van genitale wratten betekent niet noodzakelijkerwijs dat je baarmoederhalskanker krijgt. Er zijn verschillende subtypes, of stammen, van HPV. Alleen bepaalde subtypes kunnen baarmoederhalskanker veroorzaken. Vaak veroorzaakt infectie met HPV helemaal geen symptomen, totdat een vrouw een voorstadium van kanker in de baarmoederhals ontwikkelt.
Omdat het hebben van een soa een risicofactor voor baarmoederhalskanker is, is elke risicofactor voor het ontwikkelen van soa’s ook een risicofactor voor het ontwikkelen van baarmoederhalskanker. Deze omvatten:
- Het hebben gehad van meerdere mannelijke seksuele partners.
- Op jonge leeftijd beginnen met geslachtsgemeenschap.
- Het hebben gehad van mannelijke seksuele partners die als hoog risico worden beschouwd (ze hebben veel seksuele partners gehad en/of zijn op jonge leeftijd begonnen met geslachtsgemeenschap).
- Diagnose van een andere seksueel overdraagbare aandoening (zoals herpes, gonorroe, syfilis of chlamydia).
HIV-infectie is een andere risicofactor voor baarmoederhalskanker, maar om een iets andere reden. Het blijkt dat elke aandoening die je immuunsysteem verzwakt ook je risico op het ontwikkelen van baarmoederhalskanker verhoogt. Aandoeningen die uw immuunsysteem verzwakken zijn onder meer HIV, een orgaantransplantatie en Hodgkin-lymfoom.
Een andere belangrijke risicofactor voor het krijgen van baarmoederhalskanker is roken. Rokers hebben ten minste twee keer zoveel kans op het ontwikkelen van baarmoederhalskanker als niet-rokers. Ten slotte lijken vrouwen die in armoede leven, een verhoogde kans te hebben om baarmoederhalskanker te ontwikkelen en eraan te sterven. Dit zou te maken kunnen hebben met een hoger percentage rokende vrouwen, of misschien met belemmeringen om jaarlijks een screening te ondergaan.
Zelfs iemand zonder risicofactoren kan baarmoederhalskanker krijgen. Tijdige screening en vroege opsporing zijn onze beste wapens om het aantal nieuwe gevallen van baarmoederhalskanker terug te dringen.
Hoe kan ik baarmoederhalskanker voorkomen?
Er zijn verschillende dingen die vrouwen kunnen doen om het risico op het krijgen van baarmoederhalskanker te verkleinen. Dit zijn onder andere:
- Draag regelmatig screenings: De drastische daling van het aantal gevallen van baarmoederhalskanker en het aantal sterfgevallen in de Verenigde Staten is te danken aan HPV- en Pap-tests. Screening zal meer worden besproken in de volgende paragraaf.
- Gevaccineerd worden:
- Drie vaccins, genaamd Gardasil, Gardasil 9, en Ceravix zijn ontwikkeld. Momenteel is alleen Gardasil 9 beschikbaar in de VS.
- Het HPV-vaccin wordt aanbevolen voor alle personen van 12-26 jaar. De Amerikaanse FDA heeft het vaccin goedgekeurd voor gebruik tot de leeftijd van 45 jaar, maar niet alle verzekeringsmaatschappijen dekken het HPV-vaccin voor personen boven de leeftijd van 26 jaar.
- Het is aangetoond dat deze vaccins effectief zijn in het voorkomen van infectie met sommige stammen van HPV als ze worden gegeven voordat een persoon wordt blootgesteld aan HPV. Ook als u al HPV heeft, kunt u gevaccineerd worden. Het vaccin kan u beschermen tegen andere soorten HPV
- Naast baarmoederhalskanker is HPV ook een oorzaak van vulvar-, vaginale, penile en anale kankers en sommige hoofd- & halskankers. Het veroorzaakt ook genitale wratten en leidt tot abnormale Pap-test resultaten die resulteren in verdere tests of behandeling.
- Begin niet met roken, en als u al rookt, is het tijd om te stoppen. Het is aangetoond dat roken het vermogen van het immuunsysteem om een HPV-infectie op te ruimen, vermindert.
- Vrouwen kunnen hun aantal seksuele partners beperken en het begin van seksuele activiteit uitstellen om het risico te verminderen, omdat meer partners de kans op infectie kunnen vergroten.
- Gebruik van een condoom en/of een beflapje (barrièremethode) kan de blootgestelde gebieden verkleinen, maar kan blootstelling niet volledig voorkomen.
Welke screeningstests worden gebruikt voor baarmoederhalskanker?
Baarmoederhalskanker wordt beschouwd als een ziekte die kan worden voorkomen. Het duurt meestal erg lang voordat voorstadia van kanker zich tot invasieve kankers ontwikkelen. Doeltreffende screeningprogramma’s in de Verenigde Staten hebben geleid tot een drastische daling van het aantal sterfgevallen door baarmoederhalskanker in de afgelopen 50 jaar. Van de vrouwen die in de ontwikkelde landen baarmoederhalskanker ontwikkelen, is 60% nooit gescreend of is de laatste vijf jaar niet gescreend. Het belang van regelmatige screening op baarmoederhalskanker kan niet genoeg worden benadrukt.
Het belangrijkste instrument voor screening op baarmoederhalskanker is de Pap-test. Pap is de afkorting van Papanicolaou, de uitvinder van de test, die in 1941 een baanbrekend artikel publiceerde. Een Pap-test kan gemakkelijk worden uitgevoerd in het kantoor van uw arts. Tijdens een bekkenonderzoek gebruikt uw arts een houten spatel en/of een borsteltje om monsters van baarmoederhalscellen te nemen. Deze cellen worden op een objectglaasje, of in een vloeibaar bewaarmiddel, gelegd en naar een laboratorium gestuurd waar een deskundige in het onderzoeken van cellen onder een microscoop kan kijken of er kankerveranderingen zijn. Veel vrouwen vinden het onderzoek ongemakkelijk, maar zelden pijnlijk. Afhankelijk van de resultaten van de test kan het nodig zijn dat uw arts verdere onderzoeken uitvoert.
Hoewel de Pap-test zeer effectief is, is het geen perfecte test. Soms kan de test cellen missen die de potentie hebben om een invasieve vorm van kanker te worden. De test mag niet worden uitgevoerd als u menstrueert. En zelfs als de afname perfect verloopt, kunnen zelfs de beste laboratoria afwijkende cellen missen. Daarom moeten vrouwen de test regelmatig laten uitvoeren.
Onlangs zijn de aanbevelingen voor screening gewijzigd om meer nadruk te leggen op HPV-tests. HPV-tests kunnen theoretisch de overgrote meerderheid van vrouwen opsporen die risico lopen op het ontwikkelen van baarmoederhalskanker door het identificeren van degenen met hoog-risico HPV-infecties. Er zijn meer dan 100 subtypes van HPV en bepaalde types hebben een grotere kans om tot baarmoederhalskanker te leiden. Het DNA van baarmoederhalscellen kan worden getest om de aanwezigheid van hoog-risicotypes van HPV vast te stellen. De HPV-DNA-test kan worden gebruikt voor vervolgonderzoek bij vrouwen bij wie bij een pap-test afwijkingen zijn vastgesteld.
De American Cancer Society beveelt de volgende richtlijnen aan voor screening op baarmoederhalskanker:
- Alle vrouwen moeten op 25-jarige leeftijd beginnen met screening op baarmoederhalskanker.
- Vrouwen tussen de 25 en 65 jaar moeten:
- Primaire HPV-tests om de 5 jaar ondergaan. Deze test is nog niet beschikbaar in veel centra/praktijken.
- Als deze test niet beschikbaar is, moet u worden gescreend met co-testing, dat is een combinatie van een HPV- en Pap-test. Dit moet om de 5 jaar worden gedaan.
- Als HPV-tests niet beschikbaar zijn, moet alleen een Pap-test om de drie jaar worden uitgevoerd.
- Vrouwen ouder dan 65 jaar die regelmatig baarmoederhalsscreenings hebben gehad die normaal waren, moeten niet worden gescreend op baarmoederhalskanker.
- Vrouwen bij wie baarmoederhalskanker is vastgesteld, moeten gescreend blijven worden totdat zij in de afgelopen 10 jaar aan een van de volgende criteria voldoen:
- 2 negatieve, opeenvolgende HPV-tests.
- Of 2 negatieve, opeenvolgende co-tests.
- Of 3 negatieve, opeenvolgende pap-testen in de afgelopen 3-5 jaar.
- Vrouwen die het HPV-vaccin hebben gehad, moeten nog steeds de screeningsaanbevelingen voor hun leeftijdsgroep volgen.
- Weliswaar beveelt de ACS niet aan elk jaar op baarmoederhalskanker te screenen, maar vrouwen moeten wel naar hun zorgverlener gaan voor een controle.
Vrouwen bij wie de baarmoeder en baarmoederhals door middel van een hysterectomie zijn verwijderd en die geen voorgeschiedenis van baarmoederhalskanker of voorstadium van kanker hebben, hoeven niet te worden gescreend.
Vrouwen die een hoog risico op baarmoederhalskanker lopen, moeten mogelijk vaker worden gescreend. Vrouwen met een verhoogd risico kunnen bijvoorbeeld HIV-besmetting, orgaantransplantatie of blootstelling aan het geneesmiddel DES in de baarmoeder hebben. Zij moeten met hun arts of verpleegkundige praten voor specifieke aanbevelingen.
Wat zijn de tekenen van baarmoederhalskanker?
In de vroege stadia van baarmoederhalskanker zijn er meestal geen symptomen. Daarom is het belangrijk dat u een screening-PAP-test ondergaat. Naarmate een tumor groter wordt, kan deze verschillende symptomen gaan vertonen, waaronder:
- Normale bloedingen (waaronder bloedingen na geslachtsgemeenschap, tussen de menstruaties in, zwaardere/langere menstruatiebloedingen, of bloedingen na de menopauze).
- Normale vaginale afscheiding (kan vies ruiken).
- Pijn in het bekken of de rug.
- Pijn bij het plassen.
- Bloed in de ontlasting of urine.
- Pijn bij het vrijen.
Veel van deze symptomen zijn niet-specifiek en kunnen een verscheidenheid van verschillende aandoeningen vertegenwoordigen. Als u een van deze symptomen heeft, praat dan met uw zorgverlener.
Hoe wordt baarmoederhalskanker vastgesteld?
De meest voorkomende reden voor uw zorgverlener om de diagnose baarmoederhalskanker te stellen, is als u een afwijkende HPV- en/of Pap-test hebt. Onthoud dat deze tests screeningtests zijn, geen diagnosetests. Na een afwijkend resultaat is verder onderzoek nodig.
ap-tests helpen bij het opsporen van voorstadia van kanker in de baarmoederhals. Een voorstadium van kanker betekent dat er abnormaal uitziende cellen zijn, maar dat ze nog niet voorbij de weefselbarrière in de baarmoederhals zijn binnengedrongen; een voorstadium van kanker kan zich dus niet verspreiden of u schaden. Als een voorstadium van kanker echter niet wordt behandeld, kan het uitgroeien tot invasieve kanker. Pap-tests worden gerapporteerd als geen abnormale cellen, atypische (abnormale) cellen van onbepaalde betekenis, laaggradige abnormale cellen, of hooggradige abnormale cellen. Afhankelijk van uw specifieke geval, zal uw arts beslissen hoe verder te gaan.
- Een rapport van geen abnormale cellen komt overeen met een negatieve test, wat betekent dat u gewoon de volgende screening moet ondergaan volgens de richtlijnen voor screening.
- Atypische cellen van onbepaalde betekenis kunnen op drie verschillende manieren worden behandeld:
- Herhaal de HPV/Pap-test over 4-6 maanden,
- Colposcopie: Colposcopie is een procedure die tijdens een bekkenonderzoek wordt uitgevoerd met behulp van een colposcoop, die lijkt op een microscoop. Door azijnzuur op de baarmoederhals te gebruiken en deze met een colposcoop te onderzoeken, kan uw arts abnormale delen van uw baarmoederhals opsporen. Colposcopie is ongemakkelijk, maar niet pijnlijk, en kan worden gedaan in het kantoor van uw gynaecoloog.
- Een biopsie is de enige manier om zeker te weten of u kanker hebt. Het stelt uw arts in staat cellen te verkrijgen die onder een microscoop kunnen worden onderzocht. Zodra het weefsel is verwijderd, zal een patholoog het monster onderzoeken. Een biopsie kan worden uitgevoerd in combinatie met colposcopie.
Uw arts zal beslissen hoe verder te gaan met de behandeling van een Pap-test die abnormale cellen van onbepaalde betekenis laat zien, afhankelijk van de details van uw geval. Als de herhaalde Pap-tests niet normaal zijn, wordt u doorverwezen voor een colposcopie. Als u positief test op HPV, wordt u doorverwezen voor een colposcopie. Over het algemeen zullen de meeste patiënten met laaggradige abnormale cellen of hooggradige abnormale cellen onmiddellijk worden doorverwezen voor colposcopie. Als u zwanger, adolescent, seropositief of postmenopauzaal bent, kan uw arts iets andere aanbevelingen doen. In sommige gevallen zal de Pap-test cellen bevatten die er abnormaal uitzien, maar die afkomstig zouden kunnen zijn van hoger in de baarmoeder. In dat geval bestaat de kans dat er een monster van het baarmoederslijmvlies moet worden genomen. Praat met uw arts over de resultaten van uw Pap-test en de volgende stappen na een afwijkende Pap-test.
Als u symptomen (bloedingen/uitvloeiingen) heeft van baarmoederhalskanker, dan kan de tumor waarschijnlijk worden gezien tijdens een bekkenonderzoek. Telkens wanneer uw arts bij een bekkenonderzoek een baarmoederhalsgezwel kan zien, wordt er een biopsie genomen. Als er bij een colposcopie abnormaal uitziend weefsel wordt gezien, wordt ook daar een biopsie van genomen. Er zijn een paar verschillende manieren om een biopsie te doen:
- Een ponsbiopsie kan worden gebruikt om een klein deel van de baarmoederhals te verwijderen.
- LEEP (loop electrosurgical excision procedure) is een andere methode om een biopsie te doen waarbij een dun plakje van de baarmoederhals wordt verwijderd.
- Conisatie of kegelbiopsie kan worden uitgevoerd. Bij een kegelbiopsie wordt een dikker gedeelte van de baarmoederhals weggenomen en kan de patholoog zien of er kankercellen door de baarmoederhals zijn binnengedrongen. De kegelbiopsie heeft de toegevoegde waarde dat soms een pre-kankerachtige laesie kan worden genezen die is gelokaliseerd op een klein gebied.
Andere tests die als onderdeel van een diagnostisch onderzoek kunnen worden uitgevoerd, zijn bloedonderzoek, leverfunctietests en HIV-tests.
Hoe wordt baarmoederhalskanker in stadia ingedeeld?
Nadat deze tests zijn uitgevoerd, wordt een stadium bepaald om te helpen bij het bepalen van het behandelplan. Het stadium van de kanker, of de omvang van de ziekte, is gebaseerd op informatie die is verzameld met de verschillende tests die zijn uitgevoerd tijdens de diagnose en het onderzoek naar de kanker.
Het stadium van kanker helpt de zorgverlener bij het nemen van beslissingen over de behandeling en het zorgplan. Baarmoederhalskanker wordt geënsceneerd volgens het FIGO-systeem (International Federation of Gynecologists and Obstetricians) en het TNM-systeem (ook wel tumor – knoop – metastase systeem genoemd). De stadia van baarmoederhalskanker lopen van I-IV. In het algemeen geldt: hoe hoger het stadium, hoe ernstiger de kanker. Het stadiëringssysteem is zeer complex en wordt aan het eind van dit artikel ter referentie vermeld. Uw stadium staat vermeld in uw pathologisch rapport – u kunt vragen om een kopie van dit rapport voor uw persoonlijke dossiers. Het stadiëringssysteem is ter inzage opgenomen in de bijlage.
Hoe wordt baarmoederhalskanker behandeld?
Pre-cancereuze laesies
Vrouwen bij wie na colposcopie een biopsie wordt genomen van pre-cancereuze laesies, hebben een paar verschillende opties wat betreft de verdere behandeling. U kunt voor een specifieke optie kiezen, afhankelijk van of u al dan niet van plan bent in de toekomst kinderen te krijgen, uw huidige gezondheidstoestand en levensverwachting, en uw bezorgdheid over de toekomst en de mogelijkheid dat de kanker terugkomt. U moet met uw arts praten over uw angsten, zorgen en voorkeuren.
Als u laaggradige laesies hebt, kunt u ervoor kiezen om geen verdere behandeling te ondergaan, vooral als de biopsie de gehele laesie heeft verwijderd. Als u hiervoor kiest, moet u vaker uw bekken laten onderzoeken en Pap-testen laten doen. Bespreek met uw arts hoe vaak u deze onderzoeken moet laten doen.
Er zijn verschillende manieren om voorstadia van kanker te verwijderen zonder de hele baarmoeder te verwijderen (zodat u in de toekomst geen baby kunt krijgen). Tot de mogelijkheden behoren:
- Cryochirurgie (bevriezen van de abnormale laesie).
- LEEP (dezelfde soort elektrochirurgische procedure die voor biopsies wordt gebruikt).
- Conisatie (het dikkere type biopsie dat weefsel onder het oppervlak krijgt).
- Lasercelverwijdering.
Vrouwen die geen plannen hebben om in de toekomst kinderen te krijgen en bijzonder bezorgd zijn over hun kansen om invasieve kanker te krijgen, kunnen kiezen voor een hysterectomie (een operatie waarbij uw baarmoeder en baarmoederhals worden verwijderd). Deze ingreep is ingrijpender dan een van de eerder genoemde behandelmethoden, maar kan vrouwen die geen kinderen willen krijgen geruststellen.
Chirurgie
Chirurgie wordt meestal toegepast bij baarmoederhalskanker in een vroeg stadium. Het doel van een operatie is om zoveel mogelijk ziekte te verwijderen. Een operatie wordt echter meestal alleen uitgevoerd als alle kanker bij de operatie kan worden verwijderd. Kankers met een grote kans op uitzaaiing naar de lymfeklieren worden niet geopereerd (lymfeklieren zijn kleine stukjes weefsel ter grootte van een erwt die de lymfe, een vloeibaar afvalproduct, filteren en opruimen).
Er zijn een paar verschillende soorten operaties die kunnen worden uitgevoerd. Het soort operatie hangt af van het stadium van de tumor. Chirurgische procedures voor baarmoederhalskanker omvatten:
- Trachelectomie- Verwijdering van de baarmoederhals, de bovenste vagina en weefsel rondom de baarmoederhals. Ook kunnen lymfeklieren in het bekken worden verwijderd.
- Hysterectomie – verwijdering van de baarmoeder en de baarmoederhals. De lymfeklieren in het bekken kunnen ook worden verwijderd. Afhankelijk van de ernst van de ziekte kan het nodig zijn weefsel rond de baarmoeder, een deel van de vagina en de eileiders te verwijderen.
Een van de voordelen van een operatie bij jonge vrouwen is dat de eierstokken soms kunnen blijven zitten. Dit voorkomt dat ze al op jonge leeftijd in de menopauze komen. Ziekten in een hoger stadium worden meestal behandeld met bestraling en chemotherapie, maar soms wordt een operatie toegepast als baarmoederhalskanker terugkomt nadat het al is behandeld.
Een bekkexenteratie is voorbehouden aan terugkerende baarmoederhalskankers. Een bekkenexenteratie is een grote operatie waarbij de baarmoeder, de baarmoederhals, de eileiders, de eierstokken, de vagina, de blaas, het rectum en een deel van de dikke darm worden verwijderd.
Bestralingstherapie
Bestralingstherapie is zeer effectief gebleken bij de behandeling van baarmoederhalskanker. Bij bestraling worden hoogenergetische röntgenstralen gebruikt om kankercellen te doden. Bestralingstherapie is een andere optie naast chirurgie voor baarmoederhalskanker in een vroeg stadium. Gebleken is dat chirurgie en bestraling gelijkwaardige behandelingen zijn voor baarmoederhalskanker in een vroeg stadium. Baarmoederhalskanker in een vergevorderd stadium wordt ook met bestraling behandeld. Bestraling helpt ook om een operatie te vermijden bij patiënten die te ziek zijn om narcose te riskeren. Bestraling heeft het voordeel dat de hele ziekte in het bestralingsveld kan worden behandeld, zodat tijdens dezelfde behandeling zowel lymfeklieren als de primaire tumor kunnen worden behandeld.
Bestralingstherapie voor baarmoederhalskanker kan worden gegeven door een externe bron (buiten de patiënt, bekend als externe straling) of een interne bron (binnen de patiënt, bekend als brachytherapie). De duur van uw behandeling wordt bepaald door uw behandelteam. De behandeling duurt slechts een paar minuten en is pijnloos.
Het type bestralingstherapie dat wordt gebruikt, hangt af van het stadium van uw tumor. Bij alle gevallen van baarmoederhalskanker boven stadium IB is de standaardbenadering van bestraling het gebruik van externe bestraling in combinatie met inwendige brachytherapie. Met brachytherapie (ook wel intracavitaire bestraling genoemd) kan uw bestralingsoncoloog de stralingsdosis op de plaats van de tumor “opvoeren”. Hierdoor wordt de tumor extra geraakt terwijl uw normale weefsels worden ontzien. Dit wordt gedaan door een holle, metalen buis met twee eivormige patronen in uw vagina te brengen. Vervolgens wordt een kleine radioactieve bron in de buis en de patronen geplaatst. Een computer heeft berekend hoe lang de bron daar moet blijven, maar meestal, voor wat lage dosesnelheid (LDR) brachytherapie wordt genoemd, moet u de bron een paar dagen inhouden. Deze procedure wordt in het ziekenhuis uitgevoerd, omdat u gedurende die paar dagen in bed moet blijven.
Een andere vorm van brachytherapie, HDR-brachytherapie (High-Dose-Rate) genoemd, maakt gebruik van krachtiger bronnen die slechts een paar minuten in het lichaam blijven. Hoewel deze optie voor patiënten meestal aantrekkelijker klinkt, is er discussie over de vraag welk type effectiever is en geven sommige instellingen de voorkeur aan het ene boven het andere. Praat met uw zorgverlener over uw mogelijkheden en hun mening over HDR versus LDR voor de behandeling van baarmoederhalskanker.
Een andere toepassing van bestraling is in de palliatieve zorg. Bij patiënten met zeer vergevorderde gevallen van baarmoederhalskanker is het doel van de behandeling het verlichten van de pijn of de symptomen, in plaats van te proberen hun ziekte te genezen.
In elke setting wordt bestraling vaak gecombineerd met chemotherapie, en afhankelijk van uw geval zal uw zorgverlener samen met u beslissen wat de best mogelijke behandeling is voor uw levensstijl en wensen.
Chemotherapie
Ondanks het feit dat tumoren door middel van een operatie zijn verwijderd of met bestraling zijn behandeld, bestaat er altijd een risico op terugkeer omdat er microscopische kankercellen in het lichaam kunnen achterblijven. Om het risico van terugkeer (het terugkomen van de kanker) te verkleinen, kan u chemotherapie worden aangeboden.
Chemotherapie is het gebruik van geneesmiddelen tegen kanker die in het hele lichaam worden toegediend. De meeste patiënten die in goede gezondheid verkeren en bestraald worden voor baarmoederhalskanker stadium IIA of hoger, krijgen naast de bestraling ook chemotherapie aangeboden. Het kan zelfs worden aangeboden voor gevallen in een vroeger stadium, afhankelijk van de patiënt en haar ziekte. Er zijn veel studies die het nut aantonen van het toevoegen van chemotherapie aan bestraling voor het verminderen van de sterfte aan baarmoederhalskanker.
Er zijn veel verschillende chemotherapiemedicijnen, die vaak in combinaties gedurende een reeks van maanden worden gegeven. Afhankelijk van het type chemotherapieregime dat u krijgt, kunt u elke week of om de paar weken medicijnen krijgen. De meest gebruikte schema’s (combinaties) maken gebruik van een geneesmiddel genaamd cisplatine in combinatie met een ander geneesmiddel, meestal etoposide, paclitaxel, topotecan, carboplatine en/of bevacizumab. Pembrolizumab, albumine-gebonden paclitaxel, docetaxel, fluorouracil, gemcitabine, ifosfamide, irinotecan, mitomycine, pemetrexed, en vinorelbine kunnen worden gebruikt als tweedelijnstherapie na recidief. In sommige gevallen, wanneer de tumor bepaalde genetische mutaties vertoont, kan larotrectinib of entrectinib worden gebruikt. Uw tumor zal worden getest op deze mutaties.
Er zijn voor- en nadelen aan elk van de verschillende regimes die uw zorgverlener met u zal bespreken. Op basis van uw eigen gezondheid, uw persoonlijke waarden en wensen, en de bijwerkingen die u mogelijk wilt vermijden, kunt u samen met uw zorgverleners het beste schema voor uw levensstijl samenstellen.
Klinische trials
Er zijn klinische onderzoekstrials voor de meeste soorten kanker en elk stadium van de ziekte. Klinische trials zijn bedoeld om de waarde van specifieke behandelingen vast te stellen. De proeven zijn vaak bedoeld om een bepaald stadium van kanker te behandelen, hetzij als de eerste behandeling die wordt aangeboden, hetzij als een optie voor behandeling nadat andere behandelingen hebben gefaald. Ze kunnen worden gebruikt om medicijnen of behandelingen te evalueren om kanker te voorkomen, eerder op te sporen of de bijwerkingen te helpen beheersen. Klinische proeven zijn uiterst belangrijk om onze kennis over ziekten te vergroten. Het is door klinische proeven dat we weten wat we nu weten, en veel spannende nieuwe therapieën worden momenteel getest. Praat met uw arts over deelname aan klinische trials in uw omgeving. U kunt ook onderzoeken welke klinische trials momenteel open staan via de OncoLink Clinical Trials Matching Service.
Nazorg en overleving
Nadat u bent behandeld voor baarmoederhalskanker, moet u nauwlettend worden gevolgd voor een terugkeer. In het begin zult u vrij vaak follow-upbezoeken ondergaan. Hoe langer u ziektevrij bent, hoe minder vaak u op controle moet komen. Uw arts zal u vertellen wanneer u vervolgbezoeken, Pap-testen en/of scans wilt, afhankelijk van uw geval. Uw arts zal ook regelmatig bekkenonderzoeken doen tijdens uw bezoeken aan de praktijk. Het is heel belangrijk dat u uw zorgverlener op de hoogte stelt van alle symptomen die u ervaart en dat u al uw vervolgafspraken nakomt.
Bevreesdheid voor herhaling, relaties en seksuele gezondheid, de financiële gevolgen van de kankerbehandeling, werkgelegenheidskwesties en copingstrategieën zijn veel voorkomende emotionele en praktische problemen waarmee overlevenden van baarmoederhalskanker te maken krijgen. Uw zorgteam kan hulpbronnen identificeren voor ondersteuning en management van deze uitdagingen tijdens en na de kanker.
De overleving van kanker is een relatief nieuw aandachtspunt in de oncologische zorg. Met bijna 17 miljoen overlevenden van kanker alleen al in de VS, is er behoefte om patiënten te helpen bij de overgang van actieve behandeling naar overleving. Wat gebeurt er daarna, hoe word je weer normaal, wat moet je weten en doen om gezond verder te leven? Een overlevingsplan kan een eerste stap zijn om uzelf voor te lichten over het leven na kanker en u te helpen met kennis te communiceren met uw zorgverleners. Create a survivorship care plan today on OncoLink.
Resources for More Information
National Cervical Cancer Coalition
Provides education about HPV and cervical cancer, support through a “pals” program that links a woman with another woman who has a similar diagnosis.
Foundation for Women’s Cancers
The Foundation offers comprehensive information by cancer type that can help guide you through your diagnosis and treatment. They also offer the ‘Sisterhood of Survivorship’ to connect with others facing similar challenges.
Hope for Two
Dedicated to providing women diagnosed with cancer while pregnant with information, support, and hope.
http://www.hopefortwo.org
Appendix: FIGO Surgical Staging of Cervical Cancer (2018)
|
FIGO Stage |
Description |
|
I |
Cervical carcinoma confined to the cervix (extension to corpus should be disregarded) |
|
IA |
Invasive carcinoma diagnosed only by microscopy. Stromal invasion with a maximum depth of ≤5.0mm |
|
IA1 |
Measured stromal invasion of ≤3.0mm or less in-depth |
|
IA2 |
Measured stromal invasion >3.0mm and ≤5.0mm |
|
IB |
Invasive carcinoma with measured deepest invasion >5 mm (greater than stage IA); lesion limited to the cervix uteri with size measured by maximum tumor diameter. |
|
IB1 |
Invasive carcinoma >5mm depth of stromal invasion and ≤2cm in greatest dimension |
|
IB2 |
Invasive carcinoma >2cm and ≤ 4cm in greatest dimension |
|
IB3 |
Invasive carcinoma >4cm in greatest dimension |
|
II |
Cervical carcinoma invading beyond the uterus but not extended onto the lower third of the vagina or to the pelvic wall |
|
IIA |
Involvement limited to the upper two-thirds of the vagina without parametrial invasion. |
|
IIA1 |
Invasive carcinoma ≤4cm in greatest dimension |
|
IIA2 |
Invasive carcinoma >4cm in greatest dimension |
|
IIB |
Parametrial invasion but not up to the pelvic wall |
|
III |
The carcinoma involves the lower third of the vagina and/or extends to the pelvic wall and/or causes hydronephrosis or non-functioning kidney and/or involves pelvic and/or paraaortic lymph nodes |
|
IIIA |
Tumor involving the lower third of the vagina but no extension to the pelvic wall |
|
IIIB |
Carcinoma involves the lower third of the vagina, with no extension to the pelvic wall |
|
IIIC |
Involvement of pelvic and/or paraaortic lymph nodes (including micrometastases), irrespective of tumor size and extent (with r and p notations). |
|
IIIC1 |
Pelvic lymph node metastasis only |
|
IIIC2 |
Paraaortic lymph node metastasis only |
|
IV |
The carcinoma has extended beyond the true pelvis or has involved (biopsy-proven) the mucosa of the bladder or rectum. A bullous edema, as such, does not permit a case to be allotted to stage IV |
|
IVA |
Spread of the growth to adjacent organs |
|
IVB |
Spread to distant organs |