Classificatie van de ernst van chronische obstructieve longaandoeningen volgens de nieuwe richtlijnen van het Wereldwijd Initiatief voor Chronische Obstructieve Longaandoeningen 2011: COPD Assessment Test Versus Modified Medical Research Council Scale | Archivos de Bronconeumología
Inleiding
Chronische obstructieve longziekte (COPD) treft 9,1% van de Spaanse volwassen bevolking tussen 40 en 69 jaar en is wereldwijd een van de belangrijkste doodsoorzaken door niet-overdraagbare ziekten.1,2 De richtlijnen voor COPD-beheer bepalen dat de diagnose spirometrie moet omvatten. Deze test classificeert de ernst van de ziekte aan de hand van het percentage FEV1 ten opzichte van de voorspelde waarde (FEV1%), en de behandelingsstrategie wordt dienovereenkomstig bepaald.3,4 Deze procedure correleert echter relatief slecht met de mortaliteit en symptomatologie van de patiënt.5 Een multidimensionele evaluatie die niet alleen de longfunctie omvat, maar ook de kwantificering van de symptomen (bv. dyspneuschalen), de voedingsstatus van de patiënt en de inspanningscapaciteit, zoals de BODE-index,6 heeft bijgedragen tot een verandering in de manier waarop deze ziekte wordt waargenomen.7
In de herziening van het Global Initiative for Chronic Obstructive Lung Disease (GOLD 2011) wordt voorgesteld om patiënten te stratificeren op basis van de ernst van de ziekte, waarbij de symptomen worden bepaald met de gemodificeerde Medical Research Council (mMRC) schaal of de gezondheidstoestand met behulp van de COPD Assessment Test (CAT), evenals de voorgeschiedenis van exacerbaties van de patiënt en het post-bronchodilatator (pb) FEV1%.8 Patiënten worden ingedeeld volgens risico: laag risico (pb FEV1%≥50% of 1
%minder symptomen (CAT10 of mMRC 0-1) of meer symptomen (CAT≥10 of mMRC≥2). Er worden dus vier categorieën onderscheiden: A (laag risico, minder symptomen), B (laag risico, meer symptomen), C (hoog risico, minder symptomen), D (hoog risico, meer symptomen). De voorgestelde therapeutische aanpak is verschillend voor elke groep8 (Fig. 1).
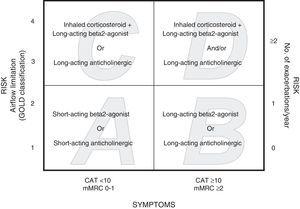
GOUD 2011-categorieën en medicamenteuze behandeling (eerste aanbeveling) voor elke categorie.
Het doel van deze studie was om aan de hand van een observationeel studiecohort (BODE Center, Zaragoza, Spanje) vast te stellen of de keuze van een symptoomschaal (mMRC) of een vragenlijst die de kwaliteit van leven meet (CAT) leidt tot verschillen in de toewijzing aan de verschillende ernstcategorieën en de overeenkomstige therapeutische implicaties.
Patiënten en MethodenStudieopzet
Het BODE Project is een multicenter observationele studie om de natuurlijke geschiedenis van COPD te evalueren. Patiënten werden initieel geselecteerd tussen 1996 en 2000 en werden jaarlijks opgevolgd. Het protocol en de belangrijkste gezondheidsuitkomsten zijn eerder beschreven.6 De diagnose COPD werd vastgesteld volgens de GOLD-criteria8: pbFEV1%/FVC%20 pack-years. Tussen januari 2010 en september 2012 werden 283 nieuwe patiënten geëvalueerd in ons centrum, en deze laatste studiegroep werd gebruikt voor deze analyse.
Procedures
Gestandaardiseerde metingen in het BODE-cohort omvatten demografische gegevens, klinische dossiers en vragenlijsten over gezondheid en kwaliteit van leven, waaronder de CAT en de mMRC.
De CAT-vragenlijst is een zelf in te vullen instrument voor de evaluatie van de levenskwaliteit van COPD-patiënten. Hij bestaat uit 8 items en levert een score op van 0-40; een hogere score wijst op een slechtere gezondheidstoestand.9 De mMRC-dyspneuschaal is een instrument dat de ernst van de dyspneu vaststelt in relatie tot verschillende fysieke taken. Het bestaat uit 5 items en wordt gescoord op een bereik van 0 (geen dyspneu of alleen bij zware inspanning) tot 4 (dyspneu in rust).10
Spirometrie werd uitgevoerd voor en 20-30min na inhalatie van 200μg salbutamol volgens een gestandaardiseerde procedure.11 Alle patiënten voerden een 6-minuten looptest uit.
Toewijzing van patiënten aan de GOLD 2011 categorieën werd onafhankelijk vastgesteld, met behulp van de mMRC-schaal (dyspneu) en de CAT-schaal (kwaliteit van leven). De stratificatieregels bepalen dat eerst de patiënt moet worden gestratificeerd in groep A of C wanneer de mMRC 0-1 is of de CAT-score Fig. 1 is). Vervolgens moet het risico van de patiënt worden vastgesteld volgens een van de twee procedures. Met de ene procedure worden patiënten met pbFEV1%≥50% ingedeeld in categorie A of B (laag risico) en patiënten met pbFEV18 Een exacerbatie werd als ernstig gedefinieerd wanneer de patiënt op de spoedeisende hulp werd gezien of in het ziekenhuis werd opgenomen. Gegevens over eerdere exacerbaties werden verkregen uit vragenlijsten die aan de patiënten werden toegediend en uit de databanken van het intranetsysteem van de Aragon Healthcare Service. Om het risico vast te stellen werd de hoogste index tussen luchtstroombeperking gemeten door pbFEV1% en exacerbatie voorgeschiedenis geselecteerd.
Statistische analyse
Er werd een beschrijvende analyse gemaakt van de karakteristieken van de patiënten die in de serie werden opgenomen. Gegevens over demografische en klinische variabelen, ademhalingsfunctietests en stresstests werden geanalyseerd. Het patiëntencohort werd ingedeeld in vier categorieën, volgens de GOLD 2011 criteria (A, B, C en D), met behulp van de CTA vragenlijst, en als alternatief, de mMRC schaal. De mate van overeenstemming tussen de resultaten verkregen door toepassing van beide methoden op hetzelfde patiëntencohort werd bepaald door berekening van de gewogen kappa-index (κ) (overeenstemming of concordantie tussen ordinale kwalitatieve diagnostische tests). De Spearman-correlatie (niet-parametrische schatter rho ) werd berekend om de consistentie tussen de twee evaluatiemethoden, vastgelegd in de ordinale kwalitatieve schaal, te evalueren. De ANOVA test werd gebruikt om de gemiddelden van de klinische en functionele variabelen in de vier GOLD 2011 categorieën te vergelijken, naargelang de ene of de andere evaluatiemethode werd gebruikt voor het classificeren van de patiënten. Analyses werden uitgevoerd met SPSS 19.0® software.
Resultaten
Van de 283 patiënten die aan de studie deelnamen, waren 260 (92%) mannen en 23 (8%) vrouwen. De gemiddelde leeftijd was 71±12 jaar. De belangrijkste demografische, klinische en functionele variabelen zijn weergegeven in tabel 1. Tabel 2 toont deze variabelen gegroepeerd per geslacht met een evaluatie van eventuele significante verschillen tussen de verschillende geanalyseerde parameters. Bij dit bezoek waren 70 (24,7%) patiënten nog actieve rokers. Het gemiddelde pbFEV1% was 62,4±19,9%. Fig. 2 toont de verdeling van de patiënten volgens hun CAT- en mMRC-waarden; de correlatie werd berekend met de Spearman-coëfficiënt ρ=0,613.
Demografische, Klinische en Functionele Variabelen (Gemiddelde±Standaardafwijking).
| Total | 283 patients |
| Sex | 260 (92%) males; 23 (8%) females |
| Age | 71±12 years |
| BMI | 28.5±4.8 |
| Active smoker | 70 patients (24.7%) |
| PYI | 61.8±36.77 |
| Comorbidities | HT: 152 patients (53.7%); dyslipidemia: 106 (37.5%); diabetes: 53 (18.7%); cardiovascular episodes: 124 (43.8%); no comorbidity: 48 (17%) |
| pbFEV1% | 62.4%±20.3 |
| PBD(+) | 33 patients (11.6%) |
| Baseline SatO2 | 93.9%±6.3 |
| Walking test | 389.2m±96.2 |
| Spirometry results | |
| FVC | 2.8l±0.8 |
| FVC% | 76.8%±19.8 |
| FEV1 | 1.6l±0.6 |
| FEV1% | 57.5%±19.9 |
| FEV1/FVC | 0.54±0.12 |
| FEV1/FVC% | 0.74±0.17 |
| pbFVC | 3.07l±0.86 |
| pbFVC% | 82.8%±19.25 |
| pbFEV1 | 1.7l±0.7 |
| pbFEV1% | 62.4%±20.3 |
| pbFEV1/FVC | 0.55±0.13 |
| pbFEV1/FVC % | 0.75±17.8 |
FEV1%: forced expiratory volume in one second, percentage of predicted value; FVC: forced vital capacity; HT: hypertension; BMI: body mass index; PYI: pack-year index; pb: post-bronchodilator; PBD(+): positive bronchodilator test; SatO2: oxygen saturation.
Demographic, Clinical and Functional Variables by Sex (Mean±Standard Deviation).
| Males | Females | P | |
| n | 260 (92%) | 23 (8%) | |
| Age | 71.3 years±7.5 | 64.5 years±8.6 | NS (P=.3) |
| BMI | 28.6±4.7 | 27.3±7.1 | P |
| Active smoker | 60 (23.1%) | 10 (43.5%) | P |
| PYI | 62.6±33.5 | 53.3±21 | P |
| pbFEV1% | 62.9%±20.1 | 57.5%±21.8 | NS (P |
| PBD(+) | 29 (11.1%) | 4 (17.4%) | NS (P=.36) |
| Baseline SatO2 | 93.3%±6.5 | 93.4%±2.7 | NS (P |
| Walking test | 390.1m±95.1 | 380.3m±111 | NS (P |
FEV1%: forced expiratory volume in one second, percentage of predicted value; BMI: body mass index; PYI: pack-year index; NS: not significant; pb: post-bronchodilator; PBD(+): positive bronchodilator test; SatO2: oxygen saturation.
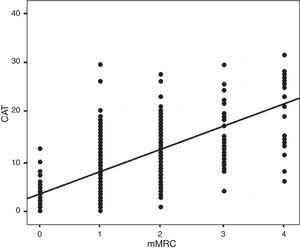
Distribution of mMRC vs CAT. Spearman correlation index: ρ=0.613; P
When the CAT questionnaire was used for classifying patients according to the GOLD 2011 criteria, the percentage distribution of patients to the groups was the following: category A, 34.3%; category B, 19.4%; category C, 19.8%, and category D, 26.5%. When the mMRC was applied, the result was: category A, 36.4%; category B, 17.3%; category C, 18.0%, and category D, 28.3% (Table 3 and Fig. 3).
Cohort GOLD 2011 Classification With CAT and mMRC (Fig. 3).
| GOLD CAT | GOLD mMRC | ||||
| A | B | C | D | Total | |
| A | 81 | 16 | 0 | 0 | 97 (35%) |
| B | 22 | 33 | 0 | 0 | 55 (19%) |
| C | 0 | 0 | 34 | 22 | 56 (20%) |
| D | 0 | 0 | 17 | 58 | 75 (26%) |
| Total | 103 (36%) | 49 (17%) | 51 (18%) | 80 (29%) | 283 (100%) |
Explanatory note: Bij toepassing van de mMRC-schaal werden 103 patiënten als A geclassificeerd; 22 van hen werden bij toepassing van de CAT-vragenlijst als B geclassificeerd. Evenzo werden bij toepassing van de CAT 97 patiënten als A geclassificeerd, maar 16 van hen werden vervolgens met behulp van de mMRC als B geclassificeerd. Met de mMRC werden 49 patiënten als B geclassificeerd, maar 16 van hen waren met de CAT als A geclassificeerd; met de CAT werden 55 patiënten als B geclassificeerd, maar 22 van hen waren met de mMRC als A geclassificeerd. Dezelfde situatie deed zich voor bij de categorieën C en D, naargelang de ene of de andere vragenlijst werd toegepast. Er was geen migratie tussen AB en CD, aangezien dit afhangt van de risicocriteria (AB: laag risico; CD: hoog risico), zoals te zien is in fig. 1.
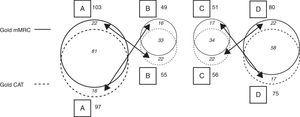
Schematic of migration between GOLD categories depending on results of the application of CAT or mMRC (see distribution of data and explanatory note in Table 3).
When the results from the application of both evaluation methods were examined, it was found that in category A, the classification of 81 patients coincided (83.5% of those classified using CAT and 78.6% of those classified with mMRC). In category B, the classification of 33 patients coincided (60% of those classified with CAT and 67.34% of those classified with mMRC). In categorie C kwamen de classificaties van 34 patiënten overeen (60,7% van degenen die met CAT en 66,7% van degenen die met mMRC waren geclassificeerd). In categorie D kwamen de classificaties van 58 patiënten overeen (77,3% van degenen die met CAT en 72,5% van degenen die met mMRC waren geclassificeerd) (tabel 3 en fig. 3).
De κ coëfficiënt voor de classificatie van de patiënten volgens de 2 methoden was 0,63, hetgeen duidt op een matige mate van overeenstemming. De berekende κ-index was 0,44 voor de 152 patiënten die in de categorieën A en B waren ingedeeld (matig-zwakke graad van concordantie). De index voor de 131 in de categorieën C en D ingedeelde patiënten was 0,38, hetgeen wijst op een nog geringere mate van overeenstemming (zwak). Dit betekent dat voor de categorieën met een laag risico (A en B) een concordantie van 75% werd bereikt, terwijl voor de categorieën met een hoog risico (C en D) de concordantie 70% bedroeg.
The clinical and functional characteristics of the patients in each of the GOLD 2011 categories, depending on the method applied (CAT or mMRC), are shown in Table 4. There were no differences in the categories for age and body mass index (BMI) between patients classified by mMRC or CTA. Only the pack-year index (PYI) was significantly different between category D and the other categories, regardless of whether the classification was made by mMRC or CAT (PP
PP=.003).
Main Clinical and Functional Characteristics of Patients Assigned to GOLD 2011 Categories, as Classified Using mMRC or CAT.
| mMRC | A | B | C | D | CAT | A | B | C | D |
| Age | 70.3 | 70.5 | 69.1 | 72.3 | Age | 71.3 | 68.8 | 70.1 | 71.8 |
| BMI | 28.6 | 29.1 | 28.1 | 28.2 | BMI | 28.5 | 29.3 | 28.1 | 28.2 |
| PYI | 58.4 | 62.3 | 55.7 | 69.7a | PYI | 58.35 | 61.96 | 55.40 | 70.86a |
| pb FEV1% | 75.3 | 69.1 | 56.3 | 44.5 | pb FEV1% | 73.4 | 73.1 | 54.6 | 45.2 |
| Walking test | 414 | 364b | 417 | 344c | Walking test | 400 | 396 | 400 | 354d |
Values expressed as means for each category.
P
P
P
P=.003 vs category C.
Discussion
The recent revision of the GOLD 2011 guidelines proposes that when classifying COPD patients, the medical community should take into consideration not only functional deterioration, but also symptoms and risk of exacerbations.8 Om de mate van functionele achteruitgang vast te stellen, is voorgesteld om dezelfde ernstgraden te handhaven als die momenteel worden gebruikt, d.w.z. mild (pbFEV1%>80%), matig (pbFEV1%≥80% en 1
%≥30% en 1% 30%). Het risico op exacerbatie wordt bepaald door de voorgeschiedenis van exacerbaties in het jaar voorafgaand aan de evaluatie (10 en hoge impact voor CAT≥10). Onze resultaten suggereren dat het gebruik van de ene of de andere evaluatiemethode de toewijzing van een aanzienlijk aantal patiënten aan de ene of de andere categorie van COPD-ernst volgens de nieuwe GOLD-richtlijnen verandert. Deze evaluatiemethoden kunnen dus niet als gelijkwaardig worden beschouwd, aangezien verschillende behandelingsstrategieën worden aanbevolen voor een individuele patiënt, afhankelijk van het gebruik van de ene of de andere methode.
De CAT-vragenlijst geeft de effecten van de ziekte op de gezondheid van de patiënt weer. Het is een specifieke vragenlijst voor de kwaliteit van leven bij COPD5,9,12,13 die niet alleen dyspneu maar ook andere ademhalingssymptomen, zoals de aanwezigheid en intensiteit van hoest of sputum, beoordeelt; de vragenlijst heeft ook in totaal 8 items, waaronder inspanningsvermogen, slaap en activiteiten van het dagelijks leven, die een score tussen 0 en 40 opleveren. De CAT is een eenvoudige vragenlijst en kan in de standaard klinische praktijk worden gebruikt. Het is echter geen diagnostisch instrument; het is bedoeld als aanvulling op de informatie die wordt verkregen uit longfunctiemetingen en er is zeer weinig bekend over de mogelijke prognostische rol van de vragenlijst.14 Deze vragenlijst is met name gevoelig voor het effect van veranderingen in de gezondheidsstatus na exacerbaties16 en het effect van respiratoire revalidatie.17 Een recente review bevestigde de validiteit van de CAT (naast andere specifieke vragenlijsten) als instrument voor het meten van de kwaliteit van leven bij COPD, in het bijzonder in vergelijking met andere generieke instrumenten. Helaas werd in deze review de validiteit van de rol van de mMRC niet geanalyseerd.5 De mMRC is een dyspneuschaal die gemakkelijker te gebruiken is, vooral in de eerstelijnszorg,18 en kan worden opgenomen in multidimensionale instrumenten voor de evaluatie van COPD, zoals BODE6 en ADO (leeftijd, dyspneu, obstructie).19 Bovendien correleert dyspneu beter met de kwaliteit van leven van COPD-patiënten dan objectieve functionele parameters.10,15 Klinische bepaling van dyspneu onthult de functionele capaciteit van de patiënt en geeft een maat voor de effectiviteit van de behandeling,20 terwijl het nauw correleert met 5-jaars overleving bij patiënten met COPD.21 Het heeft ook een groter voorspellend vermogen laten zien met betrekking tot de uitkomst van respiratoire revalidatie, ongeacht de mate van obstructie.6,18,21
Er waren geen significante verschillen in leeftijd, BMI en FEV1 tussen patiënten in de A- en B- en C- en D-groepen, ongeacht of ze waren geclassificeerd met mMRC of CAT. De inspanningscapaciteit van patiënten in de B vs A en D vs C groepen is echter lager wanneer zij worden ingedeeld met mMRC in plaats van CAT. Dit suggereert dat dyspneu veel belangrijker is dan kwaliteit van leven als variabele die het dagelijks leven van COPD-patiënten beïnvloedt.
COPD-patiënten die in ons cohort zijn opgenomen, hebben vergelijkbare demografische, klinische en functionele kenmerken als die uit andere studies die in de literatuur zijn gepubliceerd, en ook de verdeling van de patiënten over de verschillende categorieën is vergelijkbaar.22 In onze serie was de verkregen correlatie tussen het gebruik van de CAT of de mMRC matig (ρ=0,613) en vergelijkbaar met die van een andere cross-sectionele cohortstudie.13 Volgens onze resultaten zou de toepassing van CAT of mMRC voor het classificeren van patiënten naar de nieuwe GOLD 2011 categorieën een herclassificatie betekenen van patiënten in de lage (A en B) en hoge risicocategorieën (C en D). De berekening van de concordantie-index naargelang CAT of mMRC wordt toegepast, is matig-zwak voor de A-B categorieën (κ=0,44), en nog zwakker voor de C-D categorieën (κ=0,38). In relatieve termen komt dit neer op een concordantie van 75% in de categorieën A en B en 70% in de categorieën C en D. Het gebruik van deze twee evaluatiemethoden is dus niet gelijkwaardig en meer dan 25% van de patiënten wordt opnieuw ingedeeld na gebruik van de ene of de andere methode. Dit resultaat heeft aanzienlijke gevolgen voor de behandelingsstrategieën voor heringeschaalde patiënten. De grootste verschillen in behandeling worden gevonden tussen de categorieën A (de aanbevolen eerstelijns medicamenteuze behandeling is gebaseerd op kortwerkende bronchodilatoren) en B (de aanbevolen eerstelijns medicamenteuze behandeling is gebaseerd op langwerkende bronchodilatoren en longrevalidatie). Er waren kleine verschillen tussen de categorieën C en D, die alleen van invloed waren op de alternatieve medicamenteuze behandelingsopties, terwijl de aanbevelingen voor niet-medicamenteuze behandeling hetzelfde zijn.8
Een recente studie die ook de uitkomst van de toepassing van beide evaluatiemethoden vergeleek, kwam tot de conclusie dat de nieuwe GOLD 2011-classificatie wellicht enige aanpassing behoeft. Deze auteurs stellen een nieuw afkappunt voor de toepassing van de mMRC-schaal voor (weinig symptomen=0; meer symptomen≥1).23 Twee andere studies, ook recent, uitgevoerd in Zuid-Korea en in de Verenigde Staten, in zeer verschillende geografische en socioculturele omgevingen die niet te vergelijken zijn met Spanje, verkregen resultaten die identiek zijn met de onze, en trokken vergelijkbare conclusies. Eén van deze studies analyseerde 257 Zuid-Koreaanse patiënten in één centrum, en verkreeg resultaten die gelijkwaardig zijn aan de onze.24 De andere studie was een multicenter studie die 4484 Noord-Amerikaanse proefpersonen met COPD includeerde, als onderdeel van de COPDGene studie. Zij analyseerden de resultaten van de toepassing van de mMRC of de SGRQ-vragenlijst (als surrogaat voor CAT) en concludeerden op vergelijkbare wijze dat de keuze van het ene of het andere instrument voor het meten van symptomen van invloed is op de toewijzing van categorieën.25
In de laatste GOLD 2013-revisie is de evaluatie van COPD-patiënten uitgebreid met de opname van de Clinical COPD Questionnaire (CCQ).26 In het eerste deel van de revisie, Methodologie en samenvatting van nieuwe aanbevelingen, en verder in de sectie Symptoomevaluatie, wordt duidelijk gemaakt dat dit een zelf in te vullen vragenlijst is die speciaal is ontworpen voor het meten van de klinische monitoring van COPD-patiënten. In de herziening wordt onderstreept dat de gegevens de validiteit, betrouwbaarheid en gevoeligheid van deze korte en gemakkelijk af te nemen vragenlijst ondersteunen. Er wordt gespecificeerd dat op basis van de huidige kennis het afkappunt van CCQ=0-1 kan worden overwogen voor het indelen van patiënten in groep A en C, en een resultaat van CCQ>1 kan worden gebruikt voor het indelen van patiënten in groep B of D. De auteurs verklaren echter dat meer studies nodig zijn om het discriminerend vermogen en de praktische implicaties van de CCQ bij het opsporen van exacerbaties in de dagelijkse zorg te valideren. En vervolgens, in het gedeelte over gecombineerde COPD-evaluatie, wordt hetzelfde voorstel voor gecombineerde evaluatie dat in de GOLD 2011-richtlijnen naar voren is gebracht, en dat alleen gebaseerd is op CAT of mMRC voor de symptomatische evaluatie van de mate van COPD-betrokkenheid, gehandhaafd, zonder expliciete vermelding van de CCQ26
De hier gepresenteerde studie heeft bepaalde beperkingen: de steekproefgrootte is relatief klein, hoewel de meerderheid van de studies over COPD-meetinstrumenten een vergelijkbaar of kleiner aantal patiënten heeft.5,24 Aangezien dit geen transversale studie is, werd bovendien de prognostische waarde van de resultaten niet geregistreerd. Evenmin werd een correlatie met comorbiditeiten vastgesteld tussen de verschillende categorieën. Door de patiënten gepresenteerde comorbiditeiten kunnen een significant effect hebben op de ziekteprognose, en moeten ook in aanmerking worden genomen voor de gecombineerde evaluatie van COPD bij een toekomstige herziening van de GOLD-richtlijnen.27
Conclusies
De indeling van COPD-patiënten in categorieën volgens de gecombineerde evaluatie voorgesteld door de GOLD 2011-revisie varieert naargelang de evaluatiemethode gebruikt bij de symptomatische evaluatie van patiënten (CAT of mMRC). Meer dan 25% van de patiënten in de verschillende categorieën wordt heringedeeld als de ene of de andere methode wordt gebruikt, wat verschillen impliceert in de aanbevolen behandelingsstrategie. Longitudinale studies zijn nodig om te evalueren welke evaluatiemethode de patiënt het best classificeert, met aandacht voor de prognostische capaciteit van dergelijke instrumenten.
Conflict of Interests
De auteurs verklaren dat zij geen belangenconflict hebben bij het opstellen van dit manuscript.