Wie funktioniert eine Autobatterie und wie ist sie aufgebaut?
Die traditionelle Funktion der Batterie im Motorraum ist hinlänglich bekannt: Ohne die Batterie lässt sich das Fahrzeug nicht starten. Neben dem Anlasser benötigen auch die Zündkerzen, die Glühkerzen, die Beleuchtung und elektronische Anwendungen elektrische Energie. Doch wie ist eine Batterie aufgebaut und wie funktioniert sie?
Blei-Säure-Batterien: Bestandteile und Aufbau
Vielen Autofahrern wird das hohe Gewicht von Autobatterien erst beim Kauf einer neuen Batterie bewusst. Gewichte von etwa 10,5 kg, bis zu 30 kg sind möglich. Der Grund dafür sind die Bleiplatten in den Batteriezellen.
Komponenten und Aufbau einer Batteriezelle
Positive Elektrode:
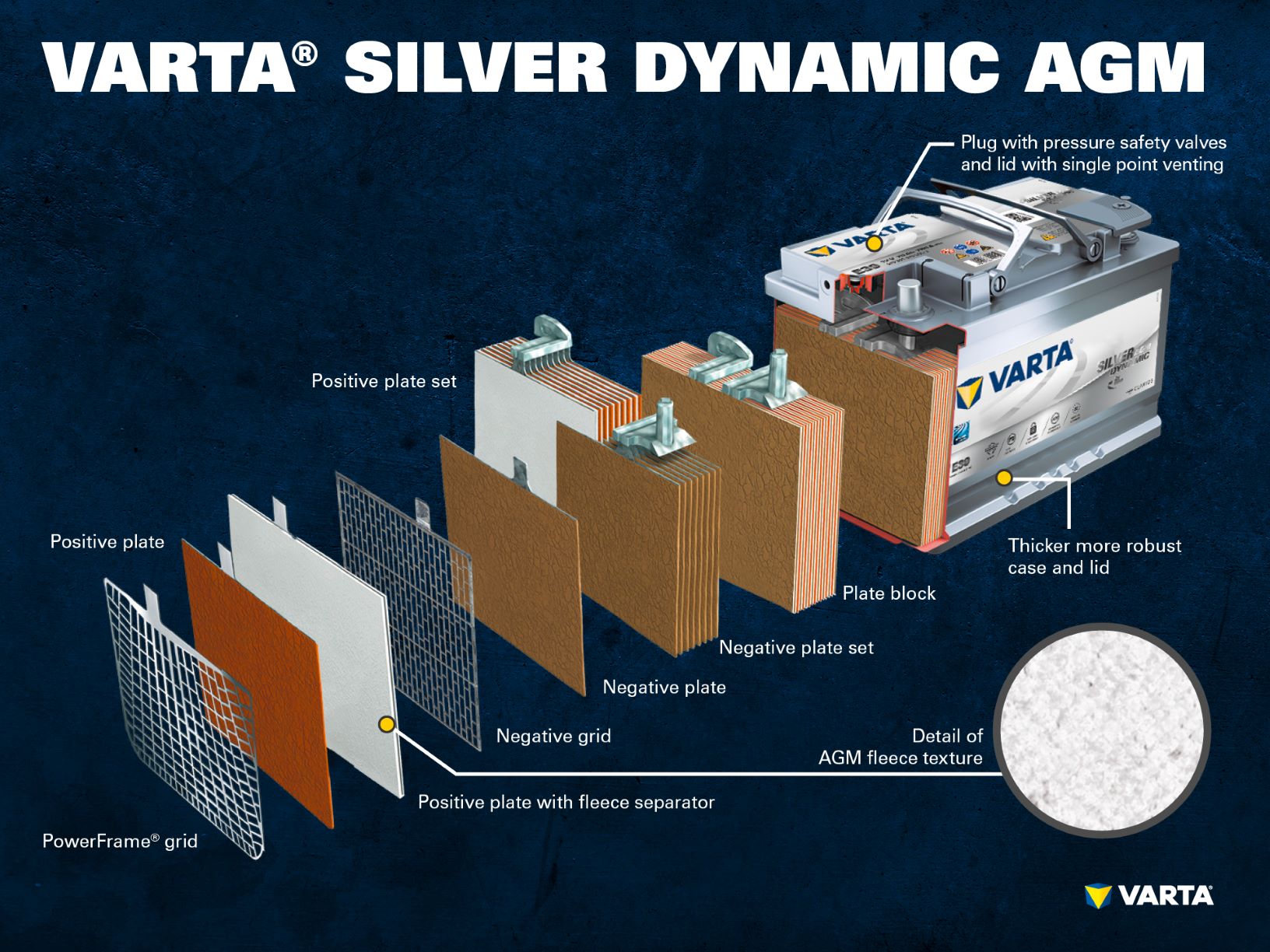
- Positivplatte: In einer Blei-Säure-Batterie besteht die positiv geladene Platte (aktives Material) aus Bleioxid (PbO2), das in einen Elektrolyten eingetaucht ist.
- Positivgitter: Das positive Gitter besteht aus einer Bleilegierung und dient zur Aufnahme des aktiven Materials und als Stromabnehmer.
Negative Elektrode:
- Negative Platte: Die negativ geladene Platte (aktives Material) besteht aus reinem Blei (Pb), das ebenfalls in einen Elektrolyten getaucht ist.
- Negative Platte: Sie besteht wie die positive Platte ebenfalls aus einer Bleilegierung und dient dem gleichen Zweck.
Die unterschiedlich geladenen Elektroden sind durch einen Trennbeutel getrennt.
Der Elektrolyt ist ein Gemisch aus Schwefelsäure (H2SO4) und destilliertem Wasser. Dieser Elektrolyt kann in flüssiger Form (wie in herkömmlichen Nassbatterien oder in der verbesserten EFB-Technologie), in Gelform oder in einer Glasmatte gebunden sein (wie in der AGM-Technologie für neuere Start-Stopp-Anwendungen).
Viele positive Elektroden bilden einen positiven Plattensatz und mehrere negative Elektroden bilden einen negativen Plattensatz. Ein negativer und ein positiver Plattensatz bilden zusammen einen Plattenblock. Ein Plattenblock ist eine Batteriezelle.
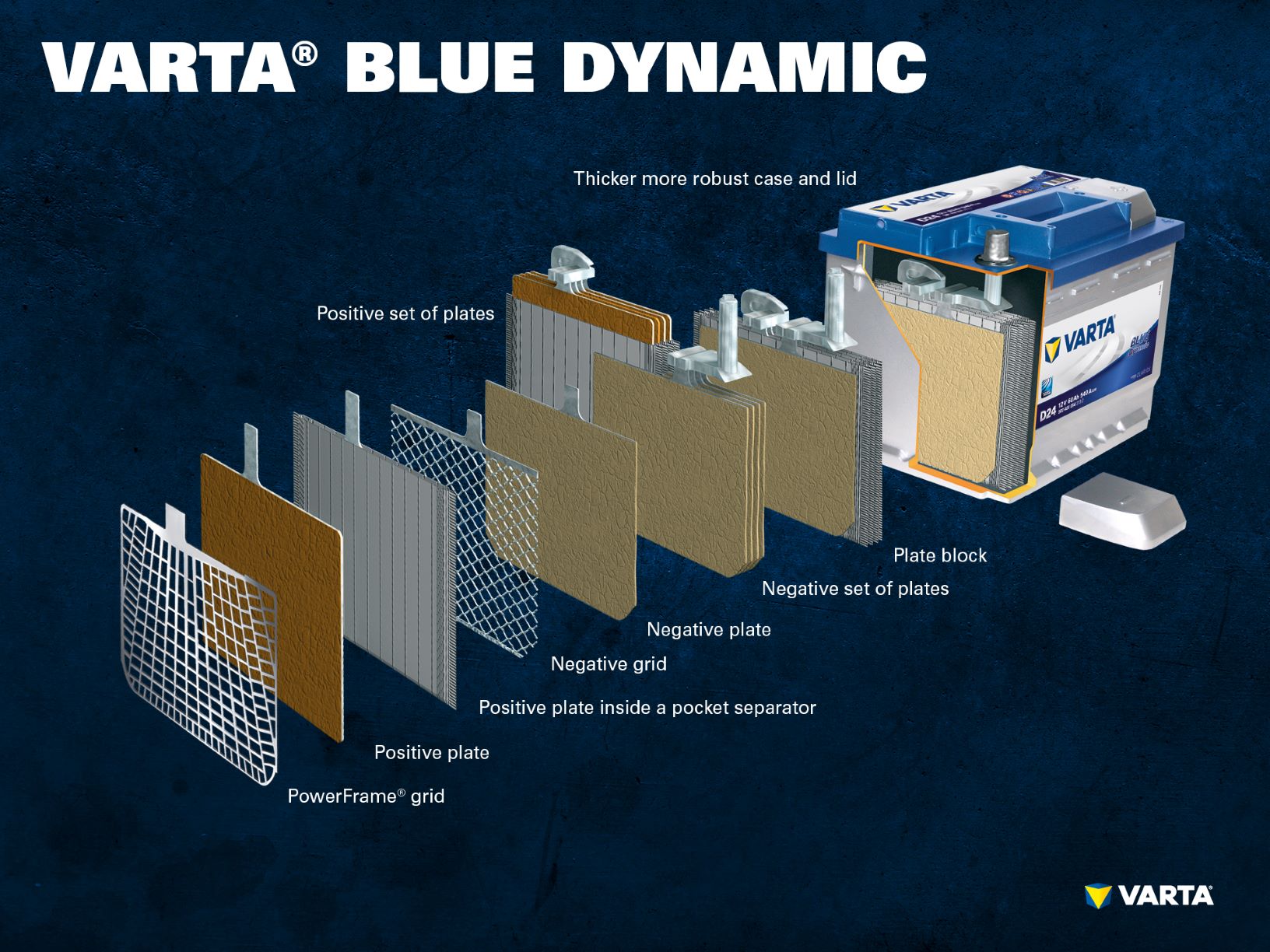
Eine herkömmliche Starterbatterie besteht aus 6 in Reihe geschalteten Zellen mit einer Nennspannung von je 2 V, was bei voller Ladung zu einer Spannung von genau 12,72 V führt. Die Kapazität und die Kaltstartfähigkeit der Batterie ergibt sich aus der Anzahl der Platten pro Zelle.
Faustregel: Je mehr Platten eine Zelle enthält und damit eine größere Fläche bildet, desto größer ist die Kaltstartleistung (CCA), die die Batterie liefern kann. Wird der Platz in der Zelle jedoch für weniger, aber dickere Platten genutzt, erhöht sich die Zyklenfestigkeit. Das bedeutet, dass die Batterie für einen höheren Ladedurchsatz (kontinuierlicher Lade- und Entladevorgang) ausgelegt ist.
Die Zellen befinden sich in einem Gehäuse, das aus säurefestem Kunststoff (Polypropylen) besteht. Dieses ist bei einer herkömmlichen SLI-Batterie mit einem Deckel mit Labyrinthsystem verschlossen, der das Austreten der Batterieflüssigkeit verhindert und die Flüssigkeit vom Gas trennt.
Frühe Batterien hatten Schraubverschlüsse, mit denen sie mit destilliertem Wasser nachgefüllt werden konnten. Moderne Batterien sind völlig wartungsfrei. Wasser muss und darf nicht nachgefüllt werden. AGM-Batterien haben zwar noch „Einwegstecker“, diese dürfen aber unter keinen Umständen geöffnet werden.
Autobatterie-Funktion: Chemische Energie wird zu elektrischer Energie
Eine Autobatterie speichert Energie in chemischer Form und wandelt sie in elektrische Energie um. Bei diesem elektrochemischen Prozess reagieren vier Stoffe miteinander:
- Wasserstoff (H)
- Sauerstoff (O2)
- Blei (Pb)
- Schwefel (S)
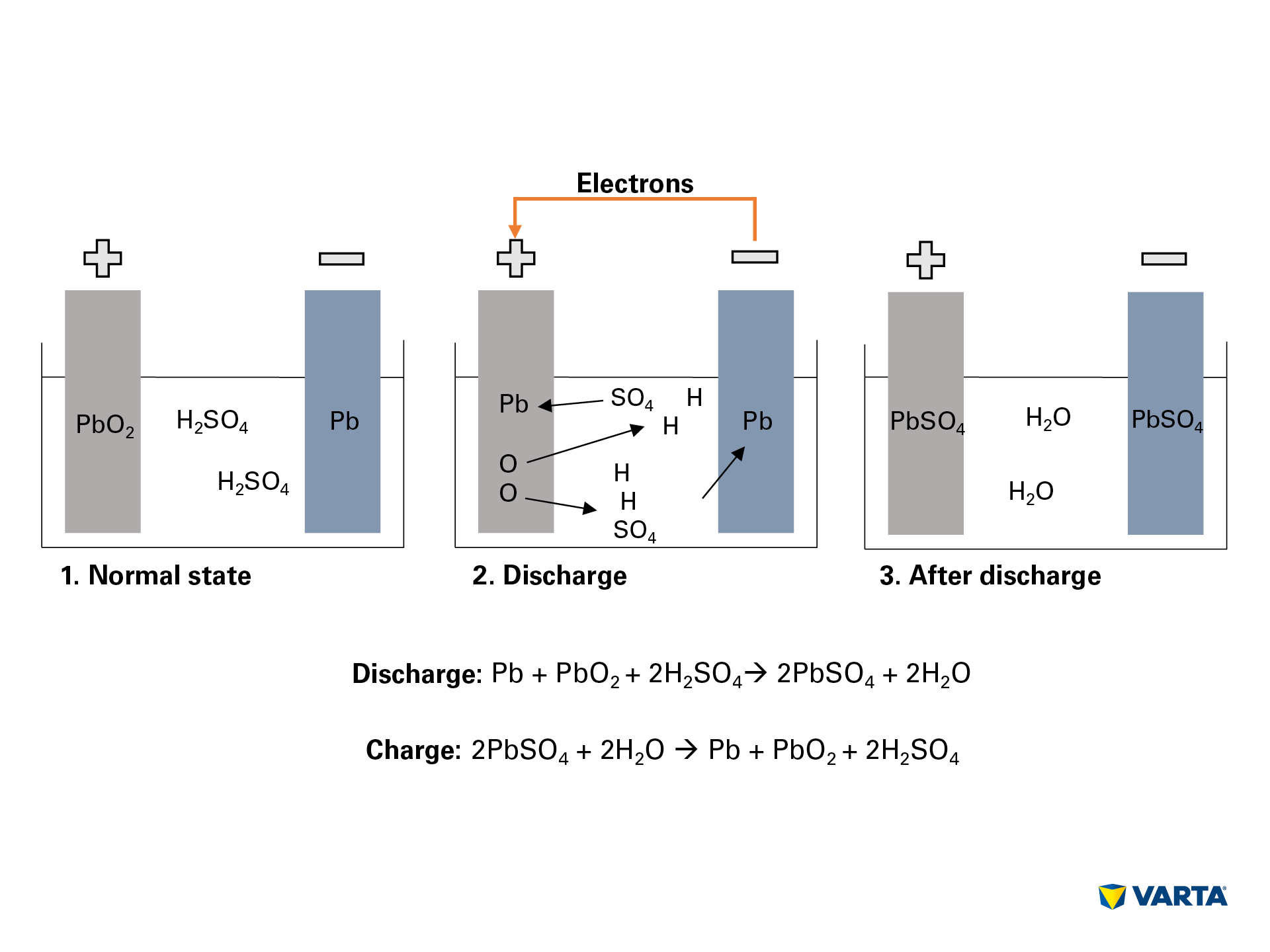
Der Anschluss eines externen Verbrauchers startet die chemische Reaktion in der Batterie:
- Der Elektrolyt, ein Gemisch aus Schwefelsäure (H2SO4) und destilliertem Wasser, zerfällt in positiv geladene Wasserstoff-Ionen (H+) und negativ geladene Sulfat-Ionen (SO42-).
- Gleichzeitig wandern Elektronen (2e-) über den externen Verbraucher von der negativen zur positiven Elektrode.
- Um diesen Elektronenfluss zu kompensieren, wandern Sulfat-Ionen aus dem Elektrolyten in die negative Elektrode, wo sie mit dem Blei (Pb) zu Bleisulfat (PbSO4) reagieren.
- Bleisulfat entsteht auch in der positiven Elektrode: Die Bindung des Sauerstoffs (O2) im Bleioxid (PbO2) wird durch die Übertragung von Elektronen gebrochen und der Sauerstoff geht in den Elektrolyten über. Das verbleibende Blei (Pb) verbindet sich mit dem Sulfat (SO4) aus dem Elektrolyten.
- Dort verbindet sich der Sauerstoff mit dem Wasserstoff und bildet Wasser (H2O). Da die Schwefelsäure durch die Bildung von Bleisulfat verbraucht wird, sinkt die Konzentration der Elektrolytlösung. Wenn die Konzentration der Schwefelsäure unter ein bestimmtes Niveau fällt, muss die Batterie wieder aufgeladen werden.
- Beim Laden laufen die chemischen Prozesse in umgekehrter Reihenfolge ab. Am Ende finden sich die ursprünglichen Elemente wieder: Die positive Elektrode besteht aus Bleisulfat (PbSO4), die negative Elektrode aus reinem Blei (Pb) und der Elektrolyt besteht aus verdünnter Schwefelsäure (H2SO4). Da dieser Umwandlungsprozess mit Verlusten verbunden ist, kann eine Batterie nur eine begrenzte Anzahl von Ladezyklen überstehen. Ihre Nutzungsdauer ist daher begrenzt.
Probleme mit Blei-Säure-Batterien: Sulfatierung und Säureschichtung
Wird eine Batterie mit einer zu niedrigen Spannung geladen oder wird sie immer mit einer zu niedrigen Spannung (unter 80 %) betrieben, kommt es zu einer Säureschichtung, die auch als Schichtung bezeichnet wird. Die Säure im Elektrolyten schichtet sich aufgrund einer schlechten Durchmischung. Unterschiedliche Dichten bewirken eine Schichtung der Schwefelsäure am Boden und des Wassers im oberen Bereich der Batterie. Dadurch kann nur der mittlere Teil des Elektrolyten, also nur ein Drittel, für den Entlade- und Ladevorgang genutzt werden.
Eine mögliche Ursache für die Säureschichtung sind vor allem Kurzstreckenfahrten bei gleichzeitiger Nutzung einer großen Anzahl von elektrischen Verbrauchern. In diesem Fall hat die Lichtmaschine nicht genügend Zeit, die Batterie wieder aufzuladen. 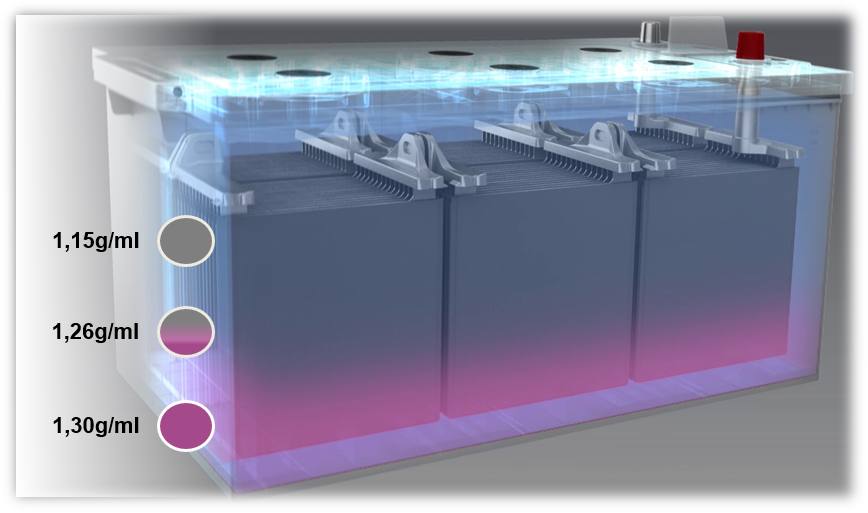
Eine Folge der Säureschichtung ist die Sulfatierung. Tritt diese in der Batterie auf oder wird sie nicht ständig ausreichend geladen, kristallisiert das Bleisulfat (PbSO4) an den Elektroden aus und bildet im Laufe der Zeit größere Kristallstrukturen. Dieser Vorgang wird als „Sulfatierung“ bezeichnet. Die Kristallisation verhindert die Rückumwandlung von Bleisulfat in die ursprünglichen Bestandteile Blei oder Bleioxid, was zu einer Verhinderung der Ladungsaufnahme und zu einer Verringerung der Kaltstartleistung führt.
Scharfe Kristalle können auch die Separatoren beschädigen oder Kurzschlüsse in den Zellen verursachen.
Um diesem Effekt entgegenzuwirken und einem vorzeitigen Ausfall der Batterie vorzubeugen, sollte eine Batterie nie über einen längeren Zeitraum einem niedrigen Ladezustand ausgesetzt werden. Dazu ist es ratsam, die Batterie regelmäßig zu testen und bei Bedarf voll aufzuladen.
Wollen Sie mehr zu diesem Thema wissen? Wie man eine Batterie richtig lädt.
Neue Batterietechnologien: AGM und Lithium-Ionen
Bislang hatten herkömmliche Blei-Säure-Batterien einen hohen Anteil am Markt. Der Markt verändert sich jedoch schnell: Innovative Batterietechnologien für Start-Stopp-Fahrzeuge wie AGM verwenden in einer Matte gebundene Säure, um eine höhere Zyklenstabilität und eine zuverlässige Leistung in Fahrzeugen mit erhöhtem Energiebedarf zu gewährleisten. Ein weiterer Vorteil von AGM: Durch die gebundene Säure ist keine Säureschichtung mehr möglich.
Eine neue Generation von Autobatterien für Micro-Hybrid-Fahrzeuge arbeitet mit 48V und verwendet Zellen mit Lithium-Ionen-Technologie.