Appliquer les géosciences aux défis les plus importants de l’Australie
Introduction

Feuilles d’aluminium. Source : Wikimedia Commons
L’aluminium est partout autour de vous – des objets du quotidien comme une canette de boisson gazeuse aux avions qui vous survolent. L’aluminium est l’un des matériaux les plus utiles connus de l’homme. Il peut être allié (mélangé) à presque tous les autres métaux pour créer des matériaux aux propriétés utiles. Les métaux alliés à l’aluminium sont tous très solides tout en étant légers et résistants à la rouille.
Après l’oxygène et le silicium, l’aluminium est le troisième élément le plus abondant dans la croûte terrestre (8,2 %) et de loin le métal le plus abondant. Contrairement aux métaux tels que le cuivre, l’or, le plomb, le fer et le zinc, utilisés par l’homme depuis des milliers d’années, l’aluminium n’est utilisé couramment que depuis un peu plus de 100 ans. Cela s’explique par le fait que l’aluminium ne se trouve jamais à l’état pur dans la nature. Ainsi, alors que les humains connaissaient les composés de l’aluminium, ils n’ont découvert comment extraire l’aluminium métal qu’à la fin des années 1800.
L’aluminium peut être extrait (de manière peu rentable) de certaines argiles, mais le minerai d’aluminium le plus courant est un matériau appelé bauxite. Il faut d’abord extraire le minerai d’aluminium, puis la bauxite est raffinée en alumine (oxyde d’aluminium). De grandes quantités d’électricité sont utilisées pour fondre l’alumine en aluminium métallique.
Propriétés
L’aluminium est un métal de couleur argentée que l’on ne trouve jamais seul dans la nature. Il est très léger (environ un tiers du poids du cuivre) tout en étant solide ; certains alliages sont même plus solides que l’acier. L’aluminium est à la fois malléable (il peut être pressé en forme) et ductile (il peut être battu et étiré en fil). L’aluminium est un très bon conducteur thermique et électrique. Il est également très résistant à la rouille et n’est pas toxique. L’aluminium peut être allié à presque tous les autres métaux. L’aluminium est inflammable, non magnétique et ne produit pas d’étincelles. These properties have made it an important metal in the modern world. As aluminium is such a reactive metal, you might think it would rust badly and therefore be useless. However, pure aluminium reacts very quickly with air or water to form a thin, almost invisible layer of aluminium oxide on its surface, which then acts as a protective coating preventing any further ‘rusting’.
|
The Properties of Aluminium |
|
|---|---|
|
Chemical symbol |
Al – from the Roman word Alumen – the word for the aluminium-potassium compound alum |
|
Ore |
Bauxite |
|
Relative density |
2.7 g/cm3 |
|
Hardness |
2.75 on Mohs scale |
|
Malleability |
High |
|
Ductility |
High |
|
Melting point |
660°C |
|
Boiling Point |
2470°C |
Uses

Aluminium-bodied Austin « A40 Sports » (c. 1951). Source : Wikimedia Commons
Aluminium is smelted from alumina which is refined from bauxite ore. All three products have a number of uses.
More than 90% of the world’s bauxite production is used to make alumina with most of the remaining 10% used by the abrasive, refractory and chemical industries. Bauxite is also used in the production of high-alumina cement, as an absorbent or catalyst by the oil industry, in welding rod coatings and as a flux in making steel and ferroalloys.
Alumina’s primary use is as feedstock for aluminium smelters, however it is also used for other industrial purposes. It is used in glass, porcelain and in metallic paints, such as those sprayed on cars. Elle est également utilisée dans la production d’isolateurs de bougies d’allumage, comme composant de carburant pour les propulseurs à poudre des fusées, comme charge pour les plastiques, comme abrasif (elle est moins chère que le diamant industriel) et dans les raffineries de métaux où elle est utilisée pour convertir les gaz résiduels toxiques de sulfure d’hydrogène en soufre élémentaire.
L’alumine qui se trouve à l’état naturel et cristallin est appelée corindon minéral. Parfois, les cristaux de corindon sont contaminés par des traces de chrome, de fer, de titane, de cuivre ou de magnésium. On appelle ces cristaux des rubis et des saphirs.
Après le fer et l’acier, l’aluminium est le métal le plus utilisé sur Terre. Il est souvent allié au cuivre, au zinc, au magnésium, au manganèse ou au silicium et l’ajout de petites quantités de zirconium, d’hafnium ou de scandium à ces alliages améliore nettement leur résistance. L’aluminium lui-même a un large éventail d’utilisations, de la construction aéronautique spécialisée aux articles de tous les jours comme les couteaux et les fourchettes. Certaines de ces utilisations sont énumérées dans le tableau ci-dessous.
|
Use |
Description |
|---|---|
|
Building and construction |
Cladding, doors, window frames, awnings and bridge rails as aluminium is strong, light, easily shaped and resistant to rust. |
|
Transport |
Parts for cars, trucks, buses, aircraft, ships, rail and trams as aluminium is strong, light, easily shaped and resistant to rust. |
|
Appliances |
Fridges, washing machines, lawn mowers etc. due to its strength, malleability and rust resistance. |
|
Heating and ventilation |
Heating and cooling systems as aluminium is a good conductor of heat. |
|
Packaging |
Kitchen foil, packaging foil, cans and containers (worldwide, four out of every five drink cans are made of aluminium) as aluminium can be rolled into very thin sheets and is non-toxic. |
|
Electrical and communications |
Power transmission including towers, electrical conduits, superconductors, machinery and equipment, telephone cables and capacitors because of aluminium’s ability to conduct electricity. |
|
Other |
Utensils (cutlery, pans), industrial machinery, chemical industry, production of steel, antiperspirants, furniture, reflectors in telescopes, making high octane petrol, road signs, antacids and jewellery due to its many useful properties. |
History
Around 5300 BC: The Persians made extra strong pots from clay containing aluminium oxide.
Around 2000 BC: The ancient Egyptians and Babylonians used potassium aluminium sulphate KAl(SO4)2 as a medicine to reduce bleeding. It was sourced from naturally occurring deposits in Greece and Turkey. The ancient Romans called this medical compound « alum », which is where we get the modern day word and symbol from. Il est encore utilisé aujourd’hui pour arrêter les saignements.
Moyen-âge : La plupart de l’alun provenait du territoire papal de Tolfa, mais le prix a chuté de façon spectaculaire lorsqu’un important gisement de schiste d’alun a été découvert dans le Yorkshire au début des années 1600. Au cours des siècles suivants, l’alun a été utilisé dans deux domaines principaux : comme agent de conservation du papier et comme agent de fixation pour la teinture des tissus.
1808 : L’Anglais Sir Humphry Davy tente d’extraire l’aluminium par électrolyse. Il échoue mais établit son existence et lui donne son nom.
1821 : Le géologue français Pierre Berthier découvre un matériau riche en aluminium près du village des Baux en Provence, en France. Elle fut nommée bauxite d’après le village.
1825 : Hans Christian Oersted, au Danemark, produit de l’aluminium impur en chauffant du chlorure d’aluminium avec de l’amalgame de potassium.
1827 : Le chimiste allemand Friedrich Wöhler extrait l’aluminium sous forme de poudre en faisant réagir du potassium avec du chlorure d’aluminium anhydre en améliorant le procédé d’Oersted.
1855 : Le chimiste français Henri Saint-Claire Deville réussit à obtenir une barre d’aluminium solide en utilisant du sodium au lieu du potassium, plus coûteux. La barre d’aluminium était considérée comme si précieuse qu’elle a été exposée la même année aux côtés des joyaux de la couronne française.
1886 : Deux scientifiques sur des continents distincts (Charles Hall en Amérique et Paul Héroult en France) ont découvert indépendamment une méthode économique pour produire de l’aluminium par électrolyse dans de la cryolite (fluorure d’aluminium de sodium) fondue. Incidemment, tous deux sont nés en 1864 et tous deux sont morts en 1914.
1887 : Le chimiste autrichien Karl Josef Bayer, travaillant en Russie, met au point une méthode pour extraire l’alumine de la bauxite.
1888 : Hall fonde la Pittsburgh Reduction Company (connue sous le nom d’Alcoa depuis 1907).
1890 : Les découvertes de Hall-Héroult et de Bayer avaient fait chuter le prix de l’aluminium de 80%. En 1888, l’aluminium coûtait 4,86 dollars américains la livre. En 1893, il était de 0,78 $ US par livre et à la fin des années 1930, il ne coûtait que 0,20 $ US par livre et avait plus de 2000 utilisations.
1900 : Seulement 8000 tonnes d’aluminium ont été produites mais 100 ans plus tard, 24,5 millions de tonnes ont été produites et en 2016, on estime que 57,6 millions de tonnes ont été produites.

L’avion de chasse F-16 a été conçu pour être relativement peu coûteux à construire et plus simple à entretenir que les chasseurs de la génération précédente. La cellule est construite avec environ 80 % d’alliages d’aluminium de qualité aéronautique, 8 % d’acier, 3 % de matériaux composites et 1,5 % de titane. Source : Wikimedia Commons, Master Sgt. Andy Dunaway
1911 : Le chimiste allemand Alfred Wilm met au point d’importants alliages d’aluminium suffisamment solides pour la fabrication d’articles tels que les avions. La demande d’aluminium était importante pendant la Seconde Guerre mondiale et la guerre de Corée, car les avions étaient auparavant fabriqués en bois et en tissu.
1922 : La feuille d’aluminium est fabriquée.
1955 : La première fonderie d’aluminium d’Australie a été ouverte à Bell Bay, en Tasmanie.
1958 : Les canettes de boissons gazeuses en aluminium sont produites pour la première fois.
1961 : Alcoa forme Alcoa of Australia.
1963 : Alcoa of Australia ouvre la première raffinerie d’alumine d’Australie à Kwinana en Australie occidentale, suivie de Pinjarra en 1972 et de Wagerup en 1984.
Aujourd’hui : En 2016, on estime que 57,6 millions de tonnes d’aluminium ont été produites. C’est plus que tous les autres métaux non ferreux réunis. L’Australie exploite la bauxite dans le Queensland, l’Australie occidentale, le Territoire du Nord et la Tasmanie et est le premier producteur mondial de bauxite. L’Australie est également un leader mondial dans la production d’alumine et d’aluminium. Les trois raffineries d’Australie occidentale fournissent 45% de l’alumine australienne et 11% du total mondial, ce qui en fait la plus grande source unique d’alumine au monde.
Formation

Bauxite de Weipa, R30128. Source : Geoscience Australia.
La bauxite est le minerai d’aluminium le plus courant. La bauxite se présente sous la forme d’une couverture ou d’une couverture altérée, appelée latérite ou duricrust, sur une variété de roches contenant de l’alumine. Elle se forme lorsque de grandes quantités de pluie lessivent les éléments les plus mobiles de la roche hôte, laissant l’aluminium relativement immobile avec un peu de silicium, de fer et de titane. En raison de la façon dont il se forme, les gisements de bauxite peuvent être très étendus et se trouvent sur presque tous les continents.
Les principaux minéraux d’aluminium de la bauxite sont la gibbsite , la boehmite et la diaspore, qui est un polymorphe (forme alternative) de la boehmite mais qui est plus dense et plus dur. L’alumine pure (Al2O3) contient 52,9% d’aluminium et 47,1% d’oxygène. La bauxite peut être très dure ou aussi molle que de la boue et peut se présenter sous forme de terre compactée (friable et cimentée), de petites boules (pisolites) ou de matériau creux en forme de brindille (tubules). Ses couleurs peuvent être chamois, rose, jaune, rouge ou blanc, ou toute combinaison de ces couleurs. L’aluminium est également présent dans de nombreuses pierres précieuses telles que la turquoise, les rubis, les saphirs, les émeraudes, les topazes, le jade et les aigues-marines.
Ressources
Le minerai de bauxite contient des niveaux suffisamment élevés d’oxydes d’aluminium et des niveaux suffisamment faibles d’oxyde de fer (Fe2O3) et de silice (SiO2) pour être économiquement exploitable. La quantité de silice réactive est particulièrement importante, car cette forme de silice consomme la soude caustique nécessaire à la fabrication de l’alumine ; une faible quantité de silice réactive est donc souhaitable. Les autres sources potentielles d’aluminium comprennent une variété de roches et de minéraux tels que le schiste et l’ardoise alumineux, la roche de phosphate d’aluminium et les argiles à haute teneur en alumine.
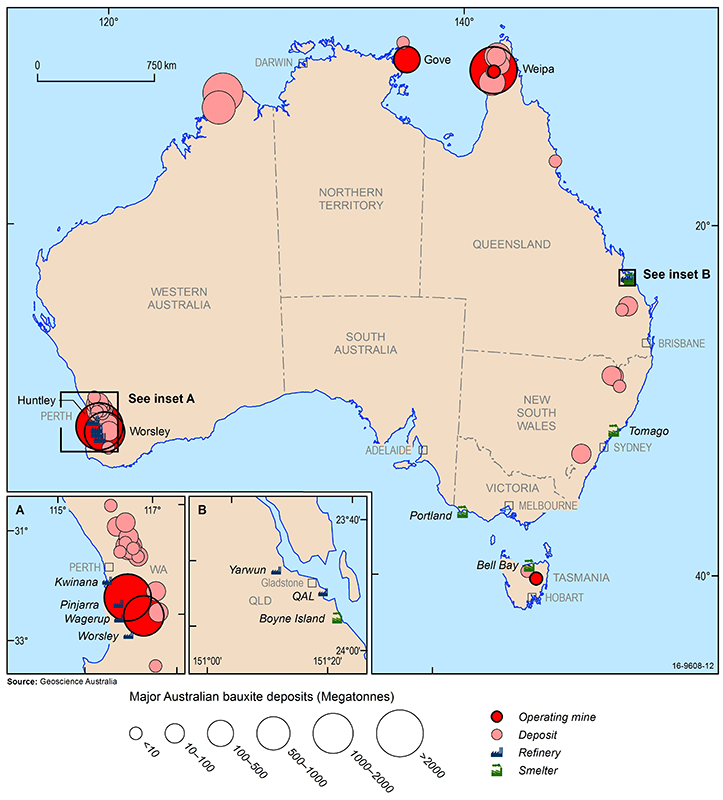
Les principaux gisements de bauxite, mines, raffineries d’alumine et fonderies d’aluminium d’Australie (2016). Source: Geoscience Australia.
Les plus grandes ressources économiques de bauxite au monde se trouvent en Guinée, en Australie, au Brésil, au Vietnam et en Jamaïque. En Australie, la bauxite est extraite à partir d’exploitations à ciel ouvert établies à Weipa dans le Queensland, à Gove dans le Territoire du Nord et dans la Darling Range en Australie occidentale. En outre, de nouvelles mines ont récemment commencé à fonctionner dans la région de Cape York dans le Queensland et dans le centre de la Tasmanie. D’autres gisements de bauxite se trouvent dans le nord de l’Australie occidentale, en Nouvelle-Galles du Sud et dans l’est du Queensland, mais leur exploitation n’est actuellement pas rentable.
Les raffineries d’alumine de l’Australie sont situées en Australie occidentale (Kwinana, Wagerup, Pinjarra et Worsely) et au Queensland (QAL et Yarwun) et ses fonderies d’aluminium sont situées en Tasmanie (Bell Bay), au Queensland (Boyne Island), dans l’État de Victoria (Portland) et en Nouvelle-Galles du Sud (Tomago). La Chine est le plus grand consommateur d’aluminium au monde et, malgré une forte production intérieure, elle importe de grandes quantités d’alumine et de bauxite brute, représentant plus de 40 % de la consommation mondiale. Les autres grands marchés de l’aluminium sont les États-Unis d’Amérique, le Japon et l’Europe, mais ces régions possèdent peu de gisements économiques de bauxite et dépendent également des importations de bauxite et d’alumine pour leurs raffineries d’alumine et leurs fonderies d’aluminium.
Plus d’informations sur les ressources et la production.
Extraction minière
L’extraction de l’aluminium métal se déroule en trois étapes principales¿l’extraction du minerai de bauxite, le raffinage du minerai pour récupérer l’alumine et la fusion de l’alumine pour produire de l’aluminium. La bauxite est exploitée par des méthodes de surface (exploitation à ciel ouvert) dans lesquelles la couche arable et les morts-terrains sont enlevés par des bulldozers et des grattoirs. La terre arable est ensuite stockée et utilisée plus tard pour revégétaliser et restaurer la zone une fois l’exploitation terminée. La bauxite sous-jacente est exploitée par des chargeurs frontaux, des pelles mécaniques ou des excavateurs hydrauliques. Certains minerais de bauxite sont simplement broyés, séchés et expédiés. D’autres bauxites sont traitées après concassage par lavage pour éliminer une partie de l’argile, de la silice réactive et des déchets de sable ; puis elles sont séchées dans des fours rotatifs. Le minerai est chargé dans des camions, des wagons ou sur des bandes transporteuses et transporté vers des navires ou des raffineries.
Un certain nombre de facteurs du cycle de production de l’aluminium ont trait à l’environnement et des ressources considérables sont allouées pour minimiser l’impact de l’exploitation minière, du raffinage et de la fusion sur le milieu environnant. La réhabilitation des mines est effectuée en faisant tout son possible pour que la zone retrouve au moins son état d’origine. La manipulation et l’élimination des boues rouges provenant des raffineries sont effectuées avec précaution. Cette boue est généralement pompée dans des barrages qui sont scellés avec des matériaux imperméables pour éviter la pollution de la campagne environnante.
Traitement
Dans presque toutes les exploitations commerciales, l’alumine est extraite de la bauxite par le procédé de raffinage Bayer. Ce procédé, découvert par Karl Josef Bayer en 1888, comprend quatre étapes.
Digestion : la bauxite finement broyée est introduite dans une unité chauffée à la vapeur appelée digesteur. Là, elle est mélangée, sous pression, à une solution chaude de soude caustique. L’oxyde d’aluminium de la bauxite (et la silice réactive) réagit avec la soude caustique en formant une solution d’aluminate de sodium ou liqueur verte et un précipité de silicate d’aluminium de sodium.
Clarification : la liqueur verte ou solution contenant de l’alumine est séparée des déchets¿les oxydes de fer non dissous et la silice qui faisaient partie de la bauxite d’origine et qui constituent maintenant les déchets de sable et de boue rouge. Cette étape se déroule en trois temps : tout d’abord, les déchets grossiers de la taille d’un sable sont retirés et lavés pour récupérer la soude caustique ; ensuite, les boues rouges sont séparées ; enfin, la liqueur verte restante est pompée à travers des filtres pour éliminer toute impureté résiduelle. Le sable et la boue sont pompés ensemble vers des lacs de résidus et la liqueur verte est pompée vers des échangeurs de chaleur où elle est refroidie de 1000°C à environ 650-790°C.
Précipitation : l’alumine est précipitée de la liqueur sous forme de cristaux d’hydrate d’alumine. Pour ce faire, la solution de liqueur verte est mélangée dans de grands récipients de précipitation avec de petites quantités d’alumine cristalline fine, ce qui stimule la précipitation d’hydrate d’alumine solide à mesure que la solution refroidit. Une fois terminé, l’hydrate d’alumine solide passe à l’étape suivante et la liqueur restante, qui contient de la soude caustique et un peu d’alumine, retourne dans les digesteurs.
Calcination : l’hydrate d’alumine est lavé pour éliminer toute liqueur restante, puis séché. Enfin, il est chauffé à environ 1000°C pour chasser l’eau de cristallisation, laissant l’alumine – un matériau sec, blanc pur, sableux. Une partie de l’alumine peut être laissée sous forme d’hydrate ou faire l’objet d’un traitement supplémentaire pour l’industrie chimique.
L’alumine est transformée en aluminium par un procédé de fusion. Toute la production commerciale d’aluminium est basée sur le procédé de fusion de Hall-Héroult, dans lequel l’aluminium et l’oxygène présents dans l’alumine sont séparés par électrolyse. L’électrolyse consiste à faire passer un courant électrique dans une solution fondue d’alumine et de cryolite (fluorure d’aluminium sodique) naturelle ou synthétique. La solution fondue est contenue dans des cellules de réduction ou des pots dont le fond est garni de carbone (la cathode) et qui sont connectés en série électrique appelée potline. Insérées dans le haut de chaque pot, des anodes de carbone dont le fond est immergé dans la solution fondue.
Le passage d’un courant électrique provoque la combinaison de l’oxygène de l’alumine avec le carbone de l’anode en formant du gaz carbonique. L’aluminium métallique fondu restant s’accumule à la cathode, au fond de la marmite. Périodiquement, il est siphonné et transféré dans de grands fours de maintien. Les impuretés sont éliminées, des éléments d’alliage ajoutés et l’aluminium fondu est coulé en lingots.
Le processus de fusion est continu. Au fur et à mesure que la teneur en alumine du bain de cryolithe diminue, on en ajoute davantage. La chaleur générée par le passage du courant électrique maintient le bain de cryolithe à l’état fondu afin qu’il dissolve l’alumine. Une grande quantité d’énergie est consommée au cours du processus de fusion ; de 14 000 à 16 000 kilowattheures d’énergie électrique sont nécessaires pour produire une tonne d’aluminium à partir d’environ deux tonnes d’alumine. L’aluminium est parfois qualifié d' »électricité solide » en raison de la grande quantité d’énergie utilisée pour sa production. La disponibilité d’une électricité bon marché est donc essentielle pour une production économique.
Les lingots d’aluminium sont produits sous différentes formes et tailles en fonction de leur utilisation finale. Ils peuvent être laminés en plaques, feuilles, pellicules, barres ou tiges. Ils peuvent être étirés en fils qui sont toronnés en câbles pour les lignes de transmission électrique. Des presses extrudent les lingots en des centaines de formes différentes, utiles et décoratives, ou des usines de fabrication peuvent les transformer en grandes formes structurelles.