Projets scientifiques pour les débutants : Chimie
Chimie
Sel ou sucre : Lequel se dissout le plus vite dans différents liquides
Les solutions ne sont rien d’autre que des mélanges de différents composés ou éléments. Vous rencontrez des solutions tous les jours sans même vous en rendre compte.
Même l’air que vous respirez… qui contient de l’eau… est une solution d’un liquide et d’un gaz. Si vous avez bu un soda aujourd’hui, vous avez en fait bu de la solution d’un gaz dissous dans de l’eau aromatisée. Si vous portez un bracelet en argent sterling, vous portez une solution de deux métaux.
Dans cette expérience, vous allez travailler avec une solution liquide, qui est l’un des trois types de solutions. Les autres types sont les solutions gazeuses et les solutions solides.
Alors, quel semble être le problème ?
Un soluté est la substance ? solide, liquide ou gazeuse ? qui se dissout. Un solvant ? qui peut également être un solide, un liquide ou un gaz ? est la substance qui effectue la dissolution. Une solution est un mélange uniforme d’un soluté (généralement un solide) dissous dans un solvant (généralement un liquide).
Lorsque vous remuez une cuillerée de sucre dans un verre d’eau, vous formez une solution. Ce type de solution liquide est composé d’un soluté solide, qui est le sucre, et d’un solvant liquide, qui est l’eau. Comme les molécules de sucre se répartissent uniformément dans l’eau, le sucre se dissout.
Mélanger un liquide dans un gaz permet d’obtenir un autre type de solution, appelée solution gazeuse. Un exemple de ce type de solution est l’humidité. L’humidité est de l’eau (un liquide) dissoute dans l’air (un gaz).
Réfléchissez à la façon dont un morceau de sucre se dissout dans l’eau, par rapport à un paquet de sucre en vrac. Le cube se dissout plus lentement car moins de molécules de sucre sont initialement en contact avec l’eau.
Dans une solution solide, comme l’argent sterling, le cuivre qui a été chauffé à haute température est mélangé à l’argent qui a également été chauffé jusqu’à ce qu’il fonde. Le cuivre est le soluté, c’est-à-dire la substance qui va se dissoudre dans le solvant. L’argent est le solvant.
Le type de solution est déterminé par l’état de la matière du solvant. Si la substance qui effectue la dissolution est un liquide, la solution est appelée solution liquide. Si le solvant est un gaz, la solution est appelée solution gazeuse. Et vous avez deviné juste : Un solvant solide formera une solution solide.
Vous pouvez vérifier la taille des cristaux de sel et de sucre au microscope ou à la loupe, ce qui vous permettra également de voir leurs formes. Si vous dessinez ce que vous voyez, en utilisant un crayon pour pouvoir illustrer l’ombrage, vous pourriez inclure l’illustration dans le cadre de l’affichage final de votre projet de foire scientifique.
Il y a quelques facteurs qui augmentent généralement la quantité de soluté qui peut être dissoute. Si vous voulez dissoudre plus de sucre dans la même quantité d’eau, par exemple, vous pourriez chauffer l’eau. Vous pourriez également broyer le sucre en plus petites particules pour augmenter sa surface, ou vous pourriez remuer le mélange.
Depuis des années que vous utilisez du sel et du sucre sur vos aliments, vous avez probablement remarqué que chaque morceau de sel ?qui est en fait un cristal… est un peu plus petit que chaque morceau de sucre, qui est également un cristal.
Une molécule est constituée de deux éléments ou plus qui sont combinés chimiquement. Une molécule de sel contient du sodium et du chlore, qui sont combinés chimiquement pour donner du chlorure de sodium. La formule chimique de ce sel est NaCl. Une molécule de sucre contient du carbone, de l’hydrogène et de l’oxygène. La formule chimique du sucre est C12H22O11.
Le problème que vous allez tenter de résoudre dans cette expérience est de savoir si le sucre ou le sel se dissout plus rapidement lorsqu’il est mélangé à divers liquides. La taille des morceaux affecte-t-elle la rapidité avec laquelle ils se mélangent au liquide ?
Lorsque vous dissolvez du sucre ou du sel dans un liquide… disons de l’eau… ce qui se passe, c’est que les molécules de sucre se déplacent pour s’insérer entre les molécules d’eau dans un verre ou un bécher. L’illustration ci-dessous montre comment les différentes molécules sont disposées dans le récipient.
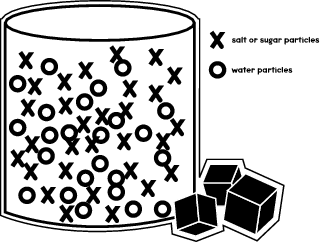
Dans votre expérience, vous verrez comment les molécules de sel et de sucre se déplacent dans différents liquides et se dissolvent à des vitesses différentes.
Le titre de cette section, ?Sel ou sucre : Lequel se dissout le plus vite dans différents liquides ? » pourrait servir de titre à votre projet, si vous le souhaitez. Vous pourriez également envisager l’un des titres suivants pour votre projet :
- Le grand concours de dissolution du sel contre le sucre
- Utiliser le sel et le sucre pour explorer la façon dont les substances se dissolvent
Le nom que vous choisissez est parfait. Prenons maintenant une minute pour réfléchir aux raisons pour lesquelles ce projet est une utilisation précieuse de votre temps.
Quel est l’intérêt ?
Lorsqu’il y a beaucoup d’espace entre les molécules d’un solvant, on dit que ce dernier est insaturé. Lorsqu’une grande quantité de soluté a été dissoute dans le solvant, mais qu’il reste encore de l’espace entre les molécules, la solution est concentrée. Quand absolument plus aucun soluté ne peut être dissous dans un solvant, la solution est saturée.
Et quand l’excès de soluté a été dissous en chauffant la solution, on dit qu’elle est sursaturée.
Le but de cette expérience, en plus d’apprendre si le sel ou le sucre se dissout plus vite dans différents liquides, est d’apprendre comment les molécules interagissent dans une solution.
Comme vous l’avez vu dans l’illustration précédente, les molécules d’eau occupent la majeure partie de la place dans le récipient. Mais il reste encore de l’espace disponible dans lequel les molécules de sucre ou de sel peuvent s’insérer. Grâce à votre expérience, vous apprendrez à quelle vitesse les molécules de sucre s’insèrent dans ces espaces, par rapport aux particules de sel.
Savoir cela vous aidera à mieux comprendre le processus qui se produit lorsqu’une substance se dissout.
Le témoin de votre expérience sera l’eau. Les autres liquides dans lesquels vous dissoudrez le sel et le sucre seront les variables.
| Contrôles : | Solvant ? eau | Solutés ?sucre, sel | Variables : | Cinq liquides clairs différents (pouvant être colorés) |
Rappelle-toi, lorsque tu réaliseras ton expérience, qu’il est très important que les liquides que tu utilises soient tous à la même température. Vous avez déjà appris que le sucre se dissout plus rapidement dans un liquide chaud que dans un liquide froid, vous savez donc que l’expérience ne serait pas précise si certains des liquides que vous utilisez sont chauds et d’autres froids. La température du liquide deviendrait une variable.
Donc, tous les liquides que vous utilisez… y compris l’eau… doivent être à température ambiante. Si vous les conservez normalement au réfrigérateur, veillez à les laisser reposer sur le comptoir toute la nuit jusqu’à ce qu’ils soient tous à la même température.
Pour vous donner un peu plus de flexibilité lorsque vous réaliserez l’expérience, vous pouvez choisir les liquides dans lesquels vous dissoudrez le sucre et le sel. Il est inutile de devoir aller acheter des liquides supplémentaires si vous avez déjà ce dont vous avez besoin.
Ne supposez pas que les liquides qui ont séjourné dans différents endroits de votre maison ont la même température. Une bouteille de soda qui a séjourné dans le garage, par exemple, peut être plus froide de plusieurs degrés que l’alcool à friction qui se trouve dans le placard de la salle de bain ou le jus de pomme qui se trouve dans le garde-manger de la cuisine. Assurez-vous que tous les liquides se trouvent au même endroit pour qu’ils atteignent la même température ambiante. If you don’t, the results of your experiment won’t be valid.
Just make sure you choose liquids that are different from each other in taste, color, odor, and purpose. You’ll also need to select those that allow you to observe the salt and sugar as it dissolves. If you use milk or orange juice, for example, you won’t be able to watch the salt and sugar dissolve. Some suggestions for liquids to consider are:
- White vinegar
- Club soda
- Ginger ale
- Glass cleaner (such as Windex)
- Lemonade
- Tea or iced tea (each at room temperature)
- Apple juice
- Rubbing alcohol
All of these are commonly found around the house, perhaps saving you a trip to the store.
What Do You Think Will Happen?
Maintenant que vous savez comment les solutions se forment et certains des facteurs qui affecteront la vitesse à laquelle le sucre et le sel que vous utiliserez se dissoudront, vous devriez pouvoir deviner lequel se dissoudra le plus rapidement.
Si vous n’avez pas fait cette expérience auparavant, vous ne saurez pas si les liquides que vous utiliserez seront un facteur de dissolution du sel et du sucre. Il est donc plus difficile de formuler une hypothèse, mais ne vous inquiétez pas. Que votre hypothèse s’avère correcte, ou non, n’affecte pas la validité ou le résultat de votre expérience.
Bien que vous ne sachiez pas avant la fin de votre expérience si les propriétés des différents liquides que vous choisissez affecteront la vitesse de dissolution du sel et du sucre, vous savez que les cristaux de sel sont généralement plus petits que les cristaux de sucre. Et vous savez que la température des liquides ne sera pas un facteur dans votre expérience.
Essayez simplement d’utiliser vos expériences passées, les informations que vous avez lues plus tôt dans cette section, et votre bon sens pour trouver une hypothèse solide.
N’oubliez pas que votre hypothèse doit être énoncée sous forme de phrase objective, et non de question. Alors allez-y et -faites votre hypothèse pour savoir si le sel ou le sucre se dissoudra plus vite, et commençons l’expérience.
Matériel dont vous aurez besoin pour ce projet
Certains liquides suggérés pour cette expérience sont le vinaigre blanc, le club soda, le soda au gingembre, le nettoyant pour vitres, l’alcool à friction, le jus de pomme, la limonade et le thé. Si vous souhaitez remplacer un ou plusieurs des liquides proposés par un autre, c’est parfait. Assurez-vous simplement que tous les liquides sont clairs et à température ambiante.
Les quantités de matériel indiquées ci-dessous sont suffisantes pour que vous puissiez réaliser l’expérience trois fois avec chaque liquide. You’ll need:
- 12 clear, plastic cups (10 ounce )
- One permanent marker
- One (1 teaspoon) (5.0 ml) measuring spoon
- One (12 teaspoon) (2.5 ml) measuring spoon
- One (1 cup) (240 ml) measuring cup
- 8 teaspoons (40 ml) salt, divided in 16 (12 teaspoon) portions
- 8 teaspoons (40 ml) sugar, divided in 16 (12 teaspoon) portions
- 48 ounces (1,440 ml) water at room temperature
- 24 ounces (720 ml) each of five different, clear liquids, all at room temperature
- One clock or watch with a second hand
- One clear plastic cup containing eight fluid ounces (240 ml) water at room temperature
Remember to make sure that all liquids are at room temperature.
Conducting Your Experiment
When you’ve gathered all your materials, you’ll be ready to begin your experiment. Il vous suffit de suivre les étapes suivantes :
Gardez une tasse d’eau plate à portée de vue afin de pouvoir la comparer aux tasses contenant du sel et du sucre. Il sera intéressant d’observer comment l’apparence des liquides change au fur et à mesure que le sel et le sucre se dissolvent.
Il va falloir un peu de temps pour que le sucre et le sel se dissolvent. Pour de meilleurs résultats, ne remuez pas les solutions, car cela présenterait une variable supplémentaire. Si vous devez remuer, alors remuez chaque solution trois fois, et arrêtez. Ne remuez qu’après avoir constaté la présence de soluté au fond de chacun des deux récipients. Si vous remuez les solutions de manière inégale, votre expérience ne sera pas valide.
- À l’aide du marqueur permanent, écrivez » sel » sur six des gobelets en plastique, et » sucre » sur les six autres.
- Mettez 1/2 cuillère à café (2,5 ml) de sel dans chacun des six gobelets étiquetés » sel « .
- Placez 1/2 cuillère à café (2,5 ml) de sucre dans chacun des six gobelets étiquetés » sucre « .
- Ajoutez 8 onces (240 ml) d’eau dans une tasse contenant du sel, et une tasse contenant du sucre. Enregistrez immédiatement l’heure à laquelle l’eau a été ajoutée sur un tableau de données similaire à celui présenté dans la section suivante, » Garder une trace de votre expérience « .
- Observez les solutés (sel et sucre) se dissoudre dans le solvant (eau). Notez sur le tableau de données le moment où il vous semble que chaque soluté s’est complètement dissous. Ces temps ne seront probablement pas les mêmes.
- Calculez le temps écoulé pendant lequel la dissolution s’est produite. Prenez le moment où l’eau a été ajoutée aux tasses et où la dissolution a commencé, et soustrayez-le du moment où la dissolution s’est terminée. Cela vous donne le total des minutes qu’il a fallu pour que le sel et le sucre se dissolvent complètement dans le liquide.
- Répétez les étapes 4 à 6, en utilisant chaque liquide différent à la place de l’eau.
- Lavez, rincez et séchez soigneusement chacune des 12 tasses.
- Répétez les étapes 2 à 8 deux autres fois, pour un total de trois essais pour chacun des six liquides.
- Calculez un temps de dissolution moyen pour le sel et le sucre dans chacun des six liquides.
Rappelle-toi que pour trouver le temps moyen qu’il a fallu au sel et au sucre pour se dissoudre dans chaque liquide, tu additionnes les trois temps enregistrés pour chacun d’eux, puis tu les divises par trois. Le nombre que vous obtenez en divisant les temps est le temps moyen.
Garder une trace de votre expérience
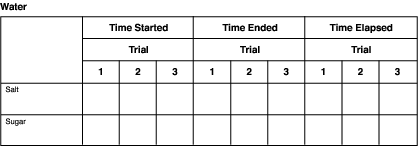
Des tableaux comme celui qui suit peuvent être utilisés pour enregistrer les informations relatives à chaque solvant. Il suffit de changer le nom des solvants dans l’intitulé.
Veuillez noter les temps au fur et à mesure. Ne comptez pas sur votre mémoire pour les écrire plus tard. Tu auras beaucoup de chiffres lorsque tu auras terminé ton expérience.
Mettre tout ça bout à bout
Qu’as-tu remarqué sur les vitesses de dissolution du sel et du sucre ? As-tu prouvé que ton hypothèse était correcte ? Ou incorrecte ? Pouviez-vous détecter un type de schéma lorsque vous avez ajouté le sel et le sucre aux différents liquides ? Était-il évident que le sel se dissolvait mieux et plus vite dans certains liquides que le sucre ? Pouvez-vous penser à des raisons pour lesquelles cela aurait pu se produire ?
Pensez-vous que les natures chimiques du soluté et du solvant ont affecté les vitesses de dissolution ? Utilisez les informations que vous avez recueillies lors de vos recherches sur votre sujet pour vous aider à répondre à ces questions.
Plus vous en saurez sur votre projet, plus vous serez en mesure d’analyser correctement vos données et de parvenir à une conclusion solide.
Poursuite des recherches
Comme mentionné précédemment, les facteurs affectant la solubilité des solutés solides sont :
- Augmentation ou diminution de la température du solvant
- Augmentation de la surface du soluté
- Agitation
Si vous vouliez pousser ce projet un ou deux pas plus loin, vous pourriez concevoir une expérience qui testerait une ?ou peut-être toutes… ces variables.
Vous pourriez facilement comparer la vitesse à laquelle les morceaux de sucre se dissolvent dans un liquide avec la vitesse de dissolution du sucre cristallisé.
Ou vous pourriez utiliser le même soluté… disons le sucre… et tester si le fait de remuer la solution l’amène à se dissoudre plus rapidement. Chauffer et refroidir le solvant au fur et à mesure que vous ajoutez le même soluté serait également une possibilité d’expérimentation supplémentaire.
Si vous êtes curieux et prêt à expérimenter, vous pouvez probablement penser à de nombreuses variations pour ce projet. Et, parce que l’expérience ne fait appel qu’à des matériaux communs et peu coûteux, vous devriez pouvoir expérimenter à votre guise.
Excerté de The Complete Idiot’s Guide to Science Fair Projects 2003 par Nancy K. O’Leary et Susan Shelly. Tous droits réservés, y compris le droit de reproduction en tout ou en partie sous quelque forme que ce soit. Utilisé par arrangement avec Alpha Books, un membre de Penguin Group (USA) Inc.
Pour commander ce livre directement auprès de l’éditeur, visitez le site Web de Penguin USA ou appelez le 1-800-253-6476. Vous pouvez également acheter ce livre sur Amazon.com et Barnes & Noble.
.