Geowetenschap toepassen op de belangrijkste uitdagingen van Australië
Inleiding

Aluminiumfolie. Bron: Wikimedia Commons
Aluminium is overal om je heen – van alledaagse voorwerpen zoals een blikje frisdrank tot de vliegtuigen die overvliegen. Aluminium is een van de nuttigste materialen die de mens kent. Het kan worden gelegeerd (gemengd) met bijna elk ander metaal om materialen met nuttige eigenschappen te creëren. Metalen die met aluminium zijn gelegeerd zijn allemaal zeer sterk en toch licht, en bestand tegen roesten.
Na zuurstof en silicium is aluminium het op twee na meest voorkomende element in de aardkorst (8,2%) en verreweg het meest overvloedige metaal. In tegenstelling tot metalen als koper, goud, lood, ijzer en zink, die al duizenden jaren door de mens worden gebruikt, is aluminium pas iets meer dan 100 jaar algemeen in gebruik. Dit komt omdat aluminium nooit in zijn zuivere vorm in de natuur wordt aangetroffen. Hoewel de mens dus op de hoogte was van aluminiumverbindingen, ontdekte hij pas eind 1800 hoe hij aluminiummetaal kon winnen.
Aluminium kan (op oneconomische wijze) worden gewonnen uit sommige kleisoorten, maar het meest voorkomende aluminiumerts is een materiaal dat bauxiet wordt genoemd. Eerst moet het aluminiumerts worden gedolven, daarna wordt het bauxiet geraffineerd tot aluminiumoxide (aluminiumoxide). Er worden grote hoeveelheden elektriciteit gebruikt om het aluminiumoxide te smelten tot aluminiummetaal.
Eigenschappen
Aluminium is een zilverkleurig metaal dat nooit als zodanig in de natuur voorkomt. Het is zeer licht (ongeveer een derde van het gewicht van koper) en toch sterk; sommige legeringen zijn zelfs sterker dan staal. Aluminium is zowel kneedbaar (kan in vorm worden geperst) als kneedbaar (kan worden geslagen en tot een draad worden getrokken). Aluminium is een zeer goede warmte- en elektrische geleider. Het is ook zeer roestbestendig en niet giftig. Aluminium kan met bijna alle andere metalen worden gelegeerd. Aluminium is ontvlambaar, niet-magnetisch en vonkvrij. These properties have made it an important metal in the modern world. As aluminium is such a reactive metal, you might think it would rust badly and therefore be useless. However, pure aluminium reacts very quickly with air or water to form a thin, almost invisible layer of aluminium oxide on its surface, which then acts as a protective coating preventing any further ‘rusting’.
|
The Properties of Aluminium |
|
|---|---|
|
Chemical symbol |
Al – from the Roman word Alumen – the word for the aluminium-potassium compound alum |
|
Ore |
Bauxite |
|
Relative density |
2.7 g/cm3 |
|
Hardness |
2.75 on Mohs scale |
|
Malleability |
High |
|
Ductility |
High |
|
Melting point |
660°C |
|
Boiling Point |
2470°C |
Uses

Aluminium-bodied Austin “A40 Sports” (c. 1951). Bron: Wikimedia Commons
Aluminium is smelted from alumina which is refined from bauxite ore. All three products have a number of uses.
More than 90% of the world’s bauxite production is used to make alumina with most of the remaining 10% used by the abrasive, refractory and chemical industries. Bauxite is also used in the production of high-alumina cement, as an absorbent or catalyst by the oil industry, in welding rod coatings and as a flux in making steel and ferroalloys.
Alumina’s primary use is as feedstock for aluminium smelters, however it is also used for other industrial purposes. It is used in glass, porcelain and in metallic paints, such as those sprayed on cars. Het wordt ook gebruikt bij de productie van isolatoren voor bougies, als brandstof voor raketboosters, als vulstof voor kunststoffen, als schuurmiddel (het is goedkoper dan industrieel diamant) en in metaalraffinaderijen waar het wordt gebruikt om giftige waterstofsulfide-afvalgassen om te zetten in elementaire zwavel.
Aluminiumoxide dat in een natuurlijke, kristallijne toestand voorkomt, wordt het mineraal korund genoemd. Soms zijn korundkristallen verontreinigd met sporen van chroom, ijzer, titanium, koper of magnesium. Deze kristallen noemen we robijnen en saffieren.
Na ijzer en staal is aluminium het meest gebruikte metaal op aarde. Het wordt vaak gelegeerd met koper, zink, magnesium, mangaan of silicium en de toevoeging van kleine hoeveelheden zirkonium, hafnium of scandium aan deze legeringen verbetert hun sterkte aanmerkelijk. Aluminium zelf heeft een breed scala van toepassingen, van gespecialiseerde vliegtuigbouw tot alledaagse voorwerpen zoals messen en vorken. Enkele van de toepassingen staan in de tabel hieronder.
|
Use |
Description |
|---|---|
|
Building and construction |
Cladding, doors, window frames, awnings and bridge rails as aluminium is strong, light, easily shaped and resistant to rust. |
|
Transport |
Parts for cars, trucks, buses, aircraft, ships, rail and trams as aluminium is strong, light, easily shaped and resistant to rust. |
|
Appliances |
Fridges, washing machines, lawn mowers etc. due to its strength, malleability and rust resistance. |
|
Heating and ventilation |
Heating and cooling systems as aluminium is a good conductor of heat. |
|
Packaging |
Kitchen foil, packaging foil, cans and containers (worldwide, four out of every five drink cans are made of aluminium) as aluminium can be rolled into very thin sheets and is non-toxic. |
|
Electrical and communications |
Power transmission including towers, electrical conduits, superconductors, machinery and equipment, telephone cables and capacitors because of aluminium’s ability to conduct electricity. |
|
Other |
Utensils (cutlery, pans), industrial machinery, chemical industry, production of steel, antiperspirants, furniture, reflectors in telescopes, making high octane petrol, road signs, antacids and jewellery due to its many useful properties. |
History
Around 5300 BC: The Persians made extra strong pots from clay containing aluminium oxide.
Around 2000 BC: The ancient Egyptians and Babylonians used potassium aluminium sulphate KAl(SO4)2 as a medicine to reduce bleeding. It was sourced from naturally occurring deposits in Greece and Turkey. The ancient Romans called this medical compound “alum”, which is where we get the modern day word and symbol from. Het wordt vandaag de dag nog steeds gebruikt om bloedingen te stelpen.
Middeleeuwen: Het meeste aluin kwam uit het pauselijke gebied van Tolfa, maar de prijs daalde drastisch toen in het begin van de jaren 1600 in Yorkshire een grote afzetting van aluinhoudende leisteen werd ontdekt. In de volgende eeuwen werd aluin op twee belangrijke gebieden gebruikt: als conserveringsmiddel voor papier en als fixeermiddel voor het verven van stoffen.
1808: De Engelsman Sir Humphry Davy probeerde aluminium te winnen door middel van elektrolyse. Hij faalde, maar stelde wel het bestaan ervan vast en gaf het zijn naam.
1821: De Franse geoloog Pierre Berthier ontdekte een aluminiumrijk materiaal in de buurt van het dorp Les Baux in de Provence, Frankrijk. Het werd bauxiet genoemd naar het dorp.
1825: Hans Christian Oersted in Denemarken produceerde onzuiver aluminium door aluminiumchloride te verhitten met kaliumamalgaam.
1827: De Duitse scheikundige Friedrich Wöhler extraheerde aluminium als poeder door kalium te laten reageren met watervrij aluminiumchloride en verbeterde daarmee het proces van Oersted.
1855: De Franse chemicus Henri Saint-Claire Deville slaagde erin een massieve staaf aluminium te verkrijgen door natrium te gebruiken in plaats van het duurdere kalium. De aluminiumstaaf werd zo kostbaar geacht dat hij nog datzelfde jaar werd tentoongesteld naast de Franse kroonjuwelen.
1886: Twee wetenschappers op verschillende continenten (Charles Hall in Amerika en Paul Heroult in Frankrijk) ontdekten onafhankelijk van elkaar een economische methode om aluminium te produceren via elektrolyse in gesmolten kryoliet (natriumaluminiumfluoride). Beiden zijn overigens geboren in 1864 en beiden overleden in 1914.
1887: De Oostenrijkse chemicus Karl Josef Bayer, werkzaam in Rusland, ontwikkelde een methode om aluminiumoxide uit bauxiet te winnen.
1888: Hall richt de Pittsburgh Reduction Company op (sinds 1907 bekend als Alcoa).
1890: De ontdekkingen van Hall-Heroult en Bayer hadden de prijs van aluminium met 80% doen kelderen. In 1888 kostte aluminium 4,86 dollar per pond. In 1893 kostte het 0,78 dollar per pond en tegen het eind van de jaren dertig kostte het nog maar 0,20 dollar per pond en had het meer dan 2000 toepassingen.
1900: Slechts 8000 ton aluminium werd geproduceerd, maar 100 jaar later werd 24,5 miljoen ton geproduceerd en in 2016 naar schatting 57,6 miljoen ton.

Het F-16 gevechtsvliegtuig is ontworpen om relatief goedkoop te bouwen en eenvoudiger te onderhouden te zijn dan gevechtsvliegtuigen van de eerdere generatie. Het casco is gebouwd met ongeveer 80% aluminiumlegeringen van luchtvaartkwaliteit, 8% staal, 3% composieten en 1,5% titanium. Bron: Wikimedia Commons, Master Sgt. Andy Dunaway
1911: De Duitse chemicus Alfred Wilm ontwikkelde belangrijke aluminiumlegeringen die stevig genoeg waren voor de fabricage van voorwerpen zoals vliegtuigen. Er was grote vraag naar aluminium tijdens de Tweede Wereldoorlog en de Koreaanse Oorlog, omdat vliegtuigen voorheen van hout en stof waren gemaakt.
1922: Aluminiumfolie werd vervaardigd.
1955: De eerste aluminiumsmelterij in Australië werd geopend in Bell Bay, Tasmanië.
1958: Aluminium frisdrankblikjes worden voor het eerst geproduceerd.
1961: Alcoa vormt Alcoa of Australia.
1963: Alcoa of Australia opent de eerste aluminiumoxideraffinaderij in Australië in Kwinana in West-Australië, gevolgd door Pinjarra in 1972 en Wagerup in 1984.
Dag van vandaag: In 2016 werd naar schatting 57,6 miljoen ton aluminium geproduceerd. Dit is meer dan alle andere non-ferrometalen samen. Australië wint bauxiet in Queensland, West-Australië, het Northern Territory en Tasmanië en is ’s werelds grootste bauxietproducent. Australië is ook een wereldleider in de productie van aluminiumoxide en aluminium. De drie West-Australische raffinaderijen leveren 45% van het Australische aluminiumoxide en 11% van het mondiale totaal, waarmee ze de grootste afzonderlijke bron van aluminiumoxide ter wereld zijn.
Vorming

Weipa bauxiet, R30128. Bron: Geoscience Australia.
Bauxiet is het meest voorkomende aluminiumerts. Bauxiet komt voor als een verweerde bedekking of deken, bekend als lateriet of duricrust, over een verscheidenheid van alumina-houdende gesteenten. Het wordt gevormd wanneer grote hoeveelheden regenval de meer mobiele elementen in het gastgesteente uitlogen, waardoor het betrekkelijk onbeweeglijke aluminium met wat silicium, ijzer en titanium overblijft. Door de manier waarop het wordt gevormd, kunnen bauxietafzettingen zeer uitgestrekt zijn en worden ze op bijna elk continent gevonden.
De belangrijkste aluminiummineralen in bauxiet zijn gibbsiet , boehmiet en diaspore, dat een polymorf (alternatieve vorm) van boehmiet is, maar dichter en harder is. Zuiver aluminiumoxide (Al2O3) bevat 52,9% aluminium en 47,1% zuurstof. Bauxiet kan zeer hard zijn of zo zacht als modder en kan voorkomen als verdichte aarde (zowel brokkelig als opnieuw verhard), kleine bolletjes (pisolieten), of hol, twijgvormig materiaal (tubules). De kleuren kunnen buff, roze, geel, rood of wit zijn, of een combinatie van deze. Aluminium is ook aanwezig in veel kostbare edelstenen zoals turkoois, robijn, saffier, smaragd, topaas, jade en aquamarijn.
Bronnen
Bauxieterts bevat voldoende hoge gehaltes aluminiumoxiden en voldoende lage gehaltes ijzeroxide (Fe2O3) en siliciumdioxide (SiO2) om economisch winbaar te zijn. De hoeveelheid reactieve silica is bijzonder belangrijk aangezien deze vorm van silica de natronloog verbruikt die nodig is om aluminiumoxide te maken, dus een lage reactieve silica is wenselijk. Andere potentiële bronnen van aluminium omvatten een verscheidenheid aan gesteenten en mineralen zoals aluminiumhoudende schalie en leisteen, aluminiumfosfaatgesteente en klei met een hoog aluminiumgehalte.
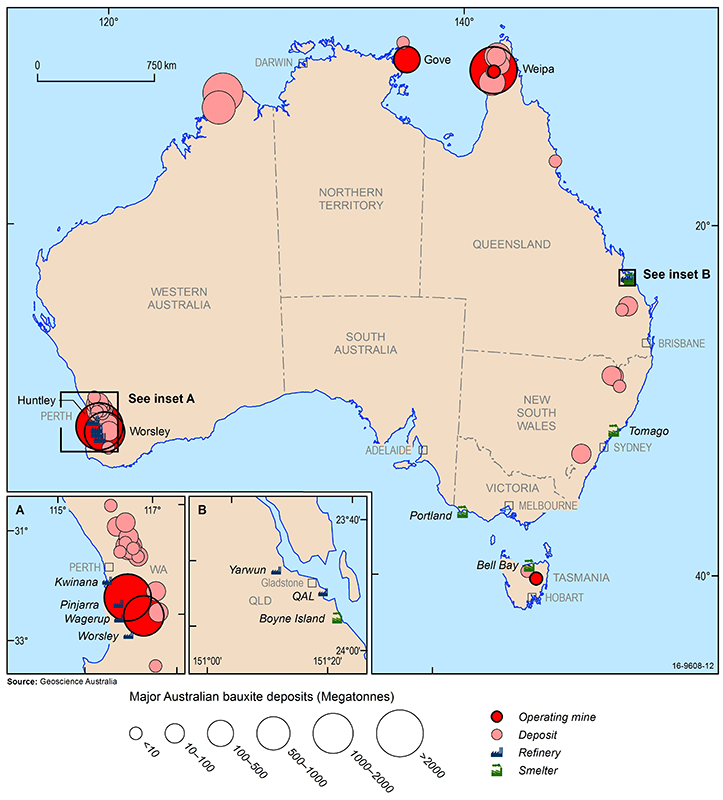
De belangrijkste bauxietafzettingen, mijnen, aluminiumoxideraffinaderijen en aluminiumsmelterijen van Australië (2016). Source: Geoscience Australia.
De grootste economische bauxietvoorraden ter wereld komen voor in Guinee, Australië, Brazilië, Vietnam en Jamaica. In Australië wordt bauxiet gewonnen in gevestigde dagbouwoperaties in Weipa in Queensland, Gove in het Northern Territory en de Darling Range in West-Australië. Bovendien zijn onlangs nieuwe mijnen in bedrijf genomen in de regio Cape York in Queensland en in centraal Tasmanië. Andere bauxietlagen komen voor in het noorden van West-Australië, New South Wales en het oosten van Queensland, maar zijn momenteel niet rendabel te ontginnen.
De aluminiumoxideraffinaderijen van Australië zijn gevestigd in West-Australië (Kwinana, Wagerup, Pinjarra en Worsely) en Queensland (QAL en Yarwun) en de aluminiumsmelterijen bevinden zich in Tasmanië (Bell Bay), Queensland (Boyne Island), Victoria (Portland) en New South Wales (Tomago). China is ’s werelds grootste verbruiker van aluminium en importeert, ondanks de sterke binnenlandse produktie, grote hoeveelheden aluminiumoxide en ruw bauxiet, goed voor meer dan 40% van het mondiale verbruik. Andere grote aluminiummarkten zijn de Verenigde Staten van Amerika, Japan en Europa, maar deze regio’s hebben weinig economische bauxietvoorkomens en zijn voor hun aluminiumoxideraffinaderijen en aluminiumsmelterijen ook afhankelijk van de invoer van bauxiet en aluminiumoxide.
Verder informatie over hulpbronnen en productie.
Mijnbouw
De winning van aluminiummetaal vindt plaats in drie hoofdfasen: de winning van bauxieterts, de raffinage van het erts om aluminiumoxide terug te winnen en het smelten van aluminiumoxide om aluminium te produceren. Bauxiet wordt aan de oppervlakte gewonnen (dagbouw), waarbij de bovengrond en de deklaag door bulldozers en schrapers worden verwijderd. De bovengrond wordt vervolgens opgeslagen en later gebruikt voor herbegroeiing en herstel van het gebied nadat de mijnbouw is voltooid. Het onderliggende bauxiet wordt gedolven met voorladers, graafmachines of hydraulische graafmachines. Sommige bauxietertsen worden alleen gebroken, gedroogd en verscheept. Andere bauxietertsen worden na het breken gewassen om een deel van de klei, reactieve silica en zandresten te verwijderen, en vervolgens gedroogd in draaiovens. Het erts wordt in vrachtwagens, treinwagons of op transportbanden geladen en naar schepen of raffinaderijen vervoerd.
Een aantal factoren in de aluminiumproduktiecyclus houdt verband met het milieu en er worden aanzienlijke middelen uitgetrokken om het effect van mijnbouw, raffinage en smelten op het omringende milieu tot een minimum te beperken. De mijnen worden gesaneerd, waarbij alles in het werk wordt gesteld om het gebied ten minste in zijn oorspronkelijke staat terug te brengen. Er wordt zorg gedragen voor de behandeling en verwijdering van rode modder uit de raffinaderijen. Deze modder wordt gewoonlijk in dammen gepompt die met ondoordringbaar materiaal worden afgedicht om verontreiniging van het omringende landschap te voorkomen.
Verwerking
In bijna alle commerciële bedrijven wordt aluminiumoxide uit het bauxiet gewonnen door middel van het Bayer-raffinageproces. Het proces, dat in 1888 werd ontdekt door Karl Josef Bayer, bestaat uit vier fasen.
Digestie: het fijngemalen bauxiet wordt toegevoerd aan een met stoom verhitte eenheid die een digester wordt genoemd. Hier wordt het onder druk gemengd met een hete oplossing van bijtende soda. Het aluminiumoxide van het bauxiet (en het reactieve kiezelzuur) reageert met het natronloog en vormt een oplossing van natriumaluminaat of “green liquor” en een neerslag van natriumaluminiumsilicaat.
Klarificatie: de “green liquor” of aluminiumhoudende oplossing wordt van het afval gescheiden¿ de onopgeloste ijzeroxiden en kiezelzuur die deel uitmaakten van het oorspronkelijke bauxiet en nu het zand en rode modderafval vormen. Dit gebeurt in drie stappen: eerst wordt het grove zand verwijderd en gewassen om het natriumhydroxide terug te winnen; vervolgens wordt het rode slib afgescheiden; en tenslotte wordt het overblijvende groene slib door filters gepompt om alle resterende onzuiverheden te verwijderen. Het zand en slib worden samen naar residubekkens gepompt en het groene slib wordt naar warmtewisselaars gepompt waar het wordt afgekoeld van 1000°C tot ongeveer 650-790°C.
Precipitatie: het aluminiumoxide wordt uit het slib geprecipiteerd in de vorm van kristallen van aluminiumhydraat. Daartoe wordt de groene liquor-oplossing in hoge precipitatorvaten gemengd met kleine hoeveelheden fijn kristallijn aluminiumoxide, wat de neerslag van vast aluminiumoxidehydraat stimuleert naarmate de oplossing afkoelt. Als het vaste aluminiumoxidehydraat klaar is, gaat het naar de volgende fase en gaat de overblijvende vloeistof, die natronloog en wat aluminiumoxide bevat, terug naar de kookketels.
Calcinatie: het aluminiumoxidehydraat wordt gewassen om eventueel achtergebleven vloeistof te verwijderen en vervolgens gedroogd. Ten slotte wordt het verhit tot ongeveer 1000°C om het kristallisatiewater te verdrijven, zodat er aluminiumoxide overblijft – een droog, zuiver wit zandig materiaal. Een deel van het aluminiumoxide kan in de hydraatvorm worden gelaten of verder worden verwerkt voor de chemische industrie.
Aluminiumoxide wordt omgezet in aluminium door middel van een smeltproces. Alle commerciële productie van aluminium is gebaseerd op het Hall-Héroult smeltproces, waarbij het aluminium en de zuurstof in het aluminiumoxide worden gescheiden door elektrolyse. Bij elektrolyse wordt een elektrische stroom door een gesmolten oplossing van aluminiumoxide en natuurlijk of synthetisch kryoliet (natriumaluminiumfluoride) geleid. De gesmolten oplossing bevindt zich in reductiecellen of potten die aan de onderkant bekleed zijn met koolstof (de kathode) en die verbonden zijn in een elektrische reeks, een zogenaamde potlijn. In de top van elke pot zijn koolstofanodes aangebracht, waarvan de bodems in de gesmolten oplossing zijn ondergedompeld.
Door de passage van een elektrische stroom verbindt de zuurstof uit de aluminiumoxide zich met de koolstof van de anode, waarbij kooldioxidegas wordt gevormd. Het resterende gesmolten metallisch aluminium verzamelt zich bij de kathode op de bodem van de pot. Periodiek wordt het overgeheveld en overgebracht naar grote opslagovens. Onzuiverheden worden verwijderd, legeringselementen toegevoegd en het gesmolten aluminium wordt tot ingots gegoten.
Het smeltproces is een continu proces. Naarmate het aluminiumoxidegehalte van het kryolietbad daalt, wordt meer aluminium toegevoegd. De door de elektrische stroom opgewekte warmte houdt het kryolietbad in zijn gesmolten toestand, zodat het aluminiumoxide oplost. Tijdens het smeltproces wordt een grote hoeveelheid energie verbruikt; tussen 14.000 en 16.000 kilowattuur elektrische energie is nodig om één ton aluminium te produceren uit ongeveer twee ton aluminiumoxide. Aluminium wordt ook wel “vaste elektriciteit” genoemd vanwege de grote hoeveelheid stroom die bij de produktie ervan wordt gebruikt. De beschikbaarheid van goedkope elektriciteit is daarom essentieel voor een economische produktie.
Aluminiumblokken worden in verschillende vormen en afmetingen geproduceerd, afhankelijk van het eindgebruik. Zij kunnen worden gewalst tot platen, vellen, folie, staven of staven. Zij kunnen worden getrokken tot draad die wordt verwerkt tot kabels voor elektrische transmissielijnen. Persen extruderen de ingots in honderden verschillende nuttige en decoratieve vormen of fabrieken verwerken ze tot grote structurele vormen.