Applicare la geoscienza alle sfide più importanti dell’Australia
Introduzione

Foglio di alluminio. Fonte: Wikimedia Commons
L’alluminio è tutto intorno a noi, dagli oggetti di uso quotidiano come la lattina di una bibita agli aerei che volano in cielo. L’alluminio è uno dei materiali più utili conosciuti dall’uomo. Può essere legato (mescolato) con quasi ogni altro metallo per creare materiali con proprietà utili. I metalli legati con l’alluminio sono tutti molto forti ma leggeri e resistenti alla ruggine.
Dopo l’ossigeno e il silicio, l’alluminio è il terzo elemento più abbondante nella crosta terrestre (8,2%) e di gran lunga il metallo più abbondante. A differenza di metalli come il rame, l’oro, il piombo, il ferro e lo zinco che sono stati usati dall’uomo per migliaia di anni, l’alluminio è entrato nell’uso comune solo da poco più di 100 anni. Questo perché l’alluminio non si trova mai allo stato puro in natura. Così, mentre l’uomo conosceva i composti dell’alluminio, ha scoperto come estrarre l’alluminio metallico solo alla fine del 1800.
L’alluminio può essere estratto (in modo antieconomico) da alcune argille, ma il minerale di alluminio più comune è un materiale chiamato bauxite. Prima bisogna estrarre il minerale di alluminio, poi la bauxite viene raffinata in allumina (ossido di alluminio). Grandi quantità di elettricità sono usate per fondere l’allumina in alluminio metallico.
Proprietà
L’alluminio è un metallo color argento che non si trova mai da solo in natura. È molto leggero (circa un terzo del peso del rame) ma forte; alcune leghe sono anche più forti dell’acciaio. L’alluminio è sia malleabile (può essere pressato in forma) che duttile (può essere battuto e tirato in un filo). L’alluminio è un ottimo conduttore di calore e di elettricità. È anche molto resistente alla ruggine e non è tossico. L’alluminio può essere legato con quasi tutti gli altri metalli. L’alluminio è infiammabile, non magnetico e non scintillante. These properties have made it an important metal in the modern world. As aluminium is such a reactive metal, you might think it would rust badly and therefore be useless. However, pure aluminium reacts very quickly with air or water to form a thin, almost invisible layer of aluminium oxide on its surface, which then acts as a protective coating preventing any further ‘rusting’.
|
The Properties of Aluminium |
|
|---|---|
|
Chemical symbol |
Al – from the Roman word Alumen – the word for the aluminium-potassium compound alum |
|
Ore |
Bauxite |
|
Relative density |
2.7 g/cm3 |
|
Hardness |
2.75 on Mohs scale |
|
Malleability |
High |
|
Ductility |
High |
|
Melting point |
660°C |
|
Boiling Point |
2470°C |
Uses

Aluminium-bodied Austin “A40 Sports” (c. 1951). Fonte: Wikimedia Commons
Aluminium is smelted from alumina which is refined from bauxite ore. All three products have a number of uses.
More than 90% of the world’s bauxite production is used to make alumina with most of the remaining 10% used by the abrasive, refractory and chemical industries. Bauxite is also used in the production of high-alumina cement, as an absorbent or catalyst by the oil industry, in welding rod coatings and as a flux in making steel and ferroalloys.
Alumina’s primary use is as feedstock for aluminium smelters, however it is also used for other industrial purposes. It is used in glass, porcelain and in metallic paints, such as those sprayed on cars. Viene anche usato nella produzione di isolanti per candele, come componente del combustibile per razzi a propellente solido, come riempitivo per la plastica, come abrasivo (è più economico del diamante industriale) e nelle raffinerie di metalli dove viene usato per convertire i gas tossici di scarto dell’idrogeno solforato in zolfo elementare.
L’allumina che si presenta in uno stato naturale e cristallino viene chiamata corindone. A volte, i cristalli di corindone sono contaminati da tracce di cromo, ferro, titanio, rame o magnesio. Questi cristalli si chiamano rubini e zaffiri.
Dopo il ferro e l’acciaio, l’alluminio è il metallo più usato sulla Terra. È spesso legato con rame, zinco, magnesio, manganese o silicio e l’aggiunta di piccole quantità di zirconio, afnio o scandio a queste leghe ne migliora notevolmente la resistenza. L’alluminio stesso ha una vasta gamma di usi, dalla costruzione di aerei specializzati agli oggetti di uso quotidiano come coltelli e forchette. Alcuni degli usi sono elencati nella tabella qui sotto.
|
Use |
Description |
|---|---|
|
Building and construction |
Cladding, doors, window frames, awnings and bridge rails as aluminium is strong, light, easily shaped and resistant to rust. |
|
Transport |
Parts for cars, trucks, buses, aircraft, ships, rail and trams as aluminium is strong, light, easily shaped and resistant to rust. |
|
Appliances |
Fridges, washing machines, lawn mowers etc. due to its strength, malleability and rust resistance. |
|
Heating and ventilation |
Heating and cooling systems as aluminium is a good conductor of heat. |
|
Packaging |
Kitchen foil, packaging foil, cans and containers (worldwide, four out of every five drink cans are made of aluminium) as aluminium can be rolled into very thin sheets and is non-toxic. |
|
Electrical and communications |
Power transmission including towers, electrical conduits, superconductors, machinery and equipment, telephone cables and capacitors because of aluminium’s ability to conduct electricity. |
|
Other |
Utensils (cutlery, pans), industrial machinery, chemical industry, production of steel, antiperspirants, furniture, reflectors in telescopes, making high octane petrol, road signs, antacids and jewellery due to its many useful properties. |
History
Around 5300 BC: The Persians made extra strong pots from clay containing aluminium oxide.
Around 2000 BC: The ancient Egyptians and Babylonians used potassium aluminium sulphate KAl(SO4)2 as a medicine to reduce bleeding. It was sourced from naturally occurring deposits in Greece and Turkey. The ancient Romans called this medical compound “alum”, which is where we get the modern day word and symbol from. Viene usato ancora oggi per fermare il sanguinamento.
Medioevo: La maggior parte dell’allume proveniva dal territorio papale di Tolfa, ma il prezzo scese drasticamente quando un grande deposito di scisto di allume fu scoperto nello Yorkshire all’inizio del 1600. Nei secoli successivi, l’allume fu usato in due aree principali: come conservante per la carta e come agente fissante per la tintura dei tessuti.
1808: L’inglese Sir Humphry Davy cerca di estrarre l’alluminio attraverso l’elettrolisi. Fallì, ma ne stabilì l’esistenza e gli diede il suo nome.
1821: Il geologo francese Pierre Berthier scoprì un materiale ricco di alluminio vicino al villaggio di Les Baux in Provenza, Francia. Fu chiamata bauxite dal nome del villaggio.
1825: Hans Christian Oersted in Danimarca produsse alluminio impuro riscaldando cloruro di alluminio con amalgama di potassio.
1827: Il chimico tedesco Friedrich Wöhler estrasse l’alluminio in polvere facendo reagire il potassio con cloruro di alluminio anidro migliorando il processo di Oersted.
1855: Il chimico francese Henri Saint-Claire Deville riuscì ad ottenere una barra solida di alluminio usando il sodio invece del più costoso potassio. La barra di alluminio fu considerata così preziosa che fu esposta lo stesso anno accanto ai gioielli della corona francese.
1886: Due scienziati in continenti diversi (Charles Hall in America e Paul Heroult in Francia) scoprirono indipendentemente un metodo economico per produrre alluminio tramite elettrolisi nella criolite fusa (fluoruro di sodio e alluminio). Per inciso, entrambi erano nati nel 1864 ed entrambi morirono nel 1914.
1887: Il chimico austriaco Karl Josef Bayer, lavorando in Russia, sviluppò un metodo per estrarre l’allumina dalla bauxite.
1888: Hall fonda la Pittsburgh Reduction Company (conosciuta come Alcoa dal 1907).
1890: Le scoperte di Hall-Heroult e Bayer avevano fatto crollare il prezzo dell’alluminio dell’80%. Nel 1888 l’alluminio costava 4,86 dollari per libbra. Nel 1893, costava 0,78 dollari per libbra e alla fine degli anni ’30 costava solo 0,20 dollari per libbra e aveva più di 2000 usi.
1900: Furono prodotte solo 8000 tonnellate di alluminio, ma 100 anni dopo ne furono prodotte 24,5 milioni di tonnellate e nel 2016 si stima che ne siano state prodotte 57,6 milioni di tonnellate.

Il caccia F-16 fu progettato per essere relativamente economico da costruire e più semplice da mantenere rispetto ai caccia della generazione precedente. La cellula è costruita con circa l’80% di leghe di alluminio per l’aviazione, 8% di acciaio, 3% di compositi e 1,5% di titanio. Fonte: Wikimedia Commons, Master Sgt. Andy Dunaway
1911: Il chimico tedesco Alfred Wilm sviluppa importanti leghe di alluminio che sono abbastanza solide per la fabbricazione di oggetti come gli aerei. C’era una grande richiesta di alluminio durante la seconda guerra mondiale e la guerra di Corea, dato che gli aerei erano precedentemente fatti di legno e tessuto.
1922: Viene prodotto il foglio di alluminio.
1955: La prima fonderia di alluminio in Australia fu aperta a Bell Bay, Tasmania.
1958: Vengono prodotte per la prima volta lattine di bibite in alluminio.
1961: Alcoa fonda Alcoa of Australia.
1963: Alcoa of Australia apre la prima raffineria di allumina in Australia a Kwinana nell’Australia occidentale, seguita da Pinjarra nel 1972 e da Wagerup nel 1984.
Oggi: Nel 2016 si stima che siano state prodotte 57,6 milioni di tonnellate di alluminio. Questo è più di tutti gli altri metalli non ferrosi messi insieme. L’Australia estrae bauxite nel Queensland, nell’Australia Occidentale, nel Territorio del Nord e in Tasmania ed è il più grande produttore mondiale di bauxite. L’Australia è anche leader mondiale nella produzione di allumina e alluminio. Le tre raffinerie dell’Australia occidentale forniscono il 45% dell’allumina australiana e l’11% del totale globale, rendendole la più grande fonte singola di allumina nel mondo.
Formazione

Weipa bauxite, R30128. Fonte: Geoscience Australia.
La bauxite è il minerale di alluminio più comune. La bauxite si presenta come una copertura o manto eroso dagli agenti atmosferici, conosciuta come laterite o duricrust, sopra una varietà di rocce contenenti allumina. Si forma quando grandi quantità di pioggia lisciviano via gli elementi più mobili nella roccia ospitante lasciando l’alluminio relativamente immobile con un po’ di silicio, ferro e titanio. A causa del modo in cui si forma, i depositi di bauxite possono essere molto estesi e si trovano in quasi tutti i continenti.
I principali minerali di alluminio nella bauxite sono gibbsite, boehmite e diaspore, che è un polimorfo (forma alternativa) della boehmite ma è più denso e più duro. L’allumina pura (Al2O3) contiene 52,9% di alluminio e 47,1% di ossigeno. La bauxite può essere molto dura o morbida come il fango e può presentarsi come terra compattata (sia friabile che cementata), piccole sfere (pisoliti), o materiale cavo, simile a un ramoscello (tubuli). I suoi colori possono essere il bufalo, il rosa, il giallo, il rosso o il bianco, o qualsiasi combinazione di questi. L’alluminio è presente anche in molte pietre preziose come turchese, rubini, zaffiri, smeraldi, topazio, giada e acquamarine.
Risorse
Il minerale di bauxite contiene livelli sufficientemente alti di ossidi di alluminio e livelli sufficientemente bassi di ossido di ferro (Fe2O3) e silice (SiO2) per essere economicamente estraibile. La quantità di silice reattiva è particolarmente importante perché questa forma di silice consuma la soda caustica necessaria per fare l’allumina, quindi è desiderabile una bassa quantità di silice reattiva. Altre potenziali fonti di alluminio includono una varietà di rocce e minerali come lo scisto e l’ardesia alluminosi, la roccia fosfatica di alluminio e le argille ad alta allumina.
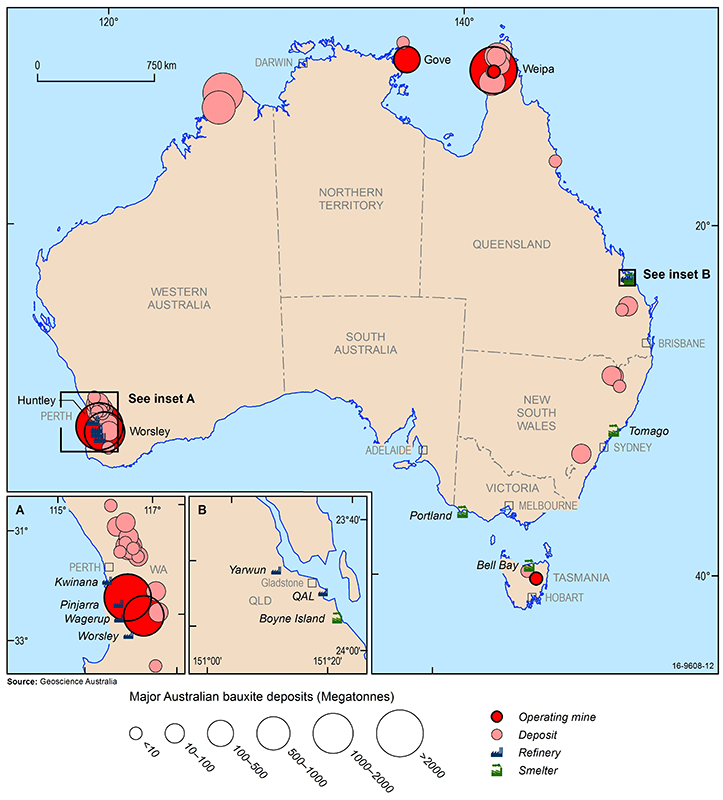
I principali depositi di bauxite, miniere, raffinerie di allumina e fonderie di alluminio dell’Australia (2016). Source: Geoscience Australia.
Le maggiori risorse economiche di bauxite al mondo si trovano in Guinea, Australia, Brasile, Vietnam e Giamaica. In Australia, la bauxite è estratta da operazioni a cielo aperto a Weipa nel Queensland, a Gove nel Territorio del Nord e nel Darling Range in Australia occidentale. Inoltre, nuove miniere hanno recentemente iniziato a funzionare nella regione di Cape York nel Queensland e nella Tasmania centrale. Altri depositi di bauxite si trovano nel nord dell’Australia Occidentale, nel Nuovo Galles del Sud e nel Queensland orientale, ma sono attualmente antieconomici.
Le raffinerie di allumina dell’Australia si trovano in Australia Occidentale (Kwinana, Wagerup, Pinjarra e Worsely) e nel Queensland (QAL e Yarwun) e le fonderie di alluminio si trovano in Tasmania (Bell Bay), Queensland (Boyne Island), Victoria (Portland) e New South Wales (Tomago). La Cina è il maggior consumatore mondiale di alluminio e, nonostante la forte produzione interna, importa grandi quantità di allumina e bauxite grezza, rappresentando più del 40% del consumo globale. Altri grandi mercati dell’alluminio sono gli Stati Uniti d’America, il Giappone e l’Europa, ma queste regioni possiedono pochi depositi economici di bauxite e dipendono anch’esse dalle importazioni di bauxite e allumina per le loro raffinerie di allumina e fonderie di alluminio.
Altre informazioni su risorse e produzione.
Mining
L’estrazione del metallo alluminio avviene in tre fasi principali: estrazione del minerale di bauxite, raffinazione del minerale per recuperare l’allumina e fusione dell’allumina per produrre alluminio. La bauxite viene estratta con metodi di superficie (miniere a cielo aperto) in cui il topsoil e lo strato di copertura vengono rimossi da bulldozer e ruspe. Il topsoil viene poi immagazzinato e successivamente utilizzato per rivegetare e ripristinare l’area dopo che l’estrazione è stata completata. La bauxite sottostante viene estratta con caricatori frontali, pale elettriche o escavatori idraulici. Alcuni minerali di bauxite sono semplicemente frantumati, essiccati e spediti. Altri tipi di bauxite vengono trattati dopo la frantumazione mediante lavaggio per rimuovere parte dell’argilla, della silice reattiva e dei residui di sabbia; e poi vengono essiccati in forni rotanti. Il minerale viene caricato su camion, vagoni ferroviari o su nastri trasportatori e trasportato su navi o raffinerie.
Diversi fattori del ciclo di produzione dell’alluminio riguardano l’ambiente e vengono stanziate notevoli risorse per ridurre al minimo l’impatto delle attività di estrazione, raffinazione e fusione sull’ambiente circostante. Viene effettuata la riabilitazione della miniera, facendo ogni sforzo per riportare l’area almeno alle sue condizioni originali. Si fa attenzione alla manipolazione e allo smaltimento del fango rosso delle raffinerie. Questo fango viene solitamente pompato in dighe che vengono sigillate con materiale impermeabile per evitare l’inquinamento della campagna circostante.
Trasformazione
In quasi tutte le operazioni commerciali, l’allumina viene estratta dalla bauxite con il processo di raffinazione Bayer. Il processo, scoperto da Karl Josef Bayer nel 1888, consiste in quattro fasi.
Digestione: la bauxite finemente macinata viene immessa in un’unità riscaldata a vapore chiamata digestore. Qui viene mescolata, sotto pressione, con una soluzione calda di soda caustica. L’ossido di alluminio della bauxite (e la silice reattiva) reagisce con la soda caustica formando una soluzione di alluminato di sodio o liquore verde e un precipitato di silicato di sodio e alluminio.
Clarificazione: il liquore verde o soluzione contenente allumina viene separato dai rifiuti: gli ossidi di ferro e la silice non disciolti che facevano parte della bauxite originale e ora costituiscono i rifiuti di sabbia e fango rosso. Questa fase comporta tre fasi: in primo luogo, i rifiuti di sabbia grossolana vengono rimossi e lavati per recuperare la soda caustica; in secondo luogo, il fango rosso viene separato e, infine, il liquido verde rimanente viene pompato attraverso dei filtri per rimuovere qualsiasi impurità residua. La sabbia e il fango vengono pompati insieme in laghi di residui e il liquido verde viene pompato in scambiatori di calore dove viene raffreddato da 1000°C a circa 650-790°C.
Precipitazione: l’allumina viene precipitata dal liquido sotto forma di cristalli di allumina idrata. Per fare questo, la soluzione di liquore verde viene mescolata in alti recipienti di precipitazione con piccole quantità di allumina cristallina fine, che stimola la precipitazione dell’idrato di allumina solido mentre la soluzione si raffredda. Una volta completato, l’idrato di allumina solido passa alla fase successiva e il liquore rimanente, che contiene soda caustica e un po’ di allumina, torna nei digestori.
Calcinazione: l’idrato di allumina viene lavato per rimuovere il liquore rimanente e poi asciugato. Infine, viene riscaldato a circa 1000°C per scacciare l’acqua di cristallizzazione, lasciando l’allumina – un materiale secco, bianco puro e sabbioso. Una parte dell’allumina può essere lasciata nella forma di idrato o ulteriormente lavorata per l’industria chimica.
L’allumina viene trasformata in alluminio attraverso un processo di fusione. Tutta la produzione commerciale di alluminio si basa sul processo di fusione di Hall-Héroult in cui l’alluminio e l’ossigeno nell’allumina sono separati per elettrolisi. L’elettrolisi comporta il passaggio di una corrente elettrica attraverso una soluzione fusa di allumina e criolite naturale o sintetica (fluoruro di sodio e alluminio). La soluzione fusa è contenuta in celle di riduzione o vasi che sono rivestiti sul fondo con carbonio (il catodo) e sono collegati in una serie elettrica chiamata potline. Inseriti nella parte superiore di ogni pentola ci sono anodi di carbonio, il cui fondo è immerso nella soluzione fusa.
Il passaggio di una corrente elettrica fa sì che l’ossigeno dell’allumina si combini con il carbonio dell’anodo formando anidride carbonica. L’alluminio metallico fuso rimanente si raccoglie al catodo sul fondo della pentola. Periodicamente, viene travasato e trasferito in grandi forni di mantenimento. Le impurità vengono rimosse, vengono aggiunti gli elementi di lega e l’alluminio fuso viene fuso in lingotti.
Il processo di fusione è continuo. Man mano che il contenuto di allumina del bagno di criolite si riduce, ne viene aggiunta altra. Il calore generato dal passaggio della corrente elettrica mantiene il bagno di criolite allo stato fuso in modo da sciogliere l’allumina. Una grande quantità di energia viene consumata durante il processo di fusione; da 14.000 a 16.000 kilowattora di energia elettrica sono necessari per produrre una tonnellata di alluminio da circa due tonnellate di allumina. L’alluminio è talvolta definito “elettricità solida” a causa della grande quantità di energia utilizzata nella sua produzione. La disponibilità di elettricità a basso costo è quindi essenziale per una produzione economica.
I lingotti di alluminio sono prodotti in varie forme e dimensioni a seconda del loro uso finale. Possono essere laminati in lastre, fogli, lamine, barre o tondini. Possono essere trafilati in fili che vengono trasformati in cavi per le linee di trasmissione elettrica. Le presse estrudono i lingotti in centinaia di diverse forme utili e decorative o gli impianti di fabbricazione possono convertirli in grandi forme strutturali.