オーストラリアの最重要課題に地球科学を応用
はじめに

アルミホイルです。 出典
清涼飲料水の缶のような日用品から、上空を飛ぶ飛行機まで、アルミニウムはあなたの周りにあふれています。 アルミニウムは、人類が知る限り最も有用な材料の1つです。 他のほとんどの金属と合金化(混合)することができ、有用な特性を持つ材料を作ることができます。
酸素とケイ素に続いて、アルミニウムは地殻で 3 番目に多い元素 (8.2%) であり、圧倒的に豊富な金属です。 銅、金、鉛、鉄、亜鉛など、何千年も前から人類が利用してきた金属とは異なり、アルミニウムが一般に使われるようになったのは、わずか100年余りのことです。 これは、アルミニウムが自然界に純粋な状態で存在することがないためです。
アルミニウムはいくつかの粘土から(非経済的に)抽出することができますが、最も一般的なアルミニウム鉱石はボーキサイトと呼ばれる物質です。
アルミニウムはいくつかの粘土から(不純物として)抽出できますが、最も一般的なアルミニウム鉱石はボーキサイトと呼ばれる物質です。まずアルミニウム鉱石を採掘し、ボーキサイトをアルミナ(酸化アルミニウム)に精製する必要があります。
特性
アルミニウムは銀色の金属で、自然界ではそれ自体で見つかることはまずありません。 非常に軽く (銅の約 3 分の 1 の重さ)、かつ強く、合金によっては鋼鉄よりも強いものもあります。 アルミニウムは可鍛性(プレスして形を作ることができる)と延性(叩いて線状にすることができる)の両方があります。 アルミニウムは非常に優れた熱および電気伝導性を持っています。 また、錆びにくく、毒性もありません。 アルミニウムは他のほとんどの金属と合金にすることができます。 アルミニウムは可燃性で、非磁性、非火花性です。 These properties have made it an important metal in the modern world. As aluminium is such a reactive metal, you might think it would rust badly and therefore be useless. However, pure aluminium reacts very quickly with air or water to form a thin, almost invisible layer of aluminium oxide on its surface, which then acts as a protective coating preventing any further ‘rusting’.
|
The Properties of Aluminium |
|
|---|---|
|
Chemical symbol |
Al – from the Roman word Alumen – the word for the aluminium-potassium compound alum |
|
Ore |
Bauxite |
|
Relative density |
2.7 g/cm3 |
|
Hardness |
2.75 on Mohs scale |
|
Malleability |
High |
|
Ductility |
High |
|
Melting point |
660°C |
|
Boiling Point |
2470°C |
Uses

Aluminium-bodied Austin “A40 Sports” (c. 1951). 出典 Wikimedia Commons
Aluminium is smelted from alumina which is refined from bauxite ore. All three products have a number of uses.
More than 90% of the world’s bauxite production is used to make alumina with most of the remaining 10% used by the abrasive, refractory and chemical industries. Bauxite is also used in the production of high-alumina cement, as an absorbent or catalyst by the oil industry, in welding rod coatings and as a flux in making steel and ferroalloys.
Alumina’s primary use is as feedstock for aluminium smelters, however it is also used for other industrial purposes. It is used in glass, porcelain and in metallic paints, such as those sprayed on cars.
天然で結晶状態のアルミナは、コランダムという鉱物と呼ばれています。 また、コランダムの結晶に、微量のクロム、鉄、チタン、銅、マグネシウムが混入していることがある。 このような結晶をルビーやサファイアと呼んでいる。
鉄と鋼に次いで、アルミニウムは地球上で最も広く使われている金属です。 銅、亜鉛、マグネシウム、マンガン、シリコンとよく合金にされ、これらの合金に少量のジルコニウム、ハフニウム、スカンジウムを加えると、強度が著しく改善されます。 アルミニウム自体は、専門的な航空機の製造からナイフやフォークのような日常品まで、幅広い用途を持っています。 下の表は、その用途の一部です。
|
Use |
Description |
|---|---|
|
Building and construction |
Cladding, doors, window frames, awnings and bridge rails as aluminium is strong, light, easily shaped and resistant to rust. |
|
Transport |
Parts for cars, trucks, buses, aircraft, ships, rail and trams as aluminium is strong, light, easily shaped and resistant to rust. |
|
Appliances |
Fridges, washing machines, lawn mowers etc. due to its strength, malleability and rust resistance. |
|
Heating and ventilation |
Heating and cooling systems as aluminium is a good conductor of heat. |
|
Packaging |
Kitchen foil, packaging foil, cans and containers (worldwide, four out of every five drink cans are made of aluminium) as aluminium can be rolled into very thin sheets and is non-toxic. |
|
Electrical and communications |
Power transmission including towers, electrical conduits, superconductors, machinery and equipment, telephone cables and capacitors because of aluminium’s ability to conduct electricity. |
|
Other |
Utensils (cutlery, pans), industrial machinery, chemical industry, production of steel, antiperspirants, furniture, reflectors in telescopes, making high octane petrol, road signs, antacids and jewellery due to its many useful properties. |
History
Around 5300 BC: The Persians made extra strong pots from clay containing aluminium oxide.
Around 2000 BC: The ancient Egyptians and Babylonians used potassium aluminium sulphate KAl(SO4)2 as a medicine to reduce bleeding. It was sourced from naturally occurring deposits in Greece and Turkey. The ancient Romans called this medical compound “alum”, which is where we get the modern day word and symbol from.
中世。 ミョウバンのほとんどは教皇領のトルファからもたらされていましたが、1600年代初頭にヨークシャーでミョウバン頁岩の大きな鉱床が発見されると、価格は劇的に下落しました。 その後何世紀にもわたり、ミョウバンは主に紙の防腐剤と布を染めるための定着剤の2つの分野で使用されました。
1808: イギリス人のサー・ハンフリー・デイヴィーが電気分解によってアルミニウムを抽出しようとしました。
1821年:フランスの地質学者ピエール・ベルティエが、フランスのプロバンス地方にあるレ・ボー村の近くでアルミニウムを多く含む物質を発見しました。
1825年。
1827年:ドイツの化学者Friedrich Wöhlerは、Oerstedのプロセスを改良し、無水塩化アルミニウムにカリウムを反応させてアルミニウムを粉末として抽出しました。 フランスの化学者Henri Saint-Claire Devilleは、より高価なカリウムの代わりにナトリウムを使って、固形のアルミニウムの棒を得ることに成功した。 このアルミニウム棒は非常に貴重なものとされ、同年、フランスの王冠の宝石と並んで展示されました
1886: 別々の大陸に住む2人の科学者(アメリカのチャールズ・ホールとフランスのポール・ヘロー)が、溶融氷晶石(フッ化アルミニウムナトリウム)での電気分解によってアルミニウムを経済的に生産する方法を独自に発見した。 ちなみに、2人とも1864年に生まれ、1914年に亡くなっています。
1887年。 ロシアで活動していたオーストリアの化学者カール・ヨーゼフ・ベイヤーが、ボーキサイトからアルミナを抽出する方法を開発しました。
1888:
1888年:ホールがピッツバーグ・リダクション社(1907年からアルコア社として知られる)を設立しました。 ホール・ヘロルトとバイエルの発見により、アルミニウムの価格は80%も急落しました。 1888年、アルミニウムの価格は1ポンドあたり4.86ドルでした。 1893年には1ポンド0.78米ドル、1930年代後半には1ポンド0.20米ドルとなり、2000以上の用途がありました。

F-16戦闘機は、初期の戦闘機よりも比較的安価に製造でき、メンテナンスが簡単なように設計されています。 機体は、約80%が航空グレードのアルミニウム合金、8%が鋼鉄、3%が複合材料、1.5%がチタンで作られています。 出典はこちら。 Wikimedia Commons, Master Sgt. Andy Dunaway
1911年。 ドイツの化学者アルフレッド・ウィルムは、航空機などの製造に十分な堅固さを持つ、重要なアルミニウム合金を開発しました。
1922年、第二次世界大戦と朝鮮戦争で、それまで木や布で作られていた航空機に、アルミニウムの大きな需要が生まれました。
1955年:アルミホイルが製造されました。
1955: オーストラリアで最初のアルミニウム製錬所がタスマニアのベル・ベイに開設されました。 アルミニウムのソフトドリンク缶が初めて製造されました。
1961: アルコアがオーストラリア・アルコアを設立。
1963: アルコア・オーストラリアが、西オーストラリアのクウィナナにオーストラリア初のアルミナ精製所を開設する。
そして今日。 2016年、推定5760万トンのアルミニウムが生産されました。 これは、他のすべての非鉄金属を合わせたよりも多い。 オーストラリアは、クイーンズランド州、西オーストラリア州、ノーザンテリトリー、タスマニア州でボーキサイトを採掘しており、世界最大のボーキサイト生産国である。 また、オーストラリアはアルミナとアルミニウムの生産でも世界をリードしている。 西オーストラリアの 3 つの精錬所は、オーストラリアのアルミナの 45%、世界全体の 11% を供給し、世界最大のアルミナの単一供給源となっています。
形成

ウェイパボーキサイト、R30128
. 出典はこちら。 Geoscience Australia.
ボーキサイトは最も一般的なアルミニウムの鉱石です。 ボーキサイトは、アルミナを含む様々な岩の上に、ラテライトまたはドゥリクラストとして知られている風化したカバーまたはブランケットとして発生します。 大量の降雨が母岩中の移動性の高い元素を溶かし出し、比較的移動性の低いアルミニウムと若干のケイ素、鉄、チタンを残すことで形成される。
ボーキサイトの主なアルミニウム鉱物は、ギブサイト、ベーマイト、ダイアスポアで、ベーマイトの多形(代替形態)であるが、より緻密で硬い。 純粋なアルミナ(Al2O3)には52.9%のアルミニウムと47.1%の酸素が含まれている。 ボーキサイトは非常に硬い場合と泥のように柔らかい場合があり、圧縮された土(破砕性と再セメント性の両方)、小さな球(ピソライト)、または中空の小枝状の物質(チューブル)として存在することがあります。 色はバフ色、ピンク色、黄色、赤色、白色、またはこれらの組み合わせがあります。
資源
ボーキサイト鉱石は、経済的に採掘できるように、十分に高いレベルのアルミニウム酸化物、適切に低いレベルの酸化鉄 (Fe2O3) とシリカ (SiO2) を含んでいます。 反応性シリカの量は、このシリカの形態がアルミナを作るために必要な苛性ソーダを消費するので特に重要であり、したがって、低反応性シリカが望ましいです。
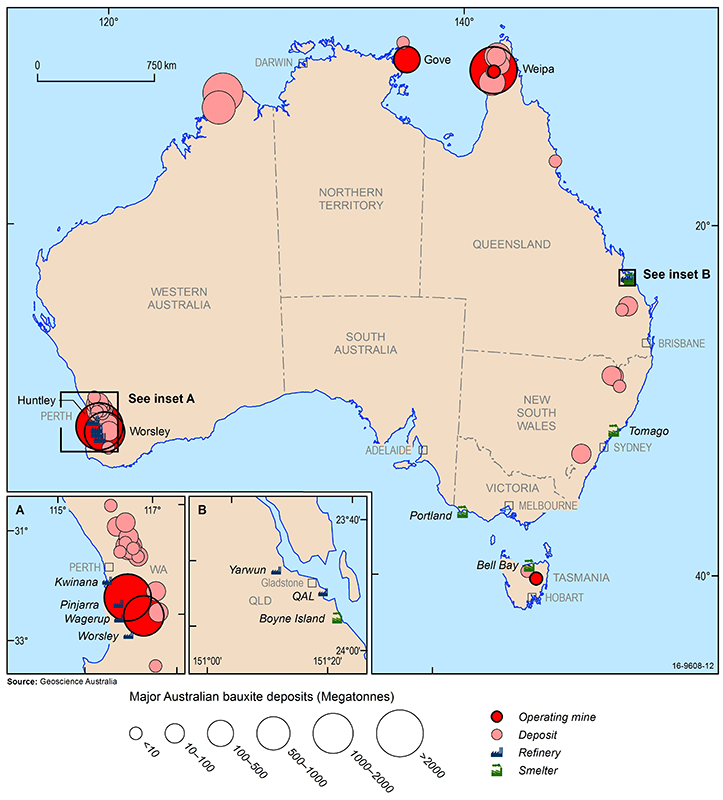
オーストラリアの主要ボーキサイト鉱床、鉱山、アルミナ精錬所、アルミニウム精錬所(2016年)。 Source: Geoscience Australia.
世界最大の経済的ボーキサイト資源は、ギニア、オーストラリア、ブラジル、ベトナム、ジャマイカで発生しています。 オーストラリアでは、ボーキサイトは、クイーンズランドのWeipa、ノーザンテリトリーのGove、西オーストラリアのDarling Rangeで確立されたオープンカット事業から採掘されています。 さらに最近、クイーンズランド州ケープ・ヨーク地域とタスマニア州中央部で新しい鉱山が操業を開始した。
オーストラリアのアルミナ精製所は、西オーストラリア州(クウィナナ、ウェゲラップ、ピンジャラ、ウォーズリー)とクイーンズランド州(QAL、ヤーウォン)にあり、アルミニウム精錬所はタスマニア(ベルベイ)、クイーンズランド(ボイン島)、ビクトリア(ポートランド)、ニューサウスウェールズ(トマゴ)にある。 中国は世界最大のアルミニウム消費国であり、強力な国内生産にもかかわらず、大量のアルミナと原料ボーキサイトを輸入しており、世界消費の40%以上を占めています。 その他の大きなアルミニウム市場は、アメリカ合衆国、日本、ヨーロッパであるが、これらの地域には経済的なボーキサイト鉱床がほとんどなく、アルミナ精製所とアルミニウム製錬所のためにボーキサイトとアルミナの輸入に頼っているのも事実である。
さらなる資源と生産に関する情報
アルミニウム金属の抽出は、ボーキサイト鉱石の採掘、アルミナを回収するための鉱石の精製、アルミニウムを生産するためのアルミナの精錬の3つの主要な段階で行われます。 ボーキサイトは、ブルドーザーやスクレーパーによって表土と表土を除去する地表法(露天掘り)によって採掘されます。 表土は保存され、採掘終了後に緑化や復元に利用される。 下層のボーキサイトは、フロントエンド・ローダー、パワーショベル、油圧ショベルなどで採掘される。 ボーキサイト鉱石の中には、単に粉砕し、乾燥させて出荷するものもあります。 その他のボーキサイトは、破砕後、粘土、反応性シリカ、砂くずの一部を取り除くために洗浄処理を行い、ロータリーキルン内で乾燥させます。 鉱石はトラックや鉄道車両、ベルトコンベアーに積み込まれ、船舶や精錬所に輸送される。
アルミニウム生産サイクルの多くの要素が環境に関連しており、採掘、精錬、製錬が周辺環境に与える影響を最小限に抑えるために、かなりの資源が割り当てられています。 鉱山の修復は、少なくとも元の状態に戻すためにあらゆる努力を払って行われます。 製錬所から出る赤泥の取り扱いや廃棄に注意する。 赤泥は通常、ダムに圧送され、不浸透性材料で密閉され、周辺地域の汚染を防止しています。
加工
ほとんどすべての商業的事業において、アルミナはバイエル精製プロセスによってボーキサイトから抽出されます。
消化:細かく砕かれたボーキサイトは、消化器と呼ばれる蒸気加熱装置に供給されます。 ここで、苛性ソーダの高温溶液と圧力下で混合されます。 ボーキサイトの酸化アルミニウム(および反応性シリカ)は、苛性ソーダと反応して、アルミン酸ナトリウムまたは緑液の溶液とケイ酸ナトリウムの沈殿物を形成します。
清算:緑液またはアルミナ含有溶液は、元のボーキサイトの一部であり現在は砂と赤泥廃棄物を構成する溶解しない酸化鉄とシリカの廃棄物と分離されています。 まず、粗い砂状の廃棄物を取り除き、洗浄して苛性ソーダを回収する。次に、赤泥を分離し、最後に残った緑泥をポンプで送り、残留する不純物を取り除くという3つの段階を経る。 砂と泥は残留湖に一緒にポンプで送られ、生液は熱交換器に送られ、1000℃から約650~790℃に冷却されます。
沈殿:アルミナは、水和アルミナの結晶として酒から沈殿されます。 そのために、背の高い沈殿槽の中で緑色の液体に少量の細かい結晶のアルミナを混ぜ、液体が冷えると固体の水和アルミナの沈殿を促します。
焼成:アルミナ水和物は洗浄され、残った液体を除去し、乾燥させます。 最後に、約1000℃に加熱して結晶水を飛ばし、乾燥した純白の砂状のアルミナを得る。
アルミナは製錬工程を経て、アルミニウムになります。
アルミナは製錬工程を経てアルミニウムになります。アルミニウムの商業生産はすべて、アルミナ中のアルミニウムと酸素を電気分解によって分離するホール-ヘロー製錬工程に基づいています。 電解では、アルミナと天然または合成の氷晶石(フッ化アルミニウムナトリウム)の溶融液に電流を流す。 溶融した溶液は、底に炭素(陰極)を敷き詰めた還元セルまたはポットに入れられ、ポットラインと呼ばれる電気的直列に接続されます。
電流が流れると、アルミナの酸素が陽極の炭素と結合し、炭酸ガスが発生します。 残った溶けた金属アルミニウムは、鍋の底にある陰極に溜まる。 定期的に吸い上げられ、大きな保持炉に移される。 不純物を取り除き、合金元素を加え、溶けたアルミニウムはインゴットに鋳造される。
製錬工程は連続したものである。
製錬工程は連続的なもので、氷晶石浴のアルミナ含有量が減少すると、より多く添加される。 電流のパスによって発生する熱は、アルミナを溶解するように、その溶融状態で氷晶石浴を維持します。 約2トンのアルミナから1トンのアルミニウムを生産するために、14,000〜16,000キロワット時の電気エネルギーが必要である。 アルミニウムは、その製造に使われる電力量が多いことから、「固体電気」と呼ばれることもある。
アルミニウムのインゴットは、最終用途に応じて、さまざまな形や大きさで生産されます。 圧延して板、シート、箔、棒、ロッドにすることができます。 また、線引きされて、送電線用のケーブルに撚り合わされることもあります。 プレス機で押し出されたインゴットは、何百種類もの有用かつ装飾的な形状に加工され、加工工場では大きな構造物の形状に変換されることもあります
。