2.3D: Separation Theory
一般論
TLCはサンプル中の混合物を分離するための優れた分析ツールである。 このセクションでは、分離の詳細について説明し、セクション2.1.Bの一般的な議論を展開します。
すべての形態のクロマトグラフィーにおいて、サンプルは固定相と移動相の間で平衡化します。
TLCのほぼすべての用途において、固定相はシリカまたはアルミナ吸着剤で、移動相はプレートを上昇する有機溶媒または溶媒混合物(「溶離液」)です(式3)。
シリカゲルは、ケイ素-酸素結合のネットワークと、その表面の水分子の層からなります(図2.16に示すとおり)。 ここではシリカゲルを使用していますが、構造的にはアルミナ に類似しています。 この極性の高い固定相と、比較的非極性の移動相(有機溶媒または溶液)を組み合わせたものが順相TLCと呼ばれるものである。
図2.16は、アセトフェノンが分子間力 (IMF) によってシリカゲルの表面に付着する様子を示しています。 この場合、アセトフェノンは酸素原子を介してシリカ表面に水素結合(図2.16aに示すIMF)することができます。 溶離液が試料上を流れると(図2.16b)、試料は固定相に吸着され、移動相に溶解するという平衡が確立されます。 移動相に溶けた化合物は、液の流れにのってプレートの上を移動し(図2.16c)、その後プレートのさらに上の固定相に再吸収されます。
.png?revision=1&size=bestfit&width=1110&height=395)
2 つの相の間の平衡分布は、いくつかの要因に依存します:
- それはサンプルと固定相の間の分子間力の強さに依存します。
シリカまたはアルミナと強い IMF を形成する化合物はしばしば固定相に有利で、溶出時間の大部分は板に付着して過ごすことになります。
酸素原子や窒素原子を持つ化合物は、固定相と水素結合できる(固定相と強いIMFを持つ)ため、ロンドン分散力(LDF)でのみ相互作用できる同サイズの化合物よりも低い値を示すはずである。 - 試料と移動相の間の相互作用の強さに依存します。
順相TLCでは移動相は常に固定相より極性が低いため、極性化合物は非極性化合物より移動相への親和性が低くなる傾向があります(「同溶体」の原則に基づく)。 したがって、極性化合物は非極性化合物よりも溶出時間が短く、プレート上を「ゆっくり」移動し、低い୧⃛(๑⃙⃘◡̈๑⃙⃘)୨⃛を持つことになります。
固定相と移動相に対する化合物の引力の程度は、同じ結論を導きます:
- 固定相との間に強いIMFの可能性があるほど(多くの場合、化合物の極性官能基ほど)、化合物が固定されている時間が長くなり、 \(R_fabulous) lower \(R_fabulous) となります。
- 極性官能基が多いほど、極性の低い溶離液に引き寄せられない傾向があり、化合物が移動する時間は短くなります♪
従って、低位にある化合物は、高位の化合物に比べて極性官能基が多い傾向があります(図2にまとめました。
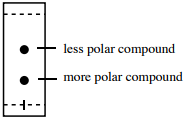
Rf に対する極性の関係: 極性がより高い化合物の上にある。