Allt om livmoderhalscancer
Vad är livmoderhalsen?
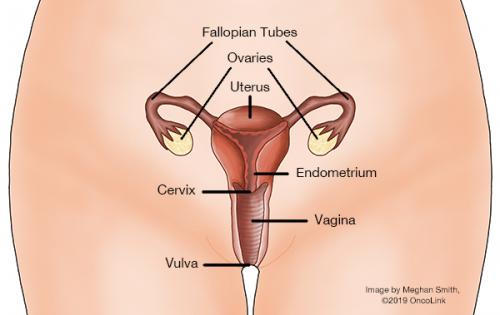
Livmoderhalsen är benämningen på den lägsta delen av livmodern. Endast kvinnor har en livmoder. Det är i livmodern som ett barn växer och utvecklas när en kvinna är gravid. Under graviditeten växer livmodern mycket i storlek. När en kvinna inte är gravid är livmodern ett litet, päronformat organ som sitter mellan kvinnans ändtarm och urinblåsa. Livmoderhalsen förbinder livmodern med förlossningskanalen (vagina). Din vårdgivare kan titta på din livmoderhals och ta ett cellprov (pap-test) under en rutinmässig bäckenundersökning.
Vad är livmoderhalscancer?
Livmoderhalscancer utvecklas när celler i livmoderhalsen börjar växa okontrollerat. Dessa celler kan också invadera närliggande vävnader eller spridas i hela kroppen. Stora samlingar av celler som växer onormalt kallas tumörer. Vanligtvis är livmoderhalscancer mycket långsamt växande. Under vissa omständigheter kan den dock växa och sprida sig snabbt.
Cancer kännetecknas av de celler som de ursprungligen bildades ur. Den vanligaste typen av livmoderhalscancer kallas skivepitelcancer. Den har sitt ursprung i celler som ligger på livmoderhalsens yta, så kallade skivepitelceller. Skivepitelcancer i livmoderhalsen utgör cirka 80 % av all livmoderhalscancer. Den näst vanligaste formen är adenokarcinom. Den kommer från celler som bildar körtlar i livmoderhalsen. Andelen livmoderhalscancer som är adenokarcinom har ökat sedan 1970-talet, men ingen vet exakt varför. Ungefär 3 % till 5 % av livmoderhalscancer har egenskaper från både skivepitel- och adenokarcinom och kallas för adenoskivala karcinom. Det finns några andra mycket sällsynta typer som småcellscancer och neuroendokrina karcinom, men de är extremt ovanliga.
Vad orsakar livmoderhalscancer och är jag i riskzonen?
Livmoderhalscancer är mycket vanligare i utvecklingsländer än i utvecklade länder. Livmoderhalscancer är den näst vanligaste orsaken till dödsfall i cancer i utvecklingsländer, och 84 % av alla fall av livmoderhalscancer inträffar i underutvecklade områden i Afrika, Latinamerika och Västindien. Den är ganska sällsynt i Förenta staterna. Varje år beräknas 13 800 fall av livmoderhalscancer diagnostiseras i USA. Antalet dödsfall i livmoderhalscancer har minskat med 75 % i de utvecklade länderna under de senaste 50 åren. Den största delen av denna minskning tillskrivs det effektiva införandet av screeningprogram för livmoderhalscancer (HPV-test och/eller Pap-test) i utvecklade länder.
En av de viktigaste riskfaktorerna för livmoderhalscancer är infektion med ett virus som kallas HPV (humant papillomvirus). Det bör betonas att endast en mycket liten andel av de kvinnor som har HPV kommer att utveckla livmoderhalscancer. Bara för att du har HPV betyder det inte att du kommer att få cancer. Nästan all livmoderhalscancer har dock tecken på HPV-virus i sig, så HPV-infektion är en viktig riskfaktor för att utveckla cancer. HPV är en sexuellt överförbar infektion (STI) som är otroligt vanlig i befolkningen. Faktum är att de flesta män och kvinnor i collegeåldern har blivit utsatta för HPV.
HPV är det virus som orsakar genitala vårtor, men att ha genitala vårtor betyder inte nödvändigtvis att du kommer att få livmoderhalscancer. Det finns olika subtyper, eller stammar, av HPV. Det är bara vissa subtyper som sannolikt orsakar livmoderhalscancer. Ofta orsakar infektion med HPV inga symtom alls, tills en kvinna utvecklar en precancerös lesion i livmoderhalsen.
Då det är en riskfaktor för livmoderhalscancer att ha en könssjukdom, är alla riskfaktorer för att utveckla könssjukdomar också en riskfaktor för att utveckla livmoderhalscancer. Dessa inkluderar:
- Har haft flera manliga sexpartners.
- Genom att börja ha samlag i tidig ålder.
- Har haft manliga sexpartners som anses vara högriskpersoner (de har haft många sexpartners och/eller börjat ha samlag i tidig ålder).
- Vara diagnostiserad med någon annan sexuellt överförbar sjukdom (som herpes, gonorré, syfilis eller klamydia).
HIV-infektion är en annan riskfaktor för livmoderhalscancer, men av en något annorlunda anledning. Det verkar som om alla tillstånd som försvagar ditt immunförsvar också ökar risken för att utveckla livmoderhalscancer. Tillstånd som försvagar immunförsvaret är bland annat hiv, att ha genomgått en organtransplantation och Hodgkinlymfom.
En annan viktig riskfaktor för att utveckla livmoderhalscancer är rökning. Rökare löper minst dubbelt så stor risk som icke-rökare att utveckla tumörer i livmoderhalsen. Slutligen verkar kvinnor som lever i fattigdom ha en ökad sannolikhet att utveckla och dö i livmoderhalscancer. Detta kan ha att göra med högre rökningstal eller kanske med hinder för att få årliga screeningundersökningar.
Även någon utan några riskfaktorer kan få livmoderhalscancer. Tidig screening och tidig upptäckt är våra bästa vapen för att minska antalet nya fall av livmoderhalscancer.
Hur kan jag förebygga livmoderhalscancer?
Det finns flera saker som kvinnor kan göra för att minska risken att få livmoderhalscancer. Detta inkluderar:
- Har regelbundna screeningundersökningar: Den drastiska minskningen av antalet fall av livmoderhalscancer och dödsfall i USA beror på HPV- och Pap-testning. Screening kommer att diskuteras mer i nästa avsnitt.
- Förhindra dig att vaccinera dig:
- Tre vacciner, som kallas Gardasil, Gardasil 9 och Ceravix har utvecklats. För närvarande finns endast Gardasil 9 tillgängligt i USA.
- Hpv-vaccinet rekommenderas för alla personer i åldern 12-26 år. Den amerikanska läkemedelsmyndigheten FDA har godkänt vaccinet för användning upp till 45 års ålder, men det är inte alla försäkringsbolag som täcker HPV-vaccinet för personer över 26 år.
- Dessa vacciner har visat sig vara effektiva för att förhindra infektion med vissa HPV-stammar om de ges innan en person exponeras för HPV. Även om du redan har HPV kan du fortfarande bli vaccinerad. Vaccinet kan skydda dig mot andra typer av HPV
- Inom livmoderhalscancer är HPV också en orsak till vulvacancer, vaginalcancer, peniscancer och analcancer samt viss huvud & halscancer. Det orsakar också genitala vårtor och leder till onormala resultat från Pap-testet som resulterar i ytterligare tester eller behandling.
- Du får inte börja röka, och om du redan är rökare är det dags att sluta. Rökning har visat sig minska immunförsvarets förmåga att rensa bort en HPV-infektion.
- Kvinnor kan begränsa antalet sexpartners och senarelägga början av sexuell aktivitet för att minska risken, eftersom fler partners kan öka sannolikheten för infektion.
- Användning av kondom och/eller tanddamm (barriärmetod) kan minska de områden som är exponerade men kan inte förhindra exponering helt.
Vilka screeningtest används för livmoderhalscancer?
Livmoderhalscancer anses vara en sjukdom som går att förebygga. Det tar vanligtvis mycket lång tid för pre-cancerösa lesioner att utvecklas till invasiv cancer. Effektiva screeningprogram i USA har lett till att antalet dödsfall i livmoderhalscancer har minskat drastiskt under de senaste 50 åren. För kvinnor som utvecklar livmoderhalscancer i utvecklade länder har 60 % av dem antingen aldrig genomgått screening eller har inte genomgått screening under de senaste fem åren. Vikten av regelbunden screening av livmoderhalscancer kan inte nog betonas.
Den viktigaste grunden för screening av livmoderhalscancer har varit Pap-testet. Pap är en förkortning av Papanicolaou, testets uppfinnare, som publicerade en banbrytande artikel 1941. Ett Pap-test är lätt att utföra på din vårdgivares kontor. Under en bäckenundersökning använder din vårdgivare en träspatel och/eller en borste för att ta prover av celler från livmoderhalsen. Dessa celler placeras på ett objektglas eller i ett flytande konserveringsmedel och skickas till ett laboratorium där en expert på att undersöka celler i mikroskop kan leta efter cancerförändringar. Många kvinnor tycker att undersökningen är obekväm, men sällan smärtsam. Beroende på resultatet av testet kan din vårdgivare behöva utföra ytterligare undersökningar.
Och även om Pap-testet är mycket effektivt är det inte ett perfekt test. Ibland kan testet missa celler som har potential att bli en invasiv cancer. Testet bör inte utföras när du har menstruation. Och även om insamlingen går perfekt kan även de bästa laboratorierna missa onormala celler. Därför måste kvinnor få testerna utförda regelbundet.
Redan nyligen ändrades screeningrekommendationerna för att fokusera mer på HPV-testning. HPV-testning kan teoretiskt sett hitta den stora majoriteten av kvinnor som löper risk att utveckla livmoderhalscancer genom att identifiera dem med högrisk HPV-infektioner. Det finns över 100 subtyper av HPV och vissa typer är mer benägna att leda till livmoderhalscancer. DNA i livmoderhalsceller kan testas för att identifiera förekomsten av högrisktyper av HPV. HPV-DNA-testet kan användas för uppföljande testning av kvinnor med avvikelser som identifierats vid ett pap-test.
The American Cancer Society rekommenderar följande riktlinjer för screening av livmoderhalscancer:
- Alla kvinnor bör börja screening av livmoderhalscancer vid 25 års ålder.
- Kvinnor mellan 25 och 65 år bör få:
- Primär HPV-testning vart femte år. Detta test är ännu inte tillgängligt på många centra/praktiker.
- Om detta test inte är tillgängligt bör du screenas med co-test, vilket är en kombination av ett HPV- och Pap-test. Detta bör göras vart femte år.
- Om HPV-testning inte finns tillgänglig bör enbart ett Pap-test göras vart tredje år.
- Kvinnor över 65 år som har genomgått regelbundna livmoderhalsundersökningar som varit normala bör inte screenas för livmoderhalscancer.
- Kvinnor som har fått diagnosen livmoderhalsförcancer bör fortsätta att screenas tills de uppfyller något av följande kriterier under de senaste 10 åren:
- 2 negativa, på varandra följande HPV-tester.
- Och 2 negativa, på varandra följande co-tester.
- Och 3 negativa, på varandra följande pap-tester under de senaste 3-5 åren.
- Kvinnor som har fått livmodern och livmoderhalsen bortopererade i en hysterektomi och som inte har någon historia av livmoderhalscancer eller cancerförstadium bör inte screenas.
- Kvinnor som har fått HPV-vaccinet bör fortfarande följa screeningrekommendationerna för sin åldersgrupp.
- Men även om ACS inte rekommenderar screening av livmoderhalscancer varje år bör kvinnor ändå träffa sin vårdgivare för en hälsokontroll.
Kvinnor som löper en hög risk att få livmoderhalscancer kan behöva screenas oftare. Kvinnor med hög risk kan vara kvinnor med hiv-infektion, organtransplantation eller exponering i fosterstadiet för läkemedlet DES. De bör tala med sin läkare eller sjuksköterska för specifika rekommendationer.
Vad är tecknen på livmoderhalscancer?
De tidiga stadierna av livmoderhalscancer har vanligtvis inga symtom. Det är därför det är viktigt att göra screening Pap-test. När en tumör växer i storlek kan den ge olika symtom, bland annat:
- Abnormala blödningar (inklusive blödningar efter samlag, mellan menstruationer, kraftigare/längre menstruationsblödningar eller blödningar efter klimakteriet).
- Abnormala vaginala flytningar (kan vara illaluktande).
- Bäcken- eller ryggsmärta.
- Smärta vid urinering.
- Blod i avföring eller urin.
- Smärta vid samlag.
Flera av dessa symtom är ospecifika och kan representera en rad olika tillstånd. Om du har något av dessa symtom ska du prata med din vårdgivare.
Hur diagnostiseras livmoderhalscancer?
Den vanligaste anledningen till att din vårdgivare söker diagnosen livmoderhalscancer är om du har ett onormalt HPV- och/eller Pap-test. Kom ihåg att dessa tester är screeningtester, inte diagnostiska. Ytterligare tester efter ett onormalt resultat behövs.
Pap-test hjälper till att hitta precancerösa lesioner i livmoderhalsen. En precancerös lesion innebär att det finns celler som ser onormala ut, men de har inte invaderat förbi en vävnadsbarriär i livmoderhalsen; en precancerös lesion kan alltså inte sprida sig eller skada dig. Om den lämnas obehandlad kan dock en precancerös lesion utvecklas till invasiv cancer. Pap-testerna rapporteras som inga onormala celler, atypiska (onormala) celler av obestämd betydelse, låggradiga onormala celler eller höggradiga onormala celler. Beroende på ditt specifika fall kommer din vårdgivare att bestämma hur du ska gå vidare.
- En rapport om inga onormala celler motsvarar ett negativt test, vilket innebär att du helt enkelt behöver göra nästa screening enligt riktlinjerna för screening.
- Atypiska celler av obestämd betydelse kan hanteras på tre olika sätt:
- Upprepapper HPV/Pap-test inom 4-6 månader,
- Kolposkopi: Kolposkopi är ett ingrepp som görs under en bäckenundersökning med hjälp av ett kolposkop, som är som ett mikroskop. Genom att använda ättiksyra på livmoderhalsen och undersöka den med ett kolposkop kan din vårdgivare leta efter onormala områden i livmoderhalsen. Kolposkopi är obekvämt, men inte smärtsamt, och kan göras hos din gynekolog.
- En biopsi är det enda sättet att säkert veta om du har cancer. Den gör det möjligt för din vårdgivare att ta ut celler som kan undersökas i ett mikroskop. När vävnaden har tagits bort kommer en patolog att undersöka provet. En biopsi kan genomföras i samband med kolposkopi.
Din vårdgivare kommer att bestämma hur du ska gå vidare med bearbetningen av ett Pap-test som visar onormala celler av obestämd betydelse, beroende på detaljerna i ditt fall. Om upprepade Pap-test inte är normala kommer du att hänvisas till kolposkopi. Om du testar positivt för HPV kommer du att hänvisas till kolposkopi. I allmänhet kommer de flesta patienter med låggradiga onormala celler eller höggradiga onormala celler omedelbart att hänvisas till kolposkopi. Om du är gravid, tonåring, hiv-positiv eller postmenopausal kan din vårdgivare ha något annorlunda rekommendationer. I vissa fall kommer Pap-testet att visa celler som ser onormala ut men som kan ha kommit från högre upp i din livmoder. Det finns en chans att du, om detta händer, måste få din livmoderslemhinna provtagen. Prata med din vårdgivare om resultaten av ditt Pap-test och om nästa steg efter ett onormalt Pap-test.
Om du har symtom (blödning/utflöde) från livmoderhalscancer kan tumören förmodligen ses vid en bäckenundersökning. Varje gång din vårdgivare kan se en tumör i livmoderhalsen vid en bäckenundersökning kommer den att biopsieras. När onormal vävnad upptäcks vid en kolposkopi kommer den också att tas till biopsi. Det finns några olika sätt att göra en biopsi:
- En stansbiopsi kan användas för att ta bort en liten del av livmoderhalsen.
- LEEP (loop electrosurgical excision procedure) är en annan metod att göra en biopsi där en tunn skiva av livmoderhalsen tas bort.
- Konisering eller konbiopsi kan utföras. Vid en konbiopsi avlägsnas en tjockare del av livmoderhalsen och patologen kan se om cancerceller har invaderat livmoderhalsen. Konusbiopsin har det mervärdet att man ibland kan bota en precancerös lesion som är lokaliserad till ett litet område.
Andra tester som kan utföras som en del av en diagnostisk utredning är bland annat blodprover, leverfunktionstester och hiv-test.
Hur stadieindelas livmoderhalscancer?
När dessa tester är utförda bestäms ett stadium för att hjälpa till att bestämma behandlingsplanen. Cancerstadiet, eller sjukdomens omfattning, baseras på information som samlas in genom de olika tester som görs när diagnosen och utredning av cancern utförs.
Cancerstadier hjälper vårdgivaren att fatta beslut om behandling och vårdplan. Livmoderhalscancer stadieindelas med hjälp av FIGO-systemet (International Federation of Gynecologists and Obstetricians) och TNM-systemet (även kallat tumör – nod – metastaseringssystem). Stadierna för livmoderhalscancer sträcker sig från I-IV. Generellt gäller att ju högre stadium, desto allvarligare är cancern. Stagesystemet är mycket komplext och finns i slutet av den här artikeln som referens. Ditt stadium redovisas på din patologirapport – du kanske vill be om en kopia av denna rapport för dina personliga handlingar. Stagesystemet finns i bilagan för genomgång.
Hur behandlas livmoderhalscancer?
Förcancerösa lesioner
Kvinnor som har förcancerösa lesioner på biopsi efter kolposkopi har några olika alternativ med hur de ska gå vidare. Du kan bestämma dig för ett specifikt alternativ beroende på om du planerar att skaffa barn i framtiden eller inte, ditt nuvarande hälsotillstånd och din förväntade livslängd samt din oro för framtiden och möjligheten att cancern ska komma tillbaka. Du bör tala med din vårdgivare om dina rädslor, farhågor och preferenser.
Om du har låggradiga lesioner kan du välja att inte få någon ytterligare behandling, särskilt om biopsin tog bort hela lesionen. Om du bestämmer dig för detta kommer du att behöva mer frekventa bäckenundersökningar och Pap-tester. Prata med din vårdgivare om hur ofta du kommer att behöva göra dessa undersökningar.
Det finns flera sätt att avlägsna precancerösa lesioner utan att ta bort hela livmodern (och därmed bevara din möjlighet att få barn i framtiden). Alternativen inkluderar:
- Kryokirurgi (frysning av den onormala lesionen).
- LEEP (samma typ av elektrokirurgiskt förfarande som används för biopsier).
- Konisering (den tjockare typen av biopsi som får vävnad under ytan).
- Lasercellborttagning.
Kvinnor som inte har några planer på att skaffa barn i framtiden och som är särskilt oroliga för sina chanser att drabbas av invasiv cancer kan välja att genomgå en hysterektomi (en operation där livmodern och livmoderhalsen avlägsnas). Detta förfarande är mer invasivt än någon av de tidigare nämnda behandlingsmetoderna men kan ge sinnesfrid åt kvinnor som inte vill ha barn.
Kirurgi
Kirurgi används i allmänhet vid livmoderhalscancer i tidigt skede. Målet med kirurgi är att ta bort så mycket sjukdom som möjligt. Den används dock vanligtvis inte om inte all cancer kan avlägsnas vid tidpunkten för operationen. Cancersjukdomar som har stor chans att redan spridas till lymfkörtlarna behandlas inte med kirurgi (lymfkörtlar är små, ärtstora vävnadsbitar som filtrerar och renar lymfan, en flytande avfallsprodukt).
Det finns några olika typer av operationer som kan utföras. Vilken typ av operation beror på tumörens stadium. Kirurgiska ingrepp för livmoderhalscancer inkluderar:
- Trakelektomi – Borttagning av livmoderhalsen, övre slidan och vävnad som omger livmoderhalsen. Lymfkörtlar i bäckenet kan också tas bort.
- Hysterektomi- Borttagning av livmodern och livmoderhalsen. Lymfkörtlar i bäckenet kan också avlägsnas. Beroende på sjukdomens omfattning kan din vårdgivare behöva ta bort vävnader runt livmodern samt en del av slidan och äggledarna.
En av fördelarna med kirurgi hos unga kvinnor är att äggstockarna ibland kan lämnas kvar. Detta gör att de inte drabbas av klimakteriet i tidig ålder. Sjukdomar i högre stadium behandlas vanligtvis med strålning och kemoterapi, men ibland används kirurgi om livmoderhalscancer kommer tillbaka efter att den redan har behandlats.
En bäckenexenteration är reserverad för återkommande livmoderhalscancer. En bäckenexenteration är en stor operation där livmodern, livmoderhalsen, äggledarna, äggstockarna, slidan, blåsan, rektum och en del av tjocktarmen avlägsnas.
Strålebehandling
Strålebehandling har visat sig vara mycket effektiv vid behandling av livmoderhalscancer. Vid strålbehandling används röntgenstrålar med hög energi för att döda cancerceller. Strålbehandling är ett annat alternativ vid sidan av kirurgi för livmoderhalscancer i tidigt stadium. Kirurgi och strålning har visat sig vara likvärdiga behandlingar för livmoderhalscancer i tidigt stadium. Livmoderhalscancer i avancerat stadium behandlas också med strålning. Strålning hjälper också till att undvika operation hos patienter som är för sjuka för att riskera att få narkos. Strålning har fördelen att kunna behandla hela sjukdomen i strålningsfältet, så att lymfkörtlar kan behandlas såväl som primärtumören under samma behandling.
Strålebehandling av livmoderhalscancer kommer antingen från en extern källa (utanför patienten, s.k. extern strålning) eller från en intern källa (inuti patienten, s.k. brachyterapi). Behandlingens längd bestäms av ditt behandlingsteam. Behandlingen tar bara några minuter och är smärtfri.
Den typ av strålbehandling som används beror på tumörens stadium. I alla livmoderhalscancerformer över stadium IB är standardmetoden med strålbehandling att använda extern strålning i kombination med intern brachyterapi. Brachyterapi (även kallad intrakavitär bestrålning) gör det möjligt för din strålningsonkolog att ”öka” stråldosen till tumörstället. Detta ger en extra effekt på tumören samtidigt som de normala vävnaderna skonas. Detta görs genom att föra in ett ihåligt metallrör med två äggformade patroner i din vagina. Därefter placeras en liten radioaktiv källa i röret och patronerna. En dator har beräknat hur länge källan behöver vara där, men vanligtvis, för det som kallas LDR-brachyterapi (low dose rate), behöver du ha källan i några dagar. Detta förfarande utförs på sjukhus eftersom du under dessa få dagar måste ligga kvar i sängen.
En annan typ av brachyterapi, som kallas HDR-brachyterapi (high dose rate), använder kraftfullare källor som bara stannar inne i några minuter. Även om detta alternativ vanligtvis låter mer tilltalande för patienterna finns det en debatt om vilken typ som är effektivast och vissa institutioner föredrar den ena framför den andra. Prata med din vårdgivare om dina alternativ och deras åsikter om HDR kontra LDR för behandling av livmoderhalscancer.
En annan användning av strålning är inom den palliativa vården. Hos patienter med mycket avancerade fall av livmoderhalscancer är målet med behandlingen att lindra smärta eller symtom, snarare än att försöka bota deras sjukdom.
I alla sammanhang kombineras strålning ofta med kemoterapi, och beroende på ditt fall kommer din vårdgivare att tillsammans med dig bestämma vilket behandlingsarrangemang som är bäst för din livsstil och dina önskemål.
Kemoterapi
Trots att tumörer avlägsnas genom kirurgi eller behandlas med strålning finns det alltid en risk för återfall, eftersom det kan finnas mikroskopiska cancerceller kvar i kroppen. För att minska risken för återfall (att cancern kommer tillbaka) kan du erbjudas kemoterapi.
Kemoterapi är användning av läkemedel mot cancer som går genom hela kroppen. De flesta patienter i god medicinsk kondition som får strålning för livmoderhalscancer i stadium IIA eller högre kommer att erbjudas kemoterapi utöver sin strålning. Det kan även erbjudas för fall i tidigare stadier beroende på patienten och hennes sjukdom. Det har gjorts många studier som visar på nyttan av att lägga till kemoterapi till strålning när det gäller att minska dödligheten i livmoderhalscancer.
Det finns många olika kemoterapimediciner, och de ges ofta i kombinationer under en serie av månader. Beroende på vilken typ av kemoterapiregim du får kan du få medicinering varje vecka eller med några veckors mellanrum. De vanligaste regimerna (kombinationerna) använder ett läkemedel som kallas cisplatin i kombination med ett annat läkemedel, vanligtvis etoposid, paclitaxel, topotekan, karboplatin och/eller bevacizumab. Pembrolizumab, albuminbundet paklitaxel, docetaxel, fluorouracil, gemcitabin, ifosfamid, irinotekan, mitomycin, pemetrexed och vinorelbin kan användas som andrahandsbehandling efter återfall. I vissa fall där tumören har vissa genetiska mutationer kan larotrectinib eller entrectinib användas. Din tumör kommer att testas för dessa mutationer.
Det finns för- och nackdelar med var och en av de olika regimerna som din vårdgivare kommer att diskutera med dig. Baserat på din egen hälsa, dina personliga värderingar och önskemål samt biverkningar som du kanske vill undvika kan du tillsammans med dina vårdgivare komma fram till den bästa regimen för din livsstil.
Kliniska prövningar
Det finns kliniska forskningsprövningar för de flesta typer av cancer och alla stadier av sjukdomen. Kliniska prövningar är utformade för att fastställa värdet av specifika behandlingar. Försöken är ofta utformade för att behandla ett visst stadium av cancer, antingen som den första behandlingsformen som erbjuds eller som ett behandlingsalternativ efter att andra behandlingar har misslyckats. De kan användas för att utvärdera mediciner eller behandlingar för att förebygga cancer, upptäcka den tidigare eller hjälpa till att hantera biverkningar. Kliniska prövningar är oerhört viktiga för att öka vår kunskap om sjukdomar. Det är tack vare kliniska prövningar som vi vet vad vi vet idag, och många spännande nya behandlingar testas för närvarande. Prata med din vårdgivare om deltagande i kliniska prövningar i ditt område. Du kan också utforska för närvarande öppna kliniska prövningar med hjälp av OncoLink Clinical Trials Matching Service.
Följande vård och överlevnad
När du har behandlats för livmoderhalscancer måste du följas noga för att upptäcka återfall. Till en början kommer du att ha uppföljningsbesök ganska ofta. Ju längre du är fri från sjukdom, desto mer sällan behöver du gå på kontroller. Din vårdgivare kommer att tala om för dig när de vill ha uppföljningsbesök, Pap-test och/eller skanningar beroende på ditt fall. Din vårdgivare kommer också att göra bäckenundersökningar regelbundet under dina kontorsbesök. Det är mycket viktigt att du låter din vårdgivare veta om alla symtom du upplever och att du håller alla dina uppföljningsbesök.
Rädslan för återfall, relationer och sexuell hälsa, de ekonomiska konsekvenserna av cancerbehandlingen, sysselsättningsfrågor och copingstrategier är vanliga känslomässiga och praktiska frågor som livmoderhalscanceröverlevare upplever. Ditt vårdteam kan identifiera resurser för stöd och hantering av dessa utmaningar som man ställs inför under och efter cancer.
Canceröverlevnad är ett relativt nytt fokus inom onkologisk vård. Med nästan 17 miljoner canceröverlevare enbart i USA finns det ett behov av att hjälpa patienterna att övergå från aktiv behandling till överlevnad. Vad händer härnäst, hur återgår man till det normala, vad bör man veta och göra för att leva hälsosamt framöver? En vårdplan för överlevnad kan vara ett första steg för att utbilda dig själv om hur du ska navigera i livet efter cancer och hjälpa dig att kommunicera på ett kunnigt sätt med dina vårdgivare. Create a survivorship care plan today on OncoLink.
Resources for More Information
National Cervical Cancer Coalition
Provides education about HPV and cervical cancer, support through a ”pals” program that links a woman with another woman who has a similar diagnosis.
Foundation for Women’s Cancers
The Foundation offers comprehensive information by cancer type that can help guide you through your diagnosis and treatment. They also offer the ’Sisterhood of Survivorship’ to connect with others facing similar challenges.
Hope for Two
Dedicated to providing women diagnosed with cancer while pregnant with information, support, and hope.
http://www.hopefortwo.org
Appendix: FIGO Surgical Staging of Cervical Cancer (2018)
|
FIGO Stage |
Description |
|
I |
Cervical carcinoma confined to the cervix (extension to corpus should be disregarded) |
|
IA |
Invasive carcinoma diagnosed only by microscopy. Stromal invasion with a maximum depth of ≤5.0mm |
|
IA1 |
Measured stromal invasion of ≤3.0mm or less in-depth |
|
IA2 |
Measured stromal invasion >3.0mm and ≤5.0mm |
|
IB |
Invasive carcinoma with measured deepest invasion >5 mm (greater than stage IA); lesion limited to the cervix uteri with size measured by maximum tumor diameter. |
|
IB1 |
Invasive carcinoma >5mm depth of stromal invasion and ≤2cm in greatest dimension |
|
IB2 |
Invasive carcinoma >2cm and ≤ 4cm in greatest dimension |
|
IB3 |
Invasive carcinoma >4cm in greatest dimension |
|
II |
Cervical carcinoma invading beyond the uterus but not extended onto the lower third of the vagina or to the pelvic wall |
|
IIA |
Involvement limited to the upper two-thirds of the vagina without parametrial invasion. |
|
IIA1 |
Invasive carcinoma ≤4cm in greatest dimension |
|
IIA2 |
Invasive carcinoma >4cm in greatest dimension |
|
IIB |
Parametrial invasion but not up to the pelvic wall |
|
III |
The carcinoma involves the lower third of the vagina and/or extends to the pelvic wall and/or causes hydronephrosis or non-functioning kidney and/or involves pelvic and/or paraaortic lymph nodes |
|
IIIA |
Tumor involving the lower third of the vagina but no extension to the pelvic wall |
|
IIIB |
Carcinoma involves the lower third of the vagina, with no extension to the pelvic wall |
|
IIIC |
Involvement of pelvic and/or paraaortic lymph nodes (including micrometastases), irrespective of tumor size and extent (with r and p notations). |
|
IIIC1 |
Pelvic lymph node metastasis only |
|
IIIC2 |
Paraaortic lymph node metastasis only |
|
IV |
The carcinoma has extended beyond the true pelvis or has involved (biopsy-proven) the mucosa of the bladder or rectum. A bullous edema, as such, does not permit a case to be allotted to stage IV |
|
IVA |
Spread of the growth to adjacent organs |
|
IVB |
Spread to distant organs |