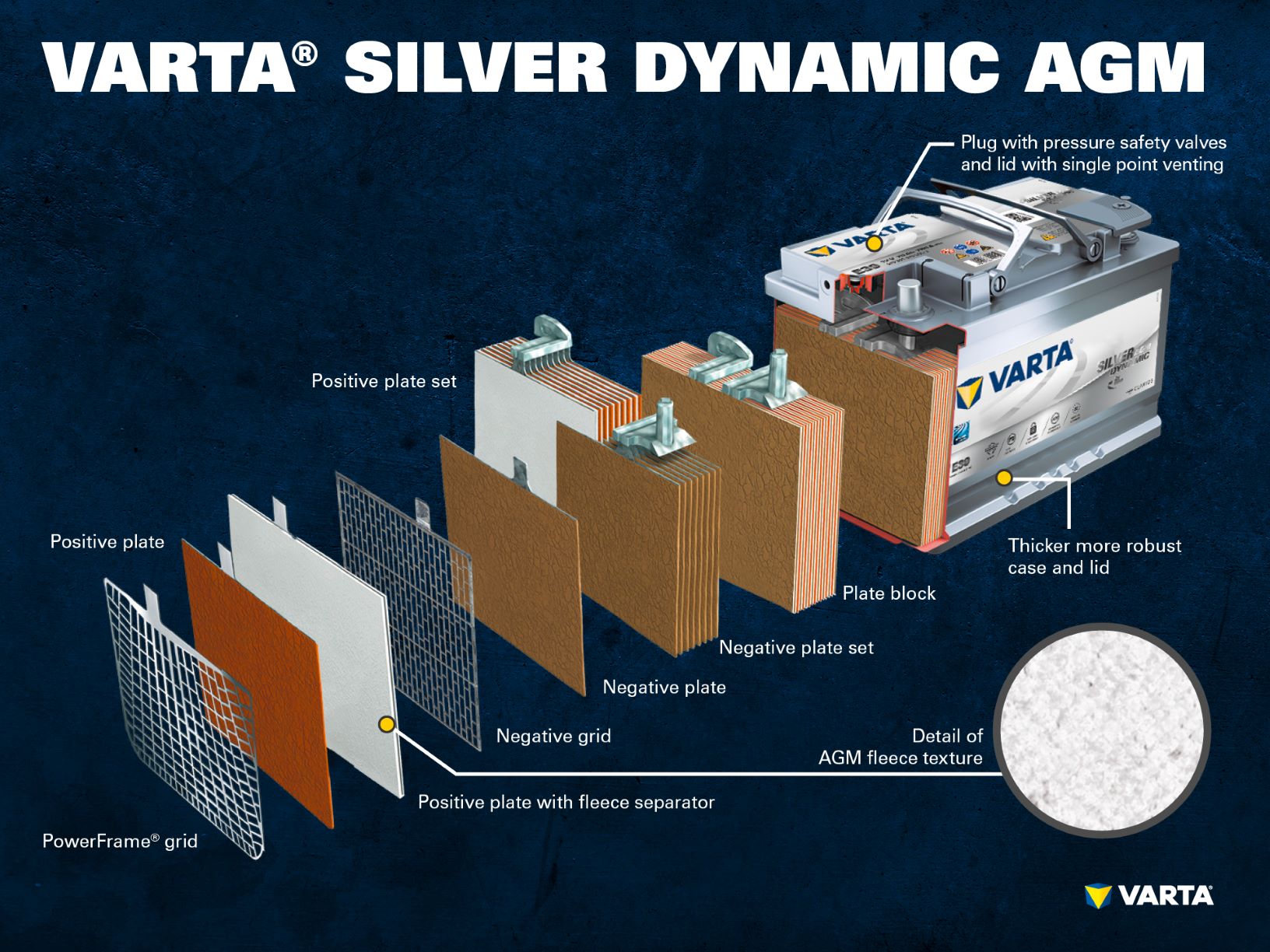
Hur fungerar ett bilbatteri och hur är det konstruerat?
Batteriets traditionella funktion i motorrummet är välkänd: Utan batteriet kan fordonet inte startas. Förutom startmotorn kräver tändstift, glödstift, lampor och elektroniska tillämpningar alla elektrisk energi. Men hur är ett batteri konstruerat och hur fungerar det?
Blybatterier: Komponenter och uppbyggnad
Många förare blir medvetna om bilbatteriernas tunga vikt när de köper ett nytt. Vikter från cirka 10,5 kg, upp till 30 kg är möjliga. Anledningen till detta är blyplattorna i battericellerna.
Komponenter och uppbyggnad av en battericell
Positivelektrod:
- Positivplatta: I ett blybatteri består den positivt laddade plattan (aktivt material) av blyoxid (PbO2) som är nedsänkt i en elektrolyt.
- Positivnät: Det positiva gallret består av en blylegering och används för att hålla det aktiva materialet och som en strömavtagare.
Negativ elektrod:
- Negativ platta: Den negativt laddade plattan (aktivt material) består av rent bly (Pb), som också är nedsänkt i en elektrolyt.
- Negativ platta: Liksom den positiva plattan består denna också av en blylegering och fyller samma funktion.
Elektroderna med olika laddningar är separerade av en separatorpåse.
Elektrolyten är en blandning av svavelsyra (H2SO4) och destillerat vatten. Denna elektrolyt kan vara i flytande form (som i konventionella våtbatterier eller i den förbättrade EFB-tekniken), i gelform eller bunden i en glasmatta (som i AGM-tekniken för nyare start-stopp-tillämpningar).
Flera positiva elektroder bildar en uppsättning positiva plattor och flera negativa elektroder bildar en uppsättning negativa plattor. Tillsammans bildar en negativ och en positiv plattuppsättning ett plattblock. Ett plattblock är en battericell.
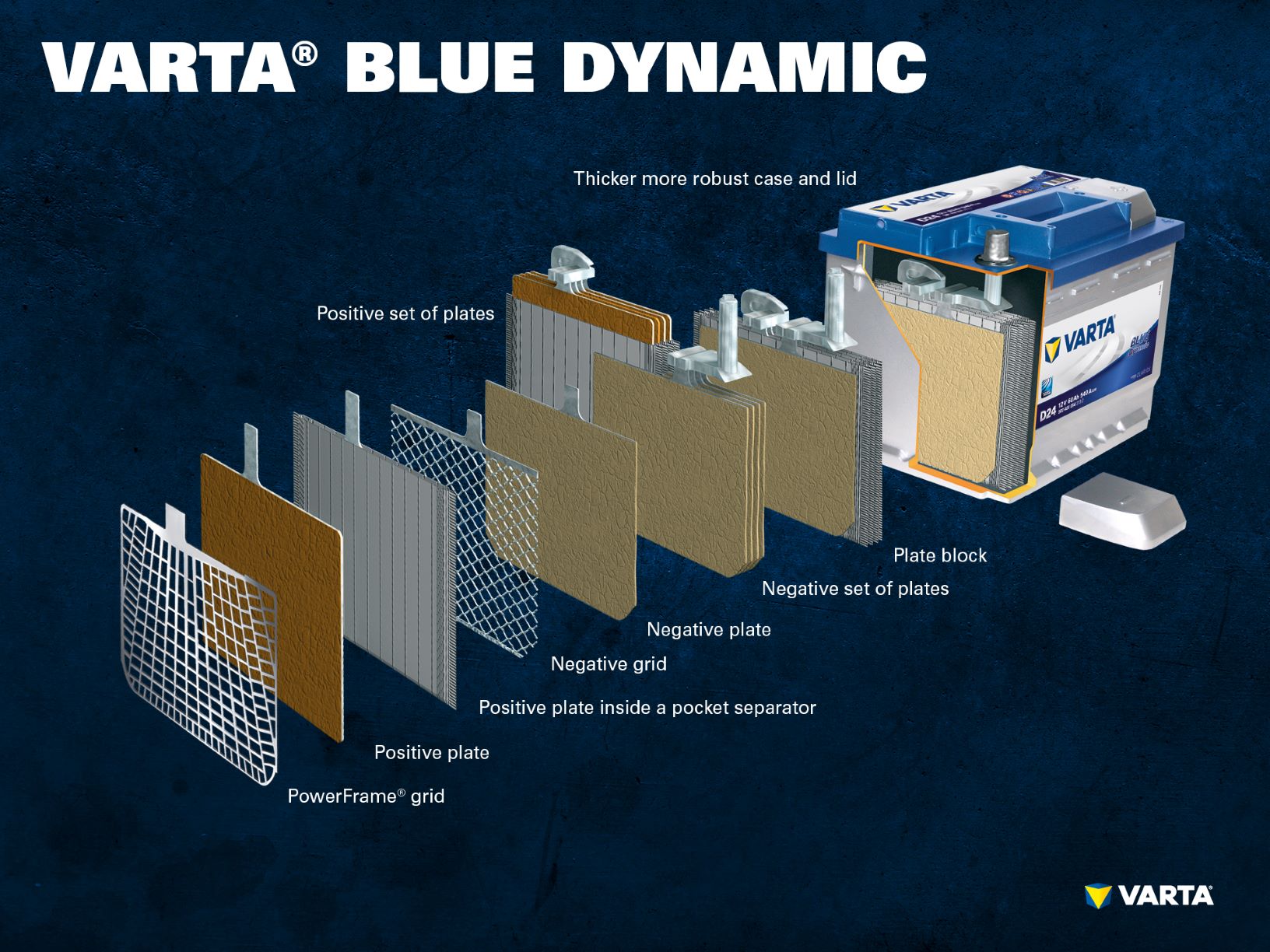
Ett konventionellt startbatteri består av 6 seriekopplade celler, var och en med en nominell spänning på 2 V, vilket resulterar i en spänning på exakt 12,72 V när batteriet är fulladdat. Batteriets kapacitet och kallstartförmåga är ett resultat av antalet plattor per cell.
Tumregel: Ju fler plattor som en cell innehåller och som därför bildar en större yta, desto större kallstartseffekt (CCA) kan batteriet leverera. Om utrymmet i cellen däremot används för färre, men tjockare plattor, ökar cykelstabiliteten. Detta innebär att batteriet är konstruerat för en högre laddningsgenomströmning (kontinuerlig laddnings- och urladdningsprocess).
Cellerna finns i ett hölje som är tillverkat av syrabeständig plast (polypropylen). I ett konventionellt SLI-batteri är detta stängt med ett lock med ett labyrintsystem som hindrar batterivätskan från att läcka ut och separerar vätskan från gasen.
Förr hade batterierna skruvpluggar som gjorde det möjligt att fylla på dem med destillerat vatten. Moderna batterier är helt underhållsfria. Vatten behöver inte och får inte fyllas på. Även om AGM-batterier fortfarande har ”envägspluggar” får dessa inte öppnas under några omständigheter.
Bilbatteriernas funktion: Kemisk energi blir elektrisk energi
Ett bilbatteri lagrar energi i kemisk form och omvandlar den till elektrisk energi. I denna elektrokemiska process reagerar fyra material med varandra:
- Vätgas (H)
- Syrgas (O2)
- Bly (Pb)
- Svavel (S)
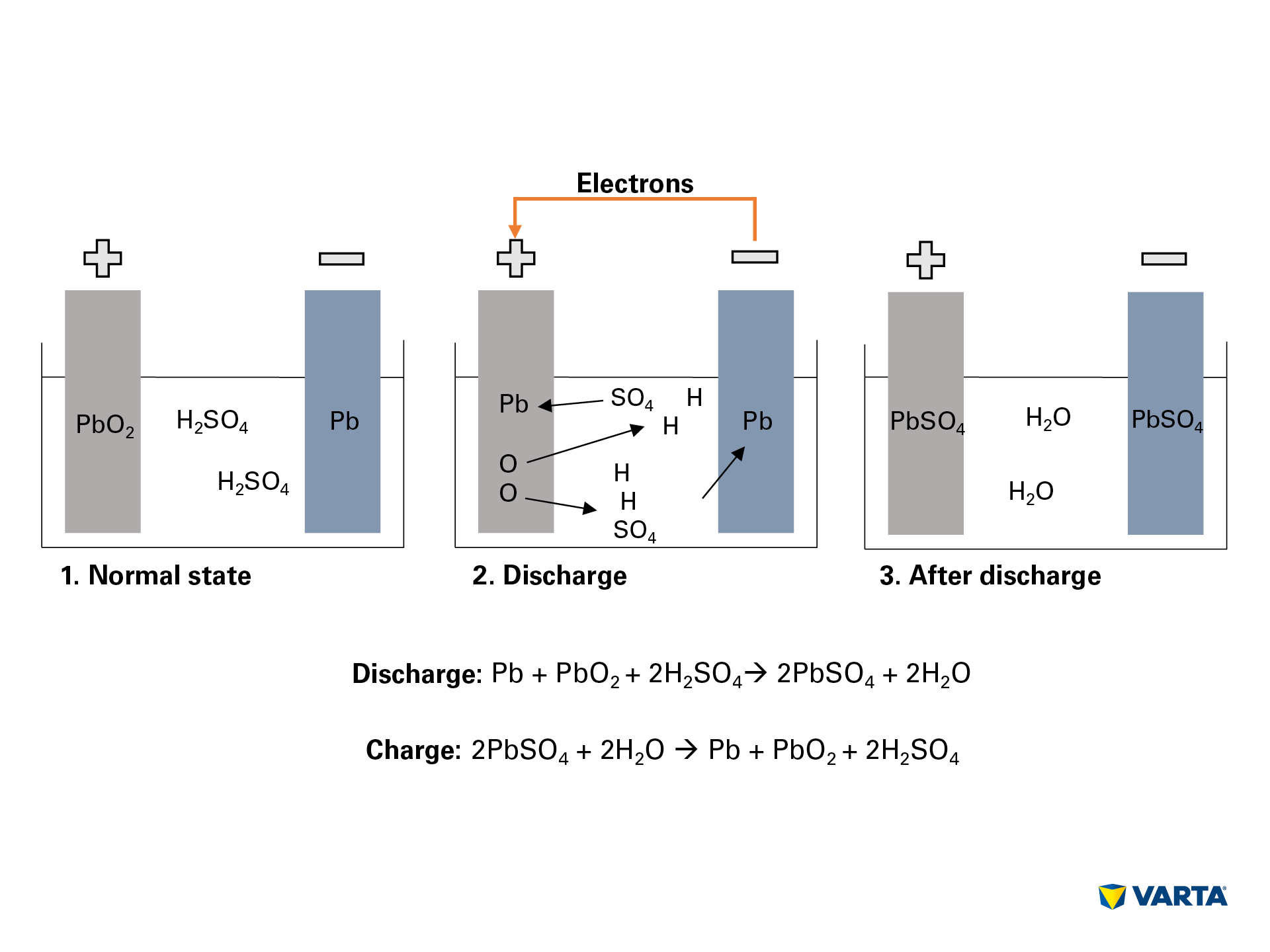
Tillkoppling av en extern förbrukare startar den kemiska reaktionen i batteriet:
- Elektrolyten, en blandning av svavelsyra (H2SO4) och destillerat vatten, sönderdelas till positivt laddade vätejoner (H+) och negativt laddade sulfatjoner (SO42-).
- Tidigare färdas elektroner (2e-) från den negativa till den positiva elektroden via den externa förbrukaren.
- För att kompensera detta elektronflöde färdas sulfatjoner från elektrolyten till den negativa elektroden, där de reagerar med blyet (Pb) för att bilda blysulfat (PbSO4).
- Blysulfat bildas också i den positiva elektroden: Bindningen av syre (O2) i blyoxiden (PbO2) bryts genom överföring av elektroner och syret passerar in i elektrolyten. Det återstående blyet (Pb) binds till sulfat (SO4) från elektrolyten.
- Där binds syret till väte för att bilda vatten (H2O). När svavelsyran förbrukas genom bildandet av blysulfat minskar koncentrationen i elektrolytlösningen. När koncentrationen av svavelsyra sjunker under en viss nivå måste batteriet laddas igen.
- Under laddningen sker de kemiska processerna i omvänd ordning. I slutet kan de ursprungliga elementen återfinnas: Den positiva elektroden består av blysulfat (PbSO4), den negativa elektroden består av rent bly (Pb) och elektrolyten består av utspädd svavelsyra (H2SO4). Eftersom denna omvandlingsprocess är förknippad med förluster kan ett batteri bara klara ett begränsat antal laddningscykler. Dess livslängd är därför begränsad.
Problem med blybatterier: Om ett batteri laddas med en för låg spänning eller om det alltid drivs med en för låg spänning (under 80 %) uppstår syrabeläggning, även kallad skiktning. Syran i elektrolyten skiktas på grund av dålig blandning. Olika tätheter orsakar skiktning av svavelsyra i botten och vatten i det övre området av batteriet. På grund av detta kan endast den mellersta delen av elektrolyten, dvs. endast en tredjedel, användas vid urladdning och laddning.
En möjlig orsak till syraskiktning är främst korta resor med samtidig användning av ett stort antal elektriska förbrukare. I detta fall har generatorn inte tillräckligt med tid för att ladda batteriet. 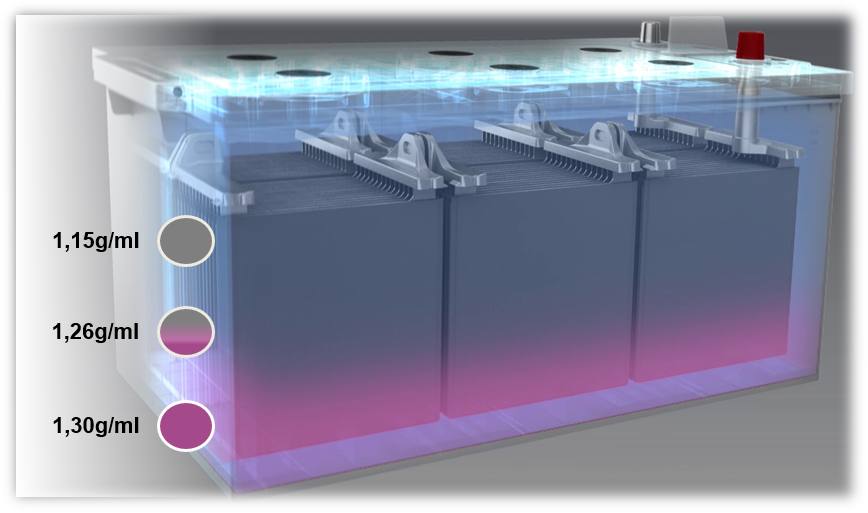
En följd av syrabeläggning är sulfatering. Om detta inträffar i batteriet, eller om det inte ständigt laddas till en tillräcklig nivå, kristalliserar blysulfat (PbSO4) på elektroderna och bildar med tiden större kristallstrukturer. Denna process är känd som ”sulfatering”. Kristalliseringen förhindrar återomvandlingen av blysulfat till de ursprungliga komponenterna bly eller blyoxid, vilket leder till att laddningsacceptans förhindras och att kallstartseffekten minskar.
Skarpa kristaller kan också skada separatorerna eller orsaka kortslutningar i cellerna.
För att motverka denna effekt och förhindra att batteriet går sönder i förtid bör ett batteri aldrig utsättas för en låg laddningsnivå under en längre period. För detta är det lämpligt att testa batteriet regelbundet och vid behov ladda det fullt ut.
Vill du veta mer om det här ämnet? Hur man laddar ett batteri på rätt sätt.
Ny batteriteknik: AGM- och litiumjonbatterier
Härför har konventionella bly-syrabatterier hittills haft en stor andel av marknaden. Marknaden håller dock på att förändras snabbt: Innovativ batteriteknik för start-stopp-fordon, t.ex. AGM, använder syra som är bunden i en matta för att ge större cykelstabilitet och garantera tillförlitlig prestanda i fordon med ökade energibehov. Ytterligare en fördel med AGM är att det inte längre är möjligt att lägga syra i lager på grund av den bundna syran.
En ny generation bilbatterier för mikrohybridfordon arbetar vid 48 V och använder celler med litiumjonteknik.