Respirační selhání – typy a léčba
Obrázek : „Školení KPR-03“ od Ramy. Licence: CC BY-SA 2.0
Definice respiračního selhání
Respirační dysfunkcí se rozumí selhání výměny plynů, tj. pokles arteriální tenze kyslíku, PaO2, pod 60 mm Hg (hypoxemie). Může, ale nemusí ji doprovázet hyperkapnie, tedy PaCO2 vyšší než 50 mm Hg (snížená eliminace CO2).
Normální fyziologie dýchání
U normálních jedinců zůstává „alveolární“ tenze kyslíku PAO2 blízko 100 mmHg, zatímco alveolární tenze oxidu uhličitého PACO2 se udržuje blízko 40 mmHg.
Mezi „alveolární (A)“ a „arteriální (a)“ tenzí kyslíku je malý rozdíl 5-10 mmHg, protože přibližně 2 % systémového srdečního výdeje obchází plicní cirkulaci (fyziologický zkrat) a není okysličováno.
V důsledku směsi malého množství odkysličené krve je PO2 arteriální krve (PaO2) o něco nižší než PO2 alveolárního vzduchu (PAO2). Normální gradient A-a je přibližně < 10 mmHg. Pokud je gradient A-a normální, znamená to, že nedochází k poruše difuze plynů. Gradient A-a pomáhá nastínit různé příčiny respiračního selhání.
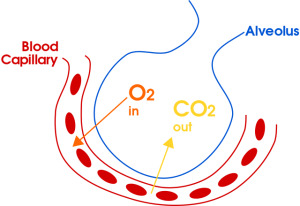
Obrázek: „Gas exchange in the alveolus“ by domdomegg. Licence: CC-BY 4.0
V ustáleném stavu je rychlost produkce oxidu uhličitého v těle konstantní. PACO2 závisí na ventilaci a je jí „nepřímo úměrná“, takže zvýšená ventilace povede ke snížení PACO2 a snížená ventilace způsobí zvýšení PACO2.
Alveolární tenze kyslíku, PAO2, závisí na koncentraci vdechovaného kyslíku (FIO2) a alveolární tenzi oxidu uhličitého (PACO2) podle následující rovnice:
PAO2 = FIO2 × (PB – PH2 O) – PACO2/R
PAO2: Alveolární PO2 FIO2: P2O2: frakční koncentrace kyslíku ve vdechovaném plynu
PB: barometrický tlak PH2O: tlak vodní páry při 37 °C
PACO2: Alveolární PCO2 R: Respirační výměnný poměr.
Typy respiračního selhání
Existují dva typy respiračního selhání, které se klasifikují pomocí analýzy arteriálních krevních plynů (ABG):
Typ I je charakterizován:
- Hypoxemie (PaO2 méně než 60 mmHg)
- Bez hyperkapnie, normální nebo nízký PaCO2 (PaCO2 méně než 50 mmHg)
- Obvykle se vyskytuje v důsledku významného ventilačně-perfuzního nesouladu
Typ II je charakterizován:
- Hypoxémie (PaO2 méně než 60 mmHg) a
- Zvýšená hyperkapnie (PaCO2 více než 50 mmHg)
- Obvykle se vyskytuje v důsledku hypoventilace
Dýchací selhání lze dále klasifikovat jako akutní nebo chronické.
Akutní respirační selhání nastává během několika minut a hodin a obvykle se jedná o urgentní stav. Je charakterizováno život ohrožujícími změnami arteriálních krevních plynů a acidobazického stavu organismu, např. tenzní pneumotorax, plicní embolie, syndrom akutní respirační tísně, anafylaktické reakce.
Chronické respirační selhání nastává postupně v průběhu týdnů a měsíců. Je méně dramatické a není vždy snadno patrné. Ledviny obvykle kompenzují a normalizují acidobazický stav organismu změnou vylučování bikarbonátů a kyselin. Může se také objevit polycytemie, chronická obstrukční plicní nemoc a pneumokonióza.
Patofyziologie hypoxemie
Hypoxemie je snížení arteriálního PO2, zatímco hypoxie je snížená dodávka kyslíku do tkání. U pacientů může dojít k hypoxii i za přítomnosti normálního PaO2, jako v případě otravy oxidem uhelnatým nebo sníženého hemoglobinu (anémie).
Existuje pět důležitých patofyziologických příčin hypoxemie a respiračního selhání.
Hypoventilace
Minutová ventilace závisí na dechové frekvenci a dechovém objemu, což je množství vdechnutého vzduchu během každého normálního nádechu v klidu.
Minutová ventilace = dechová frekvence x dechový objem
Normální dechová frekvence je přibližně 12 dechů za minutu a normální dechový objem je přibližně 500 ml. Minutový dechový objem tedy normálně činí v průměru asi 6 l/min.
Hypoventilace nastává, když dojde ke snížení dechové frekvence a/nebo dechového objemu, takže se za minutu vymění menší množství vzduchu. Dojde ke snížení vstupu kyslíku do alveolů a arterií, což vede ke snížení PaO2. Jak již bylo popsáno, PaCO2 je nepřímo úměrný ventilaci. Hypoventilace tedy povede ke zvýšení PaCO2.
Alveolárně-arteriální gradient bude normální a menší než 10 mmHg, protože nedochází k poruše difuze plynů. V těchto případech se zvýšením ventilace a/nebo zvýšením koncentrace kyslíku upraví odchylka krevních plynů.
Porucha difuze
Při poruše difuze dochází ke strukturálnímu problému v plicích. Může dojít ke zmenšení povrchu (jako u emfyzému) nebo ke zvětšení tloušťky alveolárních membrán (jako u fibrózy a restriktivních plicních onemocnění), což zhoršuje difuzi plynů přes alveoly, což vede ke zvýšení alveolo-arteriálního gradientu. Při zvýšeném gradientu A-a bude alveolární PO2 normální nebo vyšší, ale arteriální PO2 bude nižší. Čím větší je strukturální problém, tím větší bude alveolo-arteriální gradient.
Protože difuze plynů je přímo úměrná koncentraci plynů; zvýšení koncentrace vdechovaného kyslíku tedy upraví PaO2, ale zvýšený gradient A-a bude přítomen, dokud bude přítomen strukturální problém.
Plicní zkrat
Při plicním zkratu, známém také jako pravolevý zkrat, se žilní odkysličená krev z pravé strany dostává do levé strany srdce a systémového oběhu, aniž by se okysličila v plicních sklípcích. Zjednodušeně řečeno, zkrat znamená „normální perfuze, špatná ventilace“. Plíce jsou normálně prokrvené, ale ventilace je snížená nebo chybí, což vede k tomu, že nedochází k výměně plynů s přicházející odkysličenou krví. Poměr ventilace/perfuze je nulový nebo se blíží nule.
Příklad při atelektáze není zkolabovaná plíce ventilována a krev v tomto segmentu se nedokáže okysličit. Při cyanotických srdečních onemocněních krev z pravé strany obchází (shuntuje) plíce a dostává se do levé strany, což způsobuje hypoxemii a cyanózu.
Gradient A-a se zvyšuje, protože odkysličená krev vstupuje do arteriálního (systémového) oběhu, čímž se snižuje arteriální tenze kyslíku, PaO2.
Protože se žilní krev v plicním shuntu nekysličuje, zvýšení koncentrace kyslíku proto hypoxemii nenapraví. Krev bude plíce obcházet bez ohledu na to, jak vysoká je koncentrace kyslíku. Toto nezvýšení PaO2 po podání kyslíku je velmi důležitým bodem a pomáhá při diferenciální diagnostice mezi poruchou difuze a jinými příčinami hypoxemie, která se vyřeší podáním doplňkového kyslíku.
Nesoulad ventilace a perfuze (V/Q)
V/Q je poměr alveolární ventilace (V) a průtoku krve plicnicí (Q). Shoda ventilace a perfuze je nezbytná pro dosažení adekvátní výměny kyslíku a oxidu uhličitého v alveolech. Poměr V/Q se u normálních jedinců pohybuje kolem 0,8, ale tento poměr se mění, pokud dojde k významným poruchám ventilace nebo perfuze.
Ve všech plicních sklípcích není rovnoměrná ventilace a perfuze. Mají tendenci se lišit v důsledku působení gravitace. Na vrcholu plic jsou alveoly velké a zcela nafouknuté, zatímco na bázích jsou malé. Stejně tak prokrvení je větší na bázi plic než na jejich vrcholu. Tím vzniká fyziologický nesoulad ventilace (V) – perfuze (Q) mezi jednotlivými alveoly.
Snížený poměr V/Q (< 0,8) může vzniknout buď v důsledku snížené ventilace (onemocnění dýchacích cest nebo intersticiální plicní choroby), nebo v důsledku nadměrné perfuze. V těchto případech dochází k plýtvání krví, protože se nedokáže správně okysličit. V extrémních podmínkách, kdy se výrazně sníží ventilace a poměr V/Q se blíží nule, se bude chovat jako plicní zkrat.
Zvýšený poměr V/Q (> 0,8) obvykle vzniká při snížené perfuzi (plicní embolie brání průtoku krve distálně od obstrukce) nebo nadměrné ventilaci. V těchto případech dochází k plýtvání vzduchem, který není schopen difundovat v krvi. Za extrémních podmínek, kdy se perfuze výrazně sníží a V/Q se přiblíží hodnotě 1, se alveoly chovají jako mrtvý prostor a nedochází k žádné difuzi plynů.
Zvětšený nesoulad ventilace a perfuze v plicích tedy narušuje procesy výměny plynů, což v konečném důsledku vede k hypoxemii a respiračnímu selhání.
Vysoká nadmořská výška
Ve vysokých nadmořských výškách klesá barometrický tlak (PB), což povede ke snížení alveolárního PO2 podle rovnice:
PAO2 = FIO2 × (PB – PH2 O) – PACO2/R
Snížení alveolárního PAO2 povede ke snížení arteriálního PaO2 a hypoxemii, ale gradient A-a zůstane normální, protože v rámci procesů výměny plynů nedochází k poruše. Za těchto podmínek dodatečný kyslík (zvýšení FIO2) zvýší PAO2 a upraví hypoxemii.
Když člověk náhle vystoupí do vysoké nadmořské výšky, tělo reaguje na hypoxemii hyperventilací, což způsobí respirační alkalózu. Zvýší se koncentrace 2, 3-difosfoglycerátu (DPG), čímž se disociační křivka kyslík-hemoglobin posune doprava.
Chronicky dochází k aklimatizaci a tělo reaguje zvýšením schopnosti krve přenášet kyslík (polycytemie). Ledviny vylučují bikarbonáty a udržují pH v normálních mezích.
| Příčiny hypoxémie | |||
| Cause | PaO2 | A-a gradient | PaO2 response to supplemental oxygen |
| Hypoventilation | Decreased | Normal | Increases |
| Diffusion Impairment | Decreased | Increased | Increases |
| Shunt | Decreased | Increased | Does not increase. |
| V/Q Mismatch | Decreased | Increased | Usually increases (depends on V/Q mismatch type) |
| High Altitude | Decreased | Normal | Increases |
Pathophysiology of Hypercapnia
Hypercapnia occurs when carbon-dioxide tension (PCO2) increases to more than 50 mmHg. As explained above, at a steady-state, the rate of carbon dioxide production within the body is constant. The PACO2 depends on and is inversely proportional to ventilation, so decreased ventilation will cause increased PACO2 and vice versa. Therefore, hypercapnia (along with hypoxemia, Type II respiratory failure) occurs, usually due to conditions that decrease ventilation.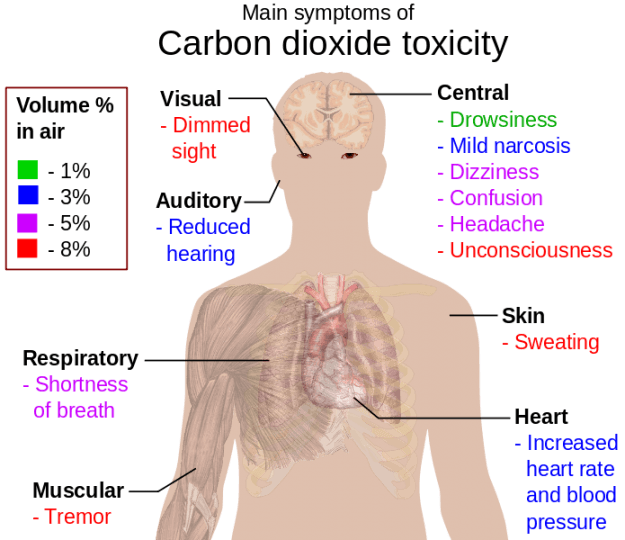
For example:
- Reduced central respiratory drive, e.g.,, předávkování opioidy nebo poranění hlavy
- Obstrukce horních cest dýchacích (cizí těleso, otok, infekce)
- Pozdější těžké akutní astma, CHOPN
- Periferní nervosvalová onemocnění, např, Guillain-Barreho syndrom, myasthenia gravis, botulismus
- Únava dýchacích svalů
Léčba respiračního selhání
Pacienti s akutním respiračním selháním mají zvýšené riziko hypoxického poškození tkání a měli by být přijati na respirační/intenzivní jednotku. Nejprve je třeba zhodnotit a zvládnout stav dýchacích cest, dýchání a oběhu (ABC) pacienta, podobně jako u všech urgentních stavů.
Prvním cílem je upravit hypoxemii a/nebo zabránit hypoxii tkání udržováním arteriální tenze kyslíku (PaO2) 60 mm Hg nebo arteriální saturace kyslíkem (SaO2) vyšší než 90 %. Obvykle je zpočátku účinné poskytování doplňkového kyslíku a mechanická ventilace, která se provádí obličejovou maskou (neinvazivně) nebo tracheální intubací.
Specifická léčba respiračního selhání závisí na základní příčině. Proto bychom se měli snažit identifikovat základní patofyziologické poruchy, které vedly k respiračnímu selhání, a korigovat je poskytnutím specifické léčby, jako jsou steroidy a bronchodilatancia u CHOPN a astmatu, antibiotika u pneumonie a heparin u plicní embolie.
Cíle mechanické ventilace
Mechanická ventilace má dva hlavní cíle:
- Zvýšení PaO2 zvýšením koncentrace vdechovaného kyslíku (FIO2) a pozitivního tlaku na konci výdechu (PEEP).
- Decrease PaCO2 by increasing the ventilation by adjusting the tidal volume and respiratory rate of the mechanical ventilators.
Mechanical ventilation is also an appropriate therapy for respiratory muscle fatigue because it rests the respiratory muscles.
Study for medical school and boards with Lecturio.
- USMLE Step 1
- USMLE Step 2
- COMLEX Level 1
- COMLEX Level 2
- ENARM
- NEET