Vědecké projekty pro začátečníky:
Chemie
Sůl nebo cukr:
Roztoky nejsou nic jiného než směsi různých sloučenin nebo prvků. S roztoky se setkáváte každý den, aniž byste si to uvědomovali.
Také vzduch, který dýcháte a který obsahuje vodu, je roztokem kapaliny a plynu. Pokud jste dnes pili limonádu, pili jste vlastně roztok plynu rozpuštěného v ochucené vodě. Pokud nosíte náramek ze stříbra, máte na sobě roztok dvou kovů.
V tomto experimentu budete pracovat s kapalným roztokem, který je jedním ze tří typů roztoků. Dalšími typy jsou plynné roztoky a pevné roztoky.
Tak co se zdá být problémem?“
Roztok je látka?buď pevná, kapalná, nebo plynná?>, která se rozpouští. Rozpouštědlo?což může být také pevná látka, kapalina nebo plyn?je látka, která se rozpouští. Roztok je stejnorodá směs rozpuštěné látky (obvykle pevné látky) rozpuštěné v rozpouštědle (obvykle kapalině).
Když zamícháte lžíci cukru do sklenice s vodou, vytvoříte roztok. Tento typ kapalného roztoku se skládá z pevné rozpuštěné látky, kterou je cukr, a kapalného rozpouštědla, kterým je voda. Jak se molekuly cukru rovnoměrně rozprostírají ve vodě, cukr se rozpouští.
Mícháním kapaliny v plynu vzniká jiný typ roztoku, který se nazývá plynný roztok. Příkladem tohoto typu roztoku je vlhkost. Vlhkost je voda (kapalina) rozpuštěná ve vzduchu (plyn).
Přemýšlejte o tom, jak se rozpouští kostka cukru ve vodě ve srovnání s balíčkem sypkého cukru. Kostka se rozpouští pomaleji, protože zpočátku je v kontaktu s vodou méně molekul cukru.
V pevném roztoku, jako je stříbro, se měď zahřátá na vysokou teplotu mísí se stříbrem, které bylo rovněž zahřáto, dokud se nerozpustí. Měď je rozpouštědlo, což je látka, která se rozpustí v rozpouštědle. Stříbro je rozpouštědlo.
Typ roztoku je určen látkovým stavem rozpouštědla. Pokud je látka, která provádí rozpouštění, kapalná, nazývá se roztok kapalným roztokem. Pokud je rozpouštědlem plyn, nazývá se roztok plynný roztok. A hádáte správně:
Velikost krystalků soli a cukru si můžete prohlédnout pod mikroskopem nebo lupou, která vám umožní vidět i jejich tvar. Pokud to, co vidíte, nakreslíte tužkou, abyste mohli znázornit stínování, můžete ilustraci zahrnout jako součást závěrečné expozice svého vědeckého projektu.
Existuje několik faktorů, které obecně zvyšují množství rozpuštěné látky. Chcete-li například rozpustit více cukru ve stejném množství vody, můžete vodu zahřát. Také byste mohli cukr rozemlít na menší částice, abyste zvětšili jeho povrch, nebo byste mohli směs promíchat.
Za ta léta, co používáte sůl a cukr na potraviny, jste si pravděpodobně všimli, že každý kousek soli?který je vlastně krystalem, je o něco menší než každý kousek cukru, který je také krystalem.
Molekula jsou dva nebo více prvků, které jsou chemicky spojeny. Molekula soli obsahuje sodík a chlor, které jsou chemicky spojeny a tvoří chlorid sodný. Chemický vzorec této soli je NaCl. Molekula cukru obsahuje uhlík, vodík a kyslík. Chemický vzorec cukru je C12H22O11.
Problém, který se budete snažit v tomto experimentu vyřešit, je, zda se po smíchání s různými kapalinami rozpouští rychleji cukr nebo sůl. Má velikost kousků vliv na to, jak rychle se smíchají s kapalinou?
Když rozpustíte cukr nebo sůl v kapalině?řekněme ve vodě?“, stane se to, že se molekuly cukru přesunou tak, aby se vešly mezi molekuly vody ve sklenici nebo kádince. Následující obrázek ukazuje, jak jsou jednotlivé molekuly v nádobě uspořádány.
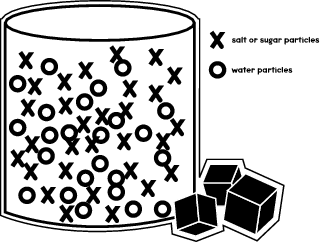
V experimentu uvidíte, jak se molekuly soli a cukru pohybují v různých kapalinách a rozpouštějí se různou rychlostí.
Název této části, ?Sůl nebo cukr: který se rozpouští rychleji v různých kapalinách?? by mohl sloužit jako název vašeho projektu, pokud chcete. Můžete také zvážit jeden z následujících názvů vašeho projektu:
- Velká soutěž v rozpouštění soli a cukru
- Pomocí soli a cukru zkoumáme, jak se látky rozpouštějí
Jakýkoli název si zvolíte, je v pořádku. Pojďme se nyní na chvíli zamyslet nad tím, proč je tento projekt hodnotným využitím vašeho času.
O co jde?“
Když je mezi molekulami rozpouštědla dostatek prostoru, říká se, že rozpouštědlo je nenasycené. Pokud je v rozpouštědle rozpuštěno velké množství rozpuštěné látky, ale mezi molekulami je stále ještě prostor, jedná se o koncentrovaný roztok. Když se v rozpouštědle nemůže rozpustit absolutně žádný další rozpouštědlo, je roztok nasycený.
A když se přebytečné množství rozpouštědla rozpustilo zahřátím roztoku, říká se, že je roztok přesycený.
Smyslem tohoto pokusu je kromě poznání, zda se v různých kapalinách rozpouští rychleji sůl nebo cukr, také naučit se, jak se molekuly v roztoku vzájemně ovlivňují.
Jak jste viděli na předchozím obrázku, molekuly vody zabírají většinu prostoru v nádobě. Stále však zůstává volný prostor, do kterého se mohou vejít molekuly cukru nebo soli. Prostřednictvím experimentu zjistíte, jak rychle se do těchto prostorů vejdou molekuly cukru ve srovnání s částicemi soli.
Znalost této skutečnosti vám pomůže lépe pochopit proces, který probíhá při rozpouštění látky.
Kontrolou ve vašem experimentu bude voda. Ostatní kapaliny, ve kterých budete rozpouštět sůl a cukr, budou proměnnými.
| Kontroly: | Rozpouštědlo? voda |
| Rozpuštěné látky?cukr, sůl | |
| Proměnné: | Pět různých čirých kapalin (mohou být barevné) |
Při provádění pokusu pamatujte, že je velmi důležité, aby všechny použité kapaliny měly stejnou teplotu. Již jste se naučili, že cukr se rozpouští rychleji v teplé kapalině než v chladné, takže víte, že by to nebyl přesný pokus, kdyby některé z kapalin, které použijete, byly teplé a některé studené. Teplota kapaliny by se stala proměnnou.
Všechny kapaliny, které použijete, včetně vody, by tedy měly mít pokojovou teplotu. Pokud je běžně uchováváte v chladničce, nezapomeňte je nechat přes noc stát na pultu, dokud nebudou mít všechny stejnou teplotu.
Abyste měli při provádění pokusu trochu větší flexibilitu, můžete si vybrat kapaliny, ve kterých budete rozpouštět cukr a sůl. Nemá smysl chodit kupovat další kapaliny, když už máte, co potřebujete.
Nepředpokládejte, že kapaliny, které stály v různých částech domu, mají stejnou teplotu. Například láhev sodovky, která ležela v garáži, může být o několik stupňů chladnější než líh ze skříně v koupelně nebo jablečný džus z kuchyňské spíže. Ujistěte se, že jsou všechny tekutiny na stejném místě, aby dosáhly stejné pokojové teploty. If you don’t, the results of your experiment won’t be valid.
Just make sure you choose liquids that are different from each other in taste, color, odor, and purpose. You’ll also need to select those that allow you to observe the salt and sugar as it dissolves. If you use milk or orange juice, for example, you won’t be able to watch the salt and sugar dissolve. Some suggestions for liquids to consider are:
- White vinegar
- Club soda
- Ginger ale
- Glass cleaner (such as Windex)
- Lemonade
- Tea or iced tea (each at room temperature)
- Apple juice
- Rubbing alcohol
All of these are commonly found around the house, perhaps saving you a trip to the store.
What Do You Think Will Happen?
Teď, když víte, jak vznikají roztoky, a znáte některé faktory, které ovlivňují rychlost rozpouštění cukru a soli, které budete používat, měli byste být schopni odhadnout, který z nich se rozpustí rychleji.
Pokud jste tento pokus ještě nedělali, nebudete vědět, zda budou použité kapaliny ovlivňovat rozpouštění soli a cukru. To ztěžuje tvorbu hypotézy, ale nemějte obavy. To, zda se vaše hypotéza ukáže jako správná, nebo ne, nemá vliv na platnost nebo výsledek vašeho experimentu.
Ačkoli až do ukončení experimentu nebudete vědět, zda vlastnosti různých kapalin, které jste zvolili, ovlivní rychlost rozpouštění soli a cukru, víte, že krystalky soli jsou obecně menší než krystalky cukru. A víte, že teplota kapalin nebude ve vašem pokusu hrát roli.
Snažte se využít své dosavadní zkušenosti, informace, které jste si přečetli dříve v této části, a zdravý rozum, abyste vytvořili správnou hypotézu.
Pamatujte, že vaše hypotéza musí být formulována jako objektivní věta, nikoli jako otázka. Takže se pusťte do tipování, zda se rychleji rozpustí sůl nebo cukr, a začněme s experimentem.
Materiál, který budete pro tento projekt potřebovat
Některé tekutiny navrhované pro použití v tomto experimentu jsou bílý ocet, sodovka, zázvorové pivo, čistič skla, alkohol, jablečná šťáva, limonáda a čaj. Pokud chcete jednu nebo více navržených tekutin nahradit jinou, je to v pořádku. Jen se ujistěte, že všechny kapaliny jsou čiré a mají pokojovou teplotu.
Množství níže uvedených materiálů stačí na to, abyste experiment provedli třikrát s každou kapalinou. You’ll need:
- 12 clear, plastic cups (10 ounce )
- One permanent marker
- One (1 teaspoon) (5.0 ml) measuring spoon
- One (12 teaspoon) (2.5 ml) measuring spoon
- One (1 cup) (240 ml) measuring cup
- 8 teaspoons (40 ml) salt, divided in 16 (12 teaspoon) portions
- 8 teaspoons (40 ml) sugar, divided in 16 (12 teaspoon) portions
- 48 ounces (1,440 ml) water at room temperature
- 24 ounces (720 ml) each of five different, clear liquids, all at room temperature
- One clock or watch with a second hand
- One clear plastic cup containing eight fluid ounces (240 ml) water at room temperature
Remember to make sure that all liquids are at room temperature.
Conducting Your Experiment
When you’ve gathered all your materials, you’ll be ready to begin your experiment. Stačí postupovat podle následujících kroků:
Mějte na očích hrnek s čistou vodou, abyste ji mohli porovnat s hrnky obsahujícími sůl a cukr. Bude zajímavé sledovat, jak se bude měnit vzhled kapalin při rozpouštění soli a cukru.
Chvíli potrvá, než se cukr a sůl rozpustí. Pro dosažení nejlepších výsledků roztoky nemíchejte, protože to představuje další proměnnou. Pokud musíte míchat, pak každý roztok třikrát promíchejte a přestaňte. Míchejte až poté, co zjistíte, že na dně obou nádob je roztok. Nerovnoměrné míchání roztoků způsobí, že váš pokus bude neplatný.
- Permanentním fixem napište na šest plastových kelímků ? „sůl“ a na dalších šest ? „cukr“.
- Do každého ze šesti kelímků s nápisem ? „sůl“ dejte 1/2 čajové lžičky (2,5 ml) soli.
- Do každého ze šesti kelímků s nápisem ? „cukr“ vložte 1/2 čajové lžičky (2,5 ml) cukru.
- Do jednoho šálku se solí a jednoho šálku s cukrem přidejte 8 uncí (240 ml) vody. Okamžitě zaznamenejte čas, kdy byla voda přidána, do datového grafu podobného tomu, který je uveden v následující části „Sledování vašeho experimentu“.
- Pozorujte rozpouštění rozpuštěných látek (soli a cukru) v rozpouštědle (vodě). Zaznamenejte do datového grafu čas, kdy se vám zdá, že se jednotlivé rozpuštěné látky zcela rozpustily. Tyto časy pravděpodobně nebudou stejné.
- Vypočítejte uplynulý čas, během kterého došlo k rozpouštění. Vezměte čas, kdy byla do kelímků přidána voda a začalo rozpouštění, a odečtěte jej od času, kdy rozpouštění skončilo. Tím získáte celkový počet minut, za které se sůl a cukr v tekutině zcela rozpustily.
- Opakujte kroky 4 až 6, přičemž místo vody použijte vždy jinou kapalinu.
- Každý z 12 šálků umyjte, opláchněte a důkladně osušte.
- Opakujte kroky 2 až 8 ještě dvakrát, celkem tedy tři pokusy pro každou ze šesti tekutin.
- Vypočítejte průměrnou dobu rozpouštění soli a cukru v každé ze šesti tekutin.
Pamatujte, že pro zjištění průměrné doby rozpouštění soli a cukru v každé kapalině sečtete tři časy zaznamenané pro každou z nich a pak je vydělíte třemi. Číslo, které získáte po vydělení časů, je průměrný čas.
Sledování pokusu
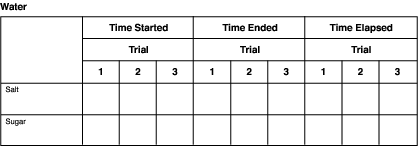
K zaznamenání informací pro jednotlivá rozpouštědla lze použít grafy, jako je následující. Stačí změnit názvy rozpouštědel v záhlaví.
Ujistěte se, že časy zaznamenáváte průběžně. Nespoléhejte se na to, že si je později zapíšete. Než pokus dokončíte, budete mít spoustu čísel.
Spojení všeho dohromady
Co jste si všimli na rychlosti rozpouštění soli a cukru? Prokázali jste správnost své hypotézy? Nebo nesprávnou? Mohli jste při přidávání soli a cukru do různých kapalin zjistit nějaký typ vzorce? Bylo zřejmé, že se sůl v některých tekutinách rozpouštěla lépe a rychleji než cukr? Napadají vás nějaké důvody, proč k tomu mohlo dojít?
Myslíte si, že chemická povaha rozpuštěné látky a rozpouštědla ovlivnila rychlost rozpouštění? K zodpovězení těchto otázek využijte informace, které jste získali při zkoumání svého tématu.
Čím více budete o svém projektu vědět, tím lépe budete schopni správně analyzovat data a dojít ke správnému závěru.
Další zkoumání
Jak již bylo zmíněno, faktory ovlivňující rozpustnost pevných roztoků jsou následující:
- Zvýšení nebo snížení teploty rozpouštědla
- Zvětšení povrchu rozpuštěné látky
- Míchání
Pokud byste chtěli tento projekt posunout o krok nebo dva dále, mohli byste navrhnout experiment, který by testoval jeden?nebo možná všechny tyto proměnné.
Mohli byste snadno porovnat rychlost rozpouštění kostek cukru v kapalině s rychlostí rozpouštění granulovaného cukru.
Nebo byste mohli použít stejnou rozpuštěnou látku?řekněme cukr?a vyzkoušet, zda míchání roztoku způsobuje jeho rychlejší rozpouštění. Zahřívání a ochlazování rozpouštědla při přidávání stejného rozpuštěného roztoku by také bylo možností pro další experimentování.
Pokud jste zvídaví a ochotní experimentovat, pravděpodobně vás napadne mnoho variant tohoto projektu. A protože experiment vyžaduje pouze běžné a levné materiály, měli byste být schopni experimentovat do sytosti.
Ukázka z knihy The Complete Idiot’s Guide to Science Fair Projects 2003 od Nancy K. O’Leary a Susan Shelly. Všechna práva vyhrazena, včetně práva na reprodukci vcelku nebo po částech v jakékoli formě. Použito po dohodě s Alpha Books, členem Penguin Group (USA) Inc.
Chcete-li si tuto knihu objednat přímo u vydavatele, navštivte webové stránky Penguin USA nebo volejte 1-800-253-6476. Tuto knihu můžete také zakoupit na stránkách Amazon.com a Barnes & Noble.