A JAK2 gén V617F mutációjának meghatározása krónikus myeloproliferatív szindrómákban hazánkban: egy esetleírás
A JAK2 gén V617F mutációjának meghatározása krónikus myeloproliferatív szindrómákban hazánkban: egy esetleírás
Drs. Daniela Lens*, Pablo Muxi†, Lics. Andreína Brugnini‡,
Natalia Trías‡, Dra. Silvia Pierri§
Hospital de Clínicas. Általános Orvostudományi Kar.
Köztársasági Egyetem. Montevideo, Uruguay
Abstract
A polycythemia vera (PV), az esszenciális trombocitémia (ET) és az idiopátiás myelofibrózis (IM) egymással szoros kapcsolatban álló, klonális myeloproliferatív betegségek, amelyeket egy vagy több myeloid vonal, például az eritrociták, vérlemezkék és fibroblasztok túlzott proliferációja jellemez a csontvelőben.
Míg szigorú kritériumok léteznek e myeloproliferatív szindrómák diagnosztizálására, a pontos kategorizálás továbbra is vita tárgyát képezi, ráadásul ezeket a rendellenességeket sok esetben nehéz megkülönböztetni a reaktív folyamatoktól.
A közelmúltban, 2005-ben a Janus kináz 2 (JAK2) tirozin-kináz gén mutációját azonosították több ilyen betegségben. Ez a mutáció az 1849-es pozícióban egy G helyett egy T-t tartalmaz, ami a fehérjében egy fenilalanin helyett egy valin helyettesítését eredményezi (JAK2 V617F).
A mutáció előfordulását a PV-es esetek mintegy 90%-ában és az IM-es és ET-es esetek mintegy 50%-ában figyelték meg.
Ebben a közleményben ismertetjük e mutáció kimutatását egy olyan betegnél, akinél valószínűsíthetően PV-t diagnosztizáltak, a mutáció kimutatására szolgáló, rendkívül érzékeny allélspecifikus polimeráz láncreakció (PCR) segítségével, és megvitatjuk e nemrégiben felfedezett mutáció jelentőségét a BCR-ABL-negatív myeloproliferatív szindrómák diagnózisában és kezelésében.
Key words: MYELOPROLIFERATIVE DISORDERS – diagnosis.
MUTATION – genetika.
PROTEIN-TYROSINE KINASE.
* Associate Professor. Általános Orvostudományi Tanszék.
† docens. Hematológiai Klinika. Klinikai Orvostudományi Tanszék.
‡ Biokémia Lic. Asszisztens. Általános Orvostudományi Tanszék.
§ docens. Hematológiai Klinika. Klinikai Orvosi Osztály.
Korrespondencia: Dr. Daniela Lens.
Megosztás. Alapvető orvostudomány. Hospital de Clínicas. Piso 15. Avda Italia s/n. Montevideo CP 11600. Montevideo, Uruguay.
Email: [email protected]
Beérkezett: 2006.7.31.
Elfogadva: 2007.2.26.
Bevezetés
A krónikus myeloid leukémiával ellentétben, ahol a specifikus BCR-ABL átrendeződés azonosítása áttörést hozott a diagnózis, a megfigyelés és a kezelés terén, a BCR-ABL-negatív krónikus myeloproliferatív szindrómákban (PMS), mint például a polycythemia vera (PV), az esszenciális trombocitémia (ET) és az idiopátiás myelofibrózis (IM), egészen a közelmúltig nem ismertek specifikus genetikai elváltozásokat.
2005 májusa és júniusa között öt kutatócsoport írt le egy új pontmutációt a JAK2 tirozinkináz génben, amely a 14. exon 1849-es nukleotidjánál egy guanin timinre cserélődik, ami a fehérje 617-es pozíciójában egy valin fenilalaninra cserélődését eredményezi, és amelyről a JAK2 mutáció a V617F(1-5) nevet kapta.
Ezt a mutációt a PV-esetek mintegy 90%-ában figyelték meg, ha nagy érzékenységű teszteket használnak a kimutatására(6). Az IM és ET esetek körülbelül 50%-ában is megtalálható volt, míg egészséges személyeknél vagy másodlagos eritrocitózisban szenvedő betegeknél nem találták meg, így ez a mutáció nagyon nagy prediktív értékkel bír az SMPC és a nem klónikus állapotok, például a másodlagos policitémia megkülönböztetésében.
Ez a mutáció a JAK2 jelátvitelt negatívan szabályozó autoinhibitoros domén egy magasan konzervált régiójában fordul elő. Számos tanulmány kimutatta, hogy ez a mutáció részt vesz ezeknek a betegségeknek a patogenezisében, különösen a JAK2 gén funkciójának erősödése és a kontroll elvesztése révén, amely e rendellenességek túlzott myeloproliferációjával jár együtt.
Ebben a közleményben ismertetjük e mutáció kimutatását egy olyan betegnél, akinél valószínűsíthetően PV-t diagnosztizáltak, és megvitatjuk ennek az új mutációnak a jelentőségét a BCR-ABL-negatív SMP-k diagnózisában és kezelésében.
Anyag és módszer
Deoxiribonukleinsav extrakció
Genomi deoxiribonukleinsav (DNS) extrakciót végeztünk 1 ml citrátos perifériás vérből, a kereskedelmi forgalomban kapható dnazol (Life Techno-logies) reagenssel, a gyártó által megadott protokollt követve. A DNS-mintákat 4°C-on tároltuk.
A Vl617F mutáció kimutatása
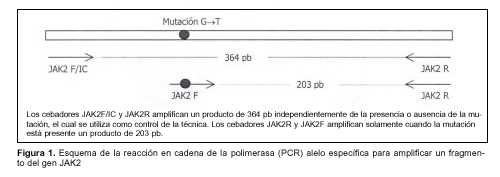
A V617F mutációt korábban nyert genomi DNS-ből mutattuk ki allélspecifikus polimeráz láncreakcióval (PCR) a Baxter és munkatársai által közzétett módszer szerint(1). Ezt a PCR-t három különböző primer, a JAK2R, a JAK2F/IC és a JAK2F (1. táblázat) használatára tervezték. A JAK2F primer specifikus a mutáns allélra, a JAK2F/IC primer pedig minden egyénben megtalálható, függetlenül a mutáció jelenlététől vagy hiányától, így a reakció belső kontrollját képezi. Így a JAK2F/IC és a JAK2R primerekkel 364 bázispár (bp) méretű termék amplifikálódik minden egyénnél, és csak a vizsgált mutációval rendelkező egyéneknél kapunk 203 bp méretű terméket a JAK2F és a JAK2R primerekkel (1. ábra).
A PCR-amplifikációt 20 uL végső térfogatban végeztük 500 ng DNS, 200 mM/L dNTP-k, 0,5 U Taq-polimeráz (New England Biolabs) és 2 uL 10x Taq-puffer felhasználásával, amely 2 mM MgCl-t (New England Biolabs), 0,5 mM JAK2 F és JAK2 F/IC primert és 1 mM JAK2 R primert tartalmazott.
A használt PCR-program 36 ciklusból áll, amely 5 perces denaturálással kezdődik, majd ciklikusan: 30 másodperc 94°C-on, 30 másodperc 58°C-on és 30 másodperc 72°C-on, végül 5 perces hosszabbítással zárul. Minden reakcióban szerepelt egy negatív kontroll, amely az amplifikációhoz szükséges összes reagenssel rendelkezett, és amelyben a DNS-templát vízzel helyettesítették. A várt PCR-termék ellenőrzését etídium-bromiddal festett 2%-os agarózgélen végeztük(7).

Az eset elemzése
Férfi beteg, 72 éves, erős dohányos, kezelt krónikus artériás hipertónia és krónikus obstruktív arteriopátia hordozója, aki 2002-ben a bal láb ötödik lábujjának amputációját határozta meg. 2004 decemberében, amikor a bal alsó végtagot érintő új obstruktív epizódot mutatott ki, a hemográfia a vörösvértestek számának emelkedését mutatta 66%-os hematokrit mellett, 24 000-es granulocitózissal és 245 000-es trombocitaszámmal. A hematokrit nem változott, a vérlemezkeszám pedig fokozatosan 710 000-re emelkedett. A csontvelőbiopsziás vizsgálatban hipercelluláris csontvelőt figyeltek meg az eritroidsorozat hiperpláziájával, ami a PV-típusú krónikus myeloproliferatív szindrómára engedett következtetni.
A beteget flebotómiával kezelték, és 2005 májusában megkezdték a hydroxyurea-kezelést, amelyet 2006 februárjában egy vérzéses szövődmény miatt abbahagytak.
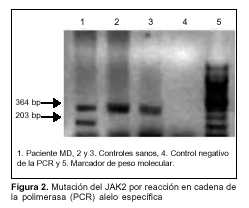
Amint a 2. ábrán látható, a betegnél a JAK2 gén V617F mutációjának allélspecifikus PCR-vizsgálata során két sávos mintázatot mutatott. Egyrészt a 364 bp-os kontrollsáv, amely a két vizsgált egészséges kontrollban is jelen van. Másrészt egy 203 bp-os termék is amplifikálódott a betegben, amely a mutáció jelenlétét mutatta. Ez a sáv nem volt megfigyelhető az egészséges kontrolloknál.
Megbeszélés és következtetések
Munkánkban leírtuk az első olyan esetet, amelyben hazánkban a JAK2 gén V617-es mutációját azonosították. Ez a munka egy multidiszciplináris projekt része, amely az Általános Orvostudományi Tanszék és a Hospital de Clínicas Hematológiai Szolgálata között zajlik, és amelynek célja e mutáció jelenlétének meghatározása 100 BCR-ABL-negatív PMS-ben szenvedő betegnél.
A JAK2 gén aktiváló V617F mutációjának közelmúltbeli azonosítása fontos előrelépést jelent a BCR-ABL-negatív myeloproliferatív szindrómák patogenezisének megismerésében. Mivel ez a mutáció nagy gyakorisággal fordul elő a PV-ben és kisebb mértékben az ET-ben és az IM-ben, feltételezték, hogy e mutáció kimutatása nagy hatással lenne ezen entitások diagnózisára, osztályozására és kezelésére. Különböző csoportok javasolták e mutáció kimutatásának első vonalbeli diagnosztikai tesztként való alkalmazását 51%-nál nagyobb hematokrit esetén vagy PV gyanúja esetén, mivel a JAK2 V617F kimutatásának 100%-os pozitív prediktív értéke van a PV diagnózisára(8,9). Másrészt több szerző azt állította, hogy e mutáció jelenléte lehetővé tenné a PMS új osztályozását, mivel a JAK2 mutációt hordozó ET, PV és MI ugyanazt a betegséget képviselhetné különböző evolúciós stádiumokban, nem pedig különböző entitásokat(10-12). A mutáció kimutatásának pontos klinikai értékét és előnyét azonban még meg kell állapítani, és e kérdések eldöntéséhez speciálisan tervezett prospektív klinikai vizsgálatokra van szükség.
Ezeken túlmenően, a mutáció felfedezése új távlatokat nyit a kifejezetten a mutáns fehérje kinázt célzó terápiák számára, hasonlóan a krónikus myeloid leukémiákban alkalmazott BCR-ABL-gátlókhoz.
Összefoglaló
A policithemia vera (PV), az esszenciális trombocitémia (ET-TE) és az idiopátiás myelofibrózis (IM-MI) klonális myeloproliferatív rendellenességek, amelyeket egy vagy több myeloid vonal, például az eritrociták, a vérlemezkék és a csontvelői fibroblasztok túlzott proliferációja jellemez.
A myeloproliferatív szindrómák pontos kategorizálása még akkor is vita tárgyát képezi, ha a diagnosztikus kritériumok szigorúak; ráadásul ezeket a rendellenességeket nehéz megkülönböztetni a reaktív folyamatoktól.
A közelmúltban, 2005-ben a JAK2-mutációt számos ilyen entitásban azonosították. A JAK2 kódoló régiójának szekvenálása egy G-T transzverziót mutatott ki az 1849-es pozícióban, amely egy valint fenilalaninra cserélt (JAK2 V617F).
A V617F-JAK2-mutáció előfordulása közel 90% volt a PV-s betegeknél, és 50% az IM-es és ET-s betegeknél.
A jelen tanulmányban a V617F-JAK2-mutáció kimutatását ismertetjük egy PV-gyanús betegnél allélspecifikus polimeráz láncreakció analízis (PCR) segítségével, és tárgyaljuk a mutáció jelentőségét a negatív BCR-ABL myeloproliferatív szindrómák diagnózisában és kezelésében.
Résumé
La polycytémie vera (PV), Az esszenciális trombocitémia (ET) és az idiopátiás myelofibrózis (IM) szorosan összefüggő klonális myeloproliferatív rendellenességek, amelyeket egy vagy több myeloid vonal, például az eritrociták, a vérlemezkék és a csontvelő fibroblasztok túlzott proliferációja jellemez.
Noha szigorú kritériumok vannak e myeloproliferatív szindrómák diagnózisára, a pontos kategorizálás továbbra is vita tárgyát képezi, ráadásul ezeket a rendellenességeket számos esetben nehéz megkülönböztetni a reaktív folyamatoktól.
A közelmúltban, 2005-ben a Janus kináz 2 (JAK2) tirozinkináz gén mutációját azonosították több ilyen betegségben. Ez a mutáció az 1849-es pozícióban egy G helyett egy T-t tartalmaz, ami a fehérjében egy fenilalanin valinra történő cseréjét eredményezi (JAK2 V617F).
A mutáció előfordulását a PV-es esetek közel 90%-ában, valamint az MI és TE-es esetek mintegy 50%-ában figyelték meg.
Ezzel a munkával leírjuk ennek a mutációnak a kimutatását egy valószínűsíthetően PV diagnózisú betegnél egy allélspecifikus polimeráz láncreakció (PCR) segítségével, amely nagy érzékenységgel rendelkezik a mutáció kimutatására, és megvitatjuk ennek az újonnan felfedezett mutációnak a jelentőségét a BCR-ABL-negatív myeloproliferatív szindrómák.
Resumo
A Policitemia Vera (PV), a trombocitemia hemorrágica (TE) és a mielofibrose idiopática (MI) são transtornos mieloproliferativos clonais fortemente relacionados e caracterizados por uma proliferação excessiva de uma ou mais línhas mielóides tais como eritrócitos, platequetas e fibroblastos da medula óssea.
Embora existam critérios rigorososos para o diagnóstico destas síndromes mieloproliferativas, a classificação precisa continua sendo discutida; ademais muitas vezes é muito difícil diferenciar estes distúrbios de processos reativos.
2005-ben a Janus kináz 2 (JAK2) tirozinkináz gén mutációját azonosították több ilyen betegségben. Ebben a mutációban az 1849-es pozícióban G-ről T-re történő szubsztitúció figyelhető meg, ami a fehérjében fenilalaninról valinra történő szubsztitúcióhoz vezet (JAK2 V617F).
Ez a mutáció a PV-es esetek körülbelül 90%-ában, valamint az MI és TE-es esetek körülbelül 50%-ában volt megfigyelhető.
Ezzel a cikkel leírjuk e mutáció kimutatását egy olyan betegnél, akinél valószínűleg PV-t diagnosztizáltak, a mutáció kimutatására szolgáló, rendkívül érzékeny allélspecifikus polimeráz láncreakció (PCR) segítségével, és megvitatjuk ennek az újonnan felfedezett mutációnak a jelentőségét a BCR-ABL-negatív myeloproliferatív szindrómák diagnózisában és kezelésében.
Bibliográfia
1. Baxter EJ, Scott LM, Campbell PJ, East C, Fourouclas N, Swanton S, et al. Acquired mutation of the tyrosine kinase JAK2 in human myeloproliferative disorders. Lancet 2005; 365: 1054-61.
2. James C, Ugo V, Le Couedic JP, Staerk J, Delhommeau F, Layout C, et al. A JAK2 egyedi klonális mutációja, amely konstitutív jelátvitelhez vezet, polycythaemia verát okoz. Nature 2005; 434: 1144-8.
3. Kralovics R, Passamonti F, Buser AS, Teo SS, Tiedt R, Passweg JR, et al. A JAK2-ben található gain of function mutáció gyakran fordul elő myeloproliferatív betegségekben szenvedő betegekben. N Engl J Med 2005; 352: 1779-90.
4. Levine RL, Waldleigh M, Cools J, Ebert BL, Werning G, Huntly BJ, et al. Aktiváló mutáció a tirozinkináz JAK2-ben polycythaemia vera, esszenciális trombocitémia és myeloid metaplasia myelofibrózissal. Cancer Cell 2005; 7: 387-97.
6. Vainshenker W, Constantinescu SN. A JAK2 egy egyedülálló aktivációs mutációja (V617F) áll a Polycythemia Vera hátterében, és lehetővé teszi a myeloproliferatív betegségek új osztályozását. Hematology Am Soc Hematol Educ Program 2005; 195-200.
7. Sambrook J, Russell DW. Molekuláris klónozás: laboratóriumi kézikönyv. 3 ed. New York: Cold Spring Harbor Laboratory, 2001.
8. Tefferi A, Pardanani A. A JAK2V617F mutációs szűrése: mikor rendeljük meg a vizsgálatot és hogyan értelmezzük az eredményeket. Leuk Res 2006; 30(6): 739-44.
9. James C, Delhommeau F, Marzac C, Teyssandier I, Couedic JP, Giraudier S, et al. A JAK2 V617F kimutatása mint az erythrocytosis első szándékú diagnosztikai tesztje. Leukémia 2006; 20: 350-3.
10. Campbell PJ, Scott LM, Buck G, Wheatley K, East CL, Marsden JT, et al. Az esszenciális trombocitémia altípusainak meghatározása és kapcsolata a polycythaemia verával a JAK2 V617F mutációs státusz alapján: prospektív vizsgálat. Lancet 2005; 366: 1945-53.
11. Antonioli E, Guglielmelli P, Pancrazzi A, Bogani C, Verrucci M, Ponziani V, et al. Clinical implications of the JAK2 V617F mutation in essential thrombocythemia. Leukémia 2005; 19: 1847-9.