Légzési elégtelenség – típusai és kezelése
Kép : “CPR training-03” by Rama. Licenc: CC BY-SA 2.0
A légzési elégtelenség definíciója
A légzési elégtelenség a gázcsere meghibásodását jelenti, azaz az artériás oxigénfeszültség, a PaO2 60 mm Hg alatti csökkenését (hipoxémia). Kísérheti vagy nem kísérheti hiperkapnia, azaz 50 mm Hg-nál magasabb PaCO2 (csökkent CO2-elimináció).
A légzés normális élettana
Normális egyéneknél az “alveoláris” oxigénfeszültség PAO2 közel 100 mmHg, míg az alveoláris szén-dioxid feszültség PACO2 40 mmHg közelében marad.
Az “alveoláris (A)” és az “artériás (a)” oxigénfeszültség között kis, 5-10 mmHg-os különbség van, mivel a szisztémás szívteljesítmény mintegy 2%-a megkerüli a tüdőkeringést (fiziológiás sönt), és nem oxigenizálódik.
A kis mennyiségű oxigénmentes vér keveredése miatt az artériás vér PO2-je (PaO2) kissé alacsonyabb, mint az alveoláris levegőé (PAO2). A normális A-a gradiens körülbelül < 10 mmHg. Ha az A-a gradiens normális, az azt jelenti, hogy nincs hiba a gázok diffúziójában. Az A-a gradiens segít körvonalazni a légzési elégtelenség különböző okait.
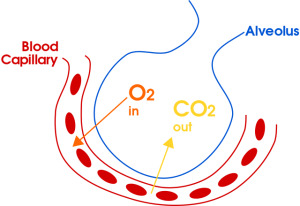
Kép: “Gas exchange in the alveolus” by domdomegg. Licenc: CC-BY 4.0
Állandó állapotban a szén-dioxid-termelés sebessége a szervezetben állandó. A PACO2 a ventilációtól függ és azzal “fordítottan arányos”, tehát a megnövekedett ventiláció csökkent PACO2-t, a csökkent ventiláció pedig megnövekedett PACO2-t eredményez.
Az alveoláris oxigénfeszültség, a PAO2, a belélegzett oxigén koncentrációjától (FIO2) és az alveoláris szén-dioxid feszültségtől (PACO2) függ, a következő egyenlet szerint:
PAO2 = FIO2 × (PB – PH2 O) – PACO2/R
PAO2: Alveoláris PO2 FIO2: Az oxigén frakcionált koncentrációja a belélegzett gázban
PB: Barometrikus nyomás PH2O: vízgőznyomás 37°C-on
PACO2: Alveoláris PCO2 R: Légzési cserearány.
A légzési elégtelenség típusai
A légzési elégtelenségnek két típusa van, amelyeket az artériás vérgázok (ABG) elemzése alapján osztályoznak:
Az I. típusra jellemző:
- Hypoxémia (PaO2 kevesebb, mint 60 mmHg)
- Hyperkapnia nélkül, normál vagy alacsony PaCO2 (PaCO2 kevesebb, mint 50 mmHg)
- Általában jelentős ventiláció-perfúzió eltérés miatt következik be
A II. típust a következők jellemzik:
- Hypoxaemia (PaO2 kevesebb, mint 60 mmHg) és
- Fokozott hypercapnia (PaCO2 több, mint 50 mmHg)
- Általában hypoventiláció miatt fordul elő
A légzési elégtelenség tovább osztályozható akut vagy krónikus kezdetűnek.
Az akut légzési elégtelenség perceken és órákon belül jelentkezik, és általában sürgősségi eset. Az artériás vérgázok és a szervezet sav-bázis állapotának életveszélyes változásai jellemzik, pl. tenziós pneumothorax, tüdőembólia, akut légzési distressz szindróma, anafilaxiás reakciók.
A krónikus légzési elégtelenség hetek és hónapok alatt fokozatosan alakul ki. Kevésbé drámai és nem mindig nyilvánvaló. A vesék általában kompenzálják és normalizálják a szervezet sav-bázis állapotát a bikarbonát- és savkiválasztás megváltoztatásával. Policitémia, krónikus obstruktív tüdőbetegség és pneumoconiosis is előfordulhat.
A hipoxémia patofiziológiája
A hipoxémia az artériás PO2 csökkenése, míg a hipoxia a szövetek csökkent oxigénellátását jelenti. A betegeknél normális PaO2 mellett is kialakulhat hipoxia, például szén-monoxid-mérgezés vagy csökkent hemoglobinszint (vérszegénység) esetén.
A hipoxémiának és a légzési elégtelenségnek öt fontos patofiziológiai oka van.
Hypoventilláció
A percventiláció a légzési frekvenciától és a légzési térfogattól függ, ami a nyugalmi állapotban minden egyes normál légzés során beszívott levegő mennyisége.
Minute ventiláció = Légzésszám x légzési térfogat
A normál légzésszám körülbelül 12 légzés/perc, a normál légzési térfogat pedig körülbelül 500 ml. Ezért a percenkénti légzési térfogat általában átlagosan körülbelül 6 L/perc.
Hypoventilláció akkor következik be, amikor a légzési frekvencia és/vagy a légzési térfogat csökken, így percenként kisebb mennyiségű levegő cserélődik ki. Ilyenkor csökken az oxigén bejutása az alveolusokba és az artériákba, ami a PaO2 csökkenéséhez vezet. Amint már leírtuk, a PaCO2 fordítottan arányos a ventilációval. Ezért a hipoventilláció megnövekedett PaCO2-t eredményez.
Az alveoláris-artériás gradiens normális és 10 mmHg-nál kisebb lesz, mivel a gázok diffúziójában nincs hiba. Ezekben az esetekben a lélegeztetés és/vagy az oxigénkoncentráció növelése korrigálja a zavart vérgázokat.
Diffúziós károsodás
Diffúziós károsodás esetén a tüdőn belül strukturális probléma áll fenn. Előfordulhat csökkent felület (mint az emphysema esetében), vagy az alveoláris membránok megnövekedett vastagsága (mint a fibrosis és a restriktív tüdőbetegségek esetében), ami rontja a gázok diffúzióját az alveolákon keresztül, ami megnövekedett alveoláris-arteriális gradienshez vezet. Megnövekedett A-a gradiens esetén az alveoláris PO2 normális vagy magasabb, de az artériás PO2 alacsonyabb lesz. Minél nagyobb a strukturális probléma, annál nagyobb lesz az alveoláris-arteriális gradiens.
Mivel a gázok diffúziója egyenesen arányos a gázok koncentrációjával; ezért a belélegzett oxigén koncentrációjának növelése korrigálja a PaO2-t, de a fokozott A-a gradiens mindaddig fennáll, amíg a strukturális probléma fennáll.
Tüdősönt
A pulmonális söntben, más néven jobb-bal söntben a jobb oldalról érkező vénás oxigénmentes vér a szív bal oldalára és a szisztémás keringésbe kerül anélkül, hogy az alveolusokban oxigenizálódna. Egyszerű szavakkal a sönt a “normális perfúzióra, rossz szellőzésre” utal. A tüdő vérellátása normális, de a szellőzés csökkent vagy hiányzik, ami azt eredményezi, hogy a beáramló oxigénmentes vérrel nem történik meg a gázcsere. A ventiláció/perfúzió arány nulla vagy nullához közeli.
Atelektázis esetén például az összeesett tüdő nem szellőzik, és az adott szegmensben lévő vér nem oxigenizálódik. Cianotikus szívbetegségekben a jobb oldali vér megkerüli (sönt) a tüdőt és a bal oldalra kerül, ami hipoxémiát és cianózist okoz.
Az A-a gradiens megnő, ahogy az oxigénmentes vér az artériás (szisztémás) keringésbe kerül, csökkentve az artériás oxigénfeszültséget, a PaO2-t.
Mivel a vénás vér nem oxigenizálódik a tüdősöntőben, ezért az oxigénkoncentráció növelése nem korrigálja a hipoxémiát. A vér megkerüli a tüdőt, függetlenül attól, hogy milyen magas az oxigénkoncentráció. Ez a PaO2-emelkedés elmaradása az oxigén beadása után nagyon fontos szempont, és segít a differenciáldiagnózis felállításában a diffúziós zavar és a hipoxémia más okai között, amelyek kiegészítő oxigénre megszűnnek.
Ventilláció – perfúzió (V/Q) eltérés
V/Q az alveoláris ventilláció (V) és a pulmonális véráramlás (Q) aránya. A ventiláció és a perfúzió összhangja elengedhetetlen az alveolusokon belüli megfelelő oxigén- és szén-dioxid-csere eléréséhez. A V/Q arány normális egyéneknél 0,8 körül van, de ez az arány megváltozik, ha jelentős szellőzési vagy perfúziós hibák állnak fenn.
A tüdőn belül nem minden alveolusban van egységes szellőzés és perfúzió. Ezek a gravitáció hatására hajlamosak változni. A tüdő csúcsán az alveolusok nagyok és teljesen felfújtak, míg a bázisokon kicsik. Hasonlóképpen a tüdő alján nagyobb a vérellátás, mint a csúcson. Ez fiziológiás ventiláció (V) – perfúzió (Q) eltérést eredményez a különböző alveolusok között.
A csökkent V/Q arány (< 0,8) vagy csökkent ventiláció (légúti vagy intersticiális tüdőbetegség) vagy túlperfúzió miatt alakulhat ki. Ezekben az esetekben a vér pazarolódik, mert nem tud megfelelően oxigénnel telítődni. Szélsőséges körülmények között, amikor a szellőzés jelentősen csökken, és a V/Q a nullához közelít, tüdősöntként viselkedik.
A megnövekedett V/Q arány (> 0,8) általában akkor fordul elő, ha a perfúzió csökken (tüdőembólia akadályozza a véráramlást az elzáródás distalis részén) vagy túlszellőzés. Ilyenkor a levegő elpazarolódik, és nem tud a vérben diffundálni. Szélsőséges körülmények között, amikor a perfúzió jelentősen csökken, és a V/Q megközelíti az 1-et, az alveolusok holt térként viselkednek, és nem történik gázdiffúzió.
Ezért a tüdőn belüli ventiláció és perfúzió fokozott eltérése károsítja a gázcsere-folyamatokat, ami végül hipoxémiához és légzési elégtelenséghez vezet.
Nagy magasságban
Nagy magasságban a barometrikus nyomás (PB) csökken, ami az egyenlet szerint az alveoláris PO2 csökkenéséhez vezet:
PAO2 = FIO2 × (PB – PH2 O) – PACO2/R
A csökkent alveoláris PAO2 csökkent artériás PaO2-hez és hipoxémiához vezet, de az A-a gradiens normális marad, mivel a gázcsere-folyamatokban nincs hiba. Ilyen körülmények között a további oxigén (a FIO2 növelése) növeli a PAO2-t és korrigálja a hipoxémiát.
Amikor egy személy hirtelen nagy magasságba emelkedik, a szervezet hiperventillációval reagál a hipoxémiára, ami légzési alkalózist okoz. A 2,3-difoszfogloglicerát (DPG) koncentrációja megnő, ami az oxigén-hemoglobin disszociációs görbét jobbra tolja el.
Krónikusan zajlik az akklimatizáció, és a szervezet a vér oxigénszállító kapacitásának növelésével válaszol (policitémia). A vesék kiválasztják a bikarbonátokat, és a pH-t a normális határokon belül tartják.
| A hipoxémia okai | |||
| Cause | PaO2 | A-a gradient | PaO2 response to supplemental oxygen |
| Hypoventilation | Decreased | Normal | Increases |
| Diffusion Impairment | Decreased | Increased | Increases |
| Shunt | Decreased | Increased | Does not increase. |
| V/Q Mismatch | Decreased | Increased | Usually increases (depends on V/Q mismatch type) |
| High Altitude | Decreased | Normal | Increases |
Pathophysiology of Hypercapnia
Hypercapnia occurs when carbon-dioxide tension (PCO2) increases to more than 50 mmHg. As explained above, at a steady-state, the rate of carbon dioxide production within the body is constant. The PACO2 depends on and is inversely proportional to ventilation, so decreased ventilation will cause increased PACO2 and vice versa. Therefore, hypercapnia (along with hypoxemia, Type II respiratory failure) occurs, usually due to conditions that decrease ventilation.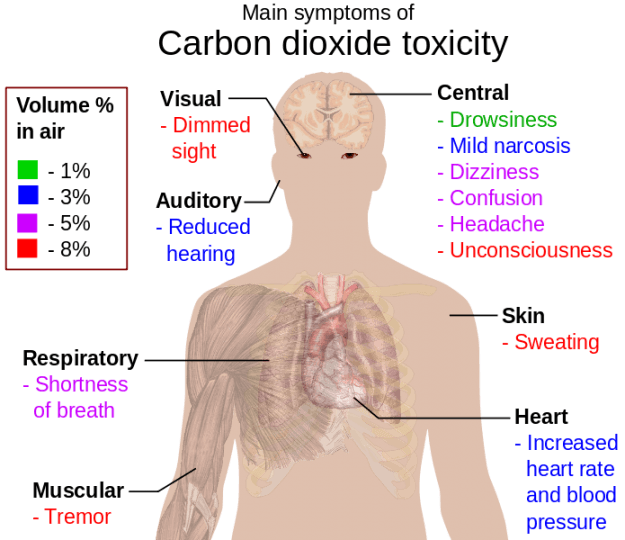
For example:
- Reduced central respiratory drive, e.g.,, opioid-túladagolás vagy fejsérülés
- Felső légúti elzáródás (idegen test, ödéma, fertőzés)
- Késői súlyos akut asztma, COPD
- Perifériás neuromuszkuláris betegségek, pl., Guillain-Barre-szindróma, myasthenia gravis, botulizmus
- Légzőizom-fáradtság
A légzési elégtelenség kezelése
Az akut légzési elégtelenségben szenvedő betegeknél fokozott a hypoxiás szövetkárosodás kockázata, és őket légző/intenzív osztályra kell felvenni. A beteg légútjait, légzését és keringését (ABC) kell először felmérni és kezelni, hasonlóan minden sürgősségi esethez.
Az első cél a hipoxémia korrigálása és/vagy a szöveti hipoxia megelőzése a 60 mm Hg értékű artériás oxigénfeszültség (PaO2) vagy a 90%-nál nagyobb artériás oxigéntelítettség (SaO2) fenntartásával. Általában kezdetben a kiegészítő oxigén biztosítása és a gépi lélegeztetés, amelyet arcmaszkkal (nem invazív) vagy légcsőintubációval biztosítanak, hatékony.
A légzési elégtelenség specifikus kezelése a kiváltó októl függ. Ezért meg kell próbálnunk azonosítani a légzési elégtelenséghez vezető alapvető patofiziológiai zavarokat, és azokat specifikus kezeléssel korrigálni, például COPD és asztma esetén szteroidokkal és hörgőtágítókkal, tüdőgyulladás esetén antibiotikumokkal, tüdőembólia esetén heparinnal.
Mechanikus lélegeztetés céljai
A mechanikus lélegeztetésnek két fő célja van:
- A PaO2 növelése a belélegzett oxigén koncentrációjának (FIO2) és a pozitív kilégzési végnyomásnak (PEEP) a növelésével.
- Decrease PaCO2 by increasing the ventilation by adjusting the tidal volume and respiratory rate of the mechanical ventilators.
Mechanical ventilation is also an appropriate therapy for respiratory muscle fatigue because it rests the respiratory muscles.
Study for medical school and boards with Lecturio.
- USMLE Step 1
- USMLE Step 2
- COMLEX Level 1
- COMLEX Level 2
- ENARM
- NEET