Neutropenia
A neutropenia lehetséges okainak listája nem rövid. A neutropenia etiológiáját koncepcionálisan kétféleképpen, mechanizmus vagy etiológiai kategória szerint tekinthetjük.
A neutropeniát okozó mechanizmusok változatosak és nem teljesen ismertek. Sok esetben a neutropenia egy gyógyszer vagy más anyag hosszan tartó expozíciója után következik be, ami a hipoplasztikus csontvelő csökkent neutrofil termelését eredményezi. Ez közvetlen őssejt-toxikus hatásra utal. Más esetekben ismételt, de időszakos gyógyszer- vagy egyéb expozícióra van szükség. Ez immunmechanizmusra utal, bár ez az elképzelés nem bizonyított. Sok klinikai helyzetben nem ismert a neutropenia kialakulásához kapcsolódó pontos expozíció és annak időtartama.
A neutropenia mechanizmusainak e hiányos ismerete miatt a széles etiológiai kategória szerinti osztályozást egyszerűbb megtartani. Ebben a sémában a neutropenia etiológiája vagy veleszületett (örökletes) vagy szerzettnek minősíthető. Bár ennek a kategorizálásnak korlátozott klinikai diagnosztikai haszna lehet, hasznos lehet a neutropenia örökletes okainak egyértelmű elkülönítése a szerzett okok sokaságától. Az örökletes neutropeniák esetében ezeket a rendellenességeket úgy lehet tovább jellemezni, mint amelyek izolált neutropeniával vagy más, akár immunrendszeri, akár fenotípusos rendellenességekkel társulnak.
Sok örökletes rendellenesség a neutrofil elasztázt kódoló gén, az ELA2 mutációjára vezethető vissza. Több allél is érintett. A leggyakoribb mutációk intronikus szubsztitúciók, amelyek inaktiválnak egy splice-helyet a 4. intronban. Az ELA2-től eltérő gének is érintettek. Az alábbi táblázat felsorol néhány érintett genetikai állapotot; ezek nem gyakori állapotok.
1. táblázat. Genetikai (örökletes) körülmények az agranulocitózisban (A táblázat megnyitása új ablakban)
|
Szindróma |
Inheritance |
Gene |
Clinical Features |
|
Cyclic neutropenia |
Autosomal dominant |
ELA2 |
Alternate 21-day cycling of neutrophils and monocytes |
|
Kostmann syndrome |
Autosomal recessive |
Unknown |
Stable neutropenia, no MDS or AML |
|
Severe congenital neutropenia |
Autosomal dominant |
ELA2 (35-84%) |
Stable neutropenia, MDS or AML |
|
Autosomal dominant |
GFI1 |
Stable neutropenia, circulating myeloid progenitors, lymphopenia |
|
|
Sex linked |
Wasp |
Neutropenic variant of Wiskott-Aldrich syndrome |
|
|
Autosomal dominant |
G-CSFR |
G-CSF–refractory neutropenia, no AML or MDS |
|
|
Hermansky-Pudlak syndrome type 2 |
Autosomal recessive |
AP3B1 |
Severe congenital neutropenia, platelet dense-body defect, oculocutaneous albinism |
|
Chediak-Higashi syndrome |
Autosomal recessive |
LYST |
Neutropenia, oculocutaneous albinism, giant lysosomes, impaired platelet function |
|
Barth syndrome |
Sex linked |
TAZ |
Neutropenia, often cyclic; cardiomyopathy, methylglutaconic aciduria |
|
Cohen syndrome |
Autosomal recessive |
COH1 |
Neutropenia, mental retardation, dysmorphism |
|
Source: Modified from Berliner et al, 2004. AML = acute myeloid leukemia; G-CSF = granulocyte colony-stimulating factor; MDS = myelodysplastic syndrome. |
|||
A szerzett neutropenia okai összetettek, de legtöbbször három fő kategóriához kapcsolódnak: fertőzés, gyógyszerek (közvetlen toxikus vagy immunmediált) és autoimmunitás. A krónikus jóindulatú neutropenia, vagy krónikus idiopátiás neutropenia átfedési zavarnak tűnik az örökletes és a szerzett formákkal, és néha megkülönböztethetetlen. Egyes neutropeniás betegek egyértelmű anamnézist és családi mintát adnak, míg másoknál nincs családi anamnézis, kevés a vérvizsgálati meghatározás, és a neutropenia időtartama ismeretlen. A betegeknek ebben a csoportjában lehet örökletes vagy szerzett neutropenia. A következőkben mind a veleszületett, mind a szerzett neutropeniás rendellenességek rövid összefoglalása következik.
Veleszületett neutropenia társuló immundefektusokkal
A rendellenes immunglobulinokkal járó neutropenia X-kapcsolt agammaglobulinémiában, izolált immunglobulin A (IgA) hiányban, X-kapcsolt hiperimmunoglobulin M (XHIGM) szindrómában és I. típusú dysgammaglobulinémiában szenvedő egyéneknél figyelhető meg. Az XHIGM-ben, amely a CD40 ligandum mutációira vezethető vissza, a betegek IgM-szintje valóban lehet normális vagy emelkedett, de a szérum IgG-szintje jelentősen csökkent. Mindezen rendellenességek esetén a fertőzésveszély magas, és a kezelés intravénás immunglobulin (IVIG).
A retikuláris diszgenezisben szenvedő betegeknél súlyos neutropenia, sejtközvetített immunitás hiánya, agammaglobulinémia és limfopénia figyelhető meg. Életveszélyes fertőzések fordulnak elő, amelyek refrakterek a granulocita kolóniastimuláló faktorra (G-CSF). A csontvelő-transzplantáció a választott kezelés.
Súlyos veleszületett vagy krónikus neutropenia
A súlyos veleszületett neutropenia (SCN) vagy Kostmann-szindróma leggyakrabban recesszív öröklődéssel alakul ki, és távoli, elszigetelt, nagyfokú rokonsági fokú populációkban fordul elő. Autoszomális domináns és sporadikus esetekről is beszámoltak, leggyakrabban a G-CSF receptor mutációi miatt. Ebben a szindrómában nem létezik egységes genetikai hiba. Az ELA2 mutációi, amelyek a ciklikus neutropeniát okozzák (lásd alább), nem elegendőek a Kostmann-szerű SCN fenotípusának magyarázatához.
A betegek 3 hónapos korukig visszatérő bakteriális fertőzésekkel jelentkeznek. A fertőzés leggyakoribb helye a száj és a perirectum. A neutropeniának ez a típusa súlyos, és a kezelés G-CSF. A monoszómia 7-es monoszómiával járó myelodysplasztikus szindrómává (MDS)/akut myelogén leukémiává (AML) való átalakulás kockázata a G-CSF-kezelést követően további szerzett mutációkkal függ össze. Ezen esetek többségét a G-CSF-receptor mutációja okozza. Azokat a betegeket, akiknek az állapota klinikailag reagál a G-CSF-re, élethossziglan kezelik.
Az SCN más formáiban szenvedő betegek egy része a GFI1-ben, egy cink-ujjas transzkripciós represszor génben mutálódott, amely részt vesz a vérképző őssejtek működésében és a vérvonalhoz kötődő döntésekben.
A ciklikus neutropeniát (CN) a fertőzéssel összefüggő időszakos neutropenia rohamok jellemzik, amelyeket a perifériás neutrofilszám helyreállása követ. Periodicitása körülbelül 21 nap (12-35 d). A granulocita prekurzorok a ciklus minden egyes neutrofil mélypontja előtt eltűnnek a csontvelőből a myeloid progenitor sejtek felgyorsult apoptózisa miatt. Egyes esetek genetikailag meghatározottak lehetnek, autoszomális recesszív öröklődéssel. Más esetek autoszomális domináns öröklődésűek lehetnek. A CN egyes sporadikus eseteiben a betegeknél az ELA2 mutációi találhatók.
A CN-ben szenvedők jellemzően csecsemőként vagy gyermekként jelentkeznek, de léteznek a CN felnőttkorban szerzett formái is. A prognózis jó, jóindulatú lefolyású; a betegek 10%-ánál azonban életveszélyes fertőzések alakulnak ki. A ciklikus neutropenia kezelése a napi G-CSF.
Krónikus jóindulatú neutropenia
A családi krónikus jóindulatú neutropenia vagy jóindulatú etnikai neutropenia autoszomális domináns öröklődési mintázatú rendellenesség, amely afrikai, jemeni zsidó, etiópiai zsidó, arab, karibi és nyugat-indiai származásúaknál figyelhető meg. Az afrikai és jemeni zsidó felmenőkkel rendelkező populációkban a genetikai vizsgálatok erős összefüggést mutatnak a DARC gén egy egynukleotid-polimorfizmusával. A betegek jellemzően tünetmentesek, és a fertőzések enyhék. A krónikus jóindulatú neutropeniában szenvedő érintetteknél összességében alacsony a fertőzés kockázata, és nincs szükség specifikus terápiára.
A nem családi krónikus jóindulatú neutropeniában a jóindulatú lefolyású, enyhe fertőzések jellemzik ezt a betegséget. Az ANC azonban reagál a stresszre, például a fertőzésre, a kortikoszteroidokra és a katekolaminokra.
Idiopátiás krónikus súlyos neutropenia
Az idiopátiás krónikus súlyos neutropenia kizárásos diagnózis. Az érintett betegeknél fertőzések és súlyos neutropenia fordul elő.
Fenotípusos eltérésekkel járó neutropenia
A Shwachman-szindróma (Shwachman-Diamond) autoszomális recesszív öröklődési mintázatú. A neutropenia mérsékelt vagy súlyos, a halálozási arány 15-25%, és a szindróma csecsemőkorban jelentkezik, visszatérő fertőzésekkel, hasmenéssel és táplálkozási nehézségekkel. Előfordulhat törpeség, chondrodysplasia és hasnyálmirigy exokrin elégtelenség.
A Shwachman-Diamond-szindróma és az X-kromoszómával összefüggő dyskeratosis congenita (DC), a porc-haj hipoplasia (CHH) és a Diamond-Blackfan-anémia (DBA) közös génhibáknak tűnnek, amelyek a riboszómaszintézisben játszanak szerepet. A Shwachman-Diamond-szindróma legtöbb esetét az SBDS gén mutációi okozzák. Ennek a génnek a pontos funkciója még tisztázásra vár, azonban részt vesz a riboszómaszintézisben és az RNS-feldolgozási reakciókban. A kezelés a G-CSF.
A CHH-ban az öröklődési minta autoszomális recesszív a 9. kromoszómán, és amish és finn családokban figyelhető meg. A CHH-t az RMRP gén mutációi okozzák, amely a ribonukleáz mitokondriális RNS-feldolgozó komplex (RNáz MRP) RNS komponensét kódolja. A neutropenia mérsékelt vagy súlyos. A CHH sejtközvetített immunitás-hibákkal, makrocitikus vérszegénységgel, gyomor-bélrendszeri betegséggel és törpeséggel jelentkezik. Rákos megbetegedésre, különösen limfómára való hajlamot is mutat. A kezelés a csontvelő-átültetés.
A dyskeratosis congenita (Zinsser-Cole-Engman-szindróma) mentális retardációval, pancytopeniával és sejtközvetített immunitás hibájával jár. A Dyskeratosis congenita gyakrabban fordul elő férfiaknál, mint nőknél, és hematológiailag a Fanconi-anémiához hasonló. A Dyskeratosis congenita általában X-hez kötött recesszív, bár létezik autoszomális domináns és autoszomális recesszív formája is.
A rendellenesség X-hez kötött recesszív formáját a DKC1 mutációihoz kapcsolták, amely a dyskerint, egy ribonukleoprotein részecskékhez kapcsolódó nukleoláris fehérjét kódolja. Az autoszomális domináns forma egy másik gén, a TERC mutációihoz kapcsolódik, amely a telomeráz része. A telomeráznak fehérje- és RNS-összetevője is van, és a TERC az RNS-összetevőt kódolja. Az ebben a rendellenességben szenvedő betegek telomerjei rövidebbek a normálisnál. A kezelés G-CSF, granulocita-macrofág kolóniastimuláló faktor (GM-CSF) és csontvelő-átültetés.
A Barth-szindróma egy X-kromoszómához kötött recesszív rendellenesség, amely csecsemőkori kardiomiopátiával, csontvázmyopátiával, visszatérő fertőzésekkel, törpeséggel és mérsékelt vagy súlyos neutropeniával jelentkezik.
A Chediak-Higashi-szindróma egy autoszomális recesszív rendellenesség, amely visszatérő fertőzésekkel, szellemi lassulással, fotofóbiával, nystagmussal, oculocutan albinizmussal, neuropátiával, vérzési zavarokkal, ínygyulladással és különböző sejtek lizoszomális granulációjával jár. A neutropenia mérsékelt vagy súlyos, a kezelés a csontvelő-átültetés.
Myelokathexis
A myelokathexis csecsemőkorban mérsékelt neutropeniával jelentkezik, és visszatérő fertőzésekkel jár. Az állapot oka a neutrofil prekurzorok felgyorsult apoptózisa és a bcl-x csökkent expressziója. Kóros nukleáris megjelenés figyelhető meg, hipersegmentációval, magszálakkal, pyknózissal és citoplazmatikus vacuolizációval. A kezelés G-CSF és GM-CSF.
Laza leukocita szindróma
A laza leukocita szindróma súlyos neutropenia, amelyhez rendellenes neutrofil motilitás társul. Az etiológia ismeretlen, a kezelés szupportív jellegű.
Metabolikus rendellenességek
Ezek krónikus neutropéniák, változó ANC-vel. They include glycogen storage disease type 1b and various acidemias, such as isovaleric, propionic, and methylmalonic. In glycogen storage disease type 1b, the treatment is G-CSF and GM-CSF.
Acquired neutropenia caused by intrinsic bone marrow disease
Intrinsic bone marrow diseases that may cause neutropenia include the following:
-
Aplastic anemia
-
Hematologic malignancy (eg, leukemia, lymphoma, myelodysplasia, myeloma)
-
Ionizing radiation
-
Tumor infiltration
-
Granulomatous infection
-
Myelofibrosis
Immune-mediated neutropenia
A drug may act as a hapten and induce antibody formation. This mechanism operates in cases due to gold, aminopyrine, and antithyroid drugs. The antibodies destroy the granulocytes and may not require the continued presence of the drug for their action. Alternatively, the drug may form immune complexes that attach to the neutrophils. This mechanism operates with quinidine.
Drug immune-mediated neutropenia may be caused by the following:
-
Aminopyrine
-
Quinidine
-
Cephalosporins
-
Penicillins
-
Sulfonamides
-
Phenothiazines
-
Hydralazine
Other medications have been implicated
Autoimmune neutropenia is the neutrophil analogue of autoimmune hemolytic anemia and of idiopathic thrombocytopenic neutropenia. It should be considered in the absence of any of the common causes. Antineutrophil antibodies have been demonstrated in these patients. Autoimmune neutropenia may be associated with the following:
-
Rheumatoid arthritis (with or without Felty syndrome)
-
Sjögren syndrome
-
Chronic, autoimmune hepatitis
-
Systemic lupus erythematosus
-
Thymoma
-
Goodpasture disease
-
Granulomatosis with polyangiitis (Wegener granulomatosis)
-
Pure red blood cell (RBC) aplasia, in which there is complete disappearance of granulocyte tissue from the bone marrow; pure RBC dysplasia is a rare disorder due to the presence of antibody-mediated, granulocyte-macrophage colony forming unit (GM-CFU) inhibitory activity, and it is often associated with thymoma
-
Transfusion reactions, which can be caused by the surface antigens of neutrophilia; az ismételt granulocita transzfúzióban részesülők alloimmunizálódhatnak
-
nagy szemcsés limfocita proliferáció vagy leukémia
Az izoimmun újszülöttkori neutropeniában az anya IgG antineutrofil antitesteket termel a magzati neutrofil antigénekkel szemben, amelyeket nem önmaguként ismer fel. Ez az élve születések 3%-ában fordul elő. A rendellenesség újszülöttkori láz, húgyúti fertőzés, cellulitis, tüdőgyulladás és szepszis formájában jelentkezik. A neutropenia időtartama jellemzően 7 hét.
A krónikus autoimmun neutropenia felnőtteknél figyelhető meg, és nincs életkori predikciója. A betegek 36%-ánál mutatkoznak szérum antineutrofil antitestek, és a klinikai lefolyás általában kevésbé súlyos. A betegeknél ez a betegség szisztémás lupus erythematosus, rheumatoid arthritis, Wegener granulomatosis és krónikus hepatitis társulhat.
Ha a krónikus autoimmun neutropenia ezekhez a betegségekhez társul, kezelésként kortikoszteroidok alkalmazása javallott. Újszülötteknél és gyermekeknél ez a rendellenesség a fertőzések kisebb kockázatával és a középfül, a gyomor-bélrendszer és a bőr enyhébb fertőzéseivel jár.
A T-gamma limfocitózis vagy limfoproliferatív rendellenesség a CD3+ T-limfociták vagy CD3- természetes ölősejtek (NK) klonális betegsége, amelyek a csontvelőt és a szöveteket infiltrálják. A nagy szemcsés limfociták leukémiája (LGL-leukémia) néven is ismert T-gamma-limfocitózis társulhat reumatoid artritiszhez, és magas titerű antineutrofil antitestekkel jár együtt. A neutropenia tartós és súlyos. A kezelés gyakran szupportív jellegű, de a klónpopuláció eliminálására is irányul.
Fertőzés okozta szerzett neutropenia
A szerzett neutropenia leggyakoribb formája a fertőzés. A neutropeniát okozó fertőzések közé tartoznak többek között a következők:
-
Bacterial sepsis
-
Viral infections (eg, influenza, measles, Epstein Barr virus , cytomegalovirus , viral hepatitis, human immunodeficiency virus -1) (see first image below)
-
Toxoplasmosis
-
Brucellosis
-
Typhoid
-
Tuberculosis (see second and third images below)
-
Malaria
-
Dengue fever
-
Rickettsial infection
-
Babesiosis
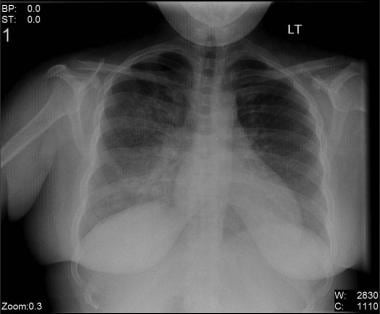 Bilateral interstitial infiltrates in a 31-year-old patient with influenza pneumonia.
Bilateral interstitial infiltrates in a 31-year-old patient with influenza pneumonia. 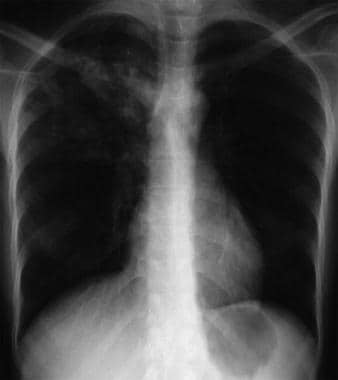 Anteroposterior chest radiograph in a young ED patient presenting with cough and malaise. The radiograph shows a classic posterior segment right upper lobe density consistent with active tuberculosis. Ezt a nőt elkülönítésre vették fel, és a sürgősségi osztályon empirikusan 4 gyógyszeres kezelést kezdtek el alkalmazni. A köpetvizsgálat megerősítette a tuberkulózist. A kép a Remote Medicine, remotemedicine.org jóvoltából.
Anteroposterior chest radiograph in a young ED patient presenting with cough and malaise. The radiograph shows a classic posterior segment right upper lobe density consistent with active tuberculosis. Ezt a nőt elkülönítésre vették fel, és a sürgősségi osztályon empirikusan 4 gyógyszeres kezelést kezdtek el alkalmazni. A köpetvizsgálat megerősítette a tuberkulózist. A kép a Remote Medicine, remotemedicine.org jóvoltából. 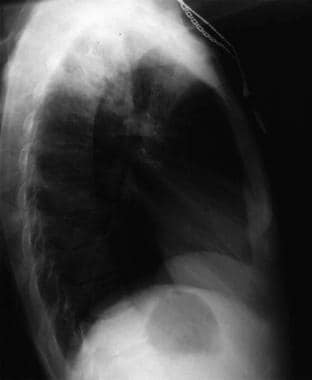 Laterális mellkasi röntgenfelvétel egy 31 éves betegnél influenzás tüdőgyulladással. A kép a Remote Medicine, remotemedicine.org jóvoltából.
Laterális mellkasi röntgenfelvétel egy 31 éves betegnél influenzás tüdőgyulladással. A kép a Remote Medicine, remotemedicine.org jóvoltából.
A leggyakrabban érintett organizmusok az endogén flórából származnak. A Staphylococcus aureus organizmusok bőrfertőzések esetén fordulnak elő. Gram-negatív organizmusok figyelhetők meg a húgyúti és gyomor-bélrendszeri fertőzésekben, különösen Escherichia coli és Pseudomonas fajok. Candida albicans fertőzések is előfordulhatnak. A szájüregben vegyes flóra fordulhat elő.
A vírusfertőzések gyakran vezetnek enyhe vagy mérsékelt neutropeniához. Az agranulocitózis ritka, de előfordulhat. A leggyakoribb kórokozók az Epstein-Barr-vírus, a hepatitis B vírus, a sárgaláz vírus, a citomegalovírus és az influenza. Számos lehengerlő fertőzés, vírusos és bakteriális egyaránt, súlyos neutropeniát okozhat.
Táplálékhiány okozta szerzett neutropenia
A neutropeniát okozó táplálékhiányok közé tartozik a B-12-vitamin, a folsav és a rézhiány.
gyógyszerek és vegyi anyagok okozta szerzett neutropenia, kivéve a citotoxikus kemoterápiát
Néhány gyógyszert hoztak kapcsolatba neutropeniával. A legnagyobb kockázati kategóriába a pajzsmirigyellenes gyógyszerek, a makrolidok és a prokainamidok tartoznak. Mint fentebb említettük, számos gyógyszer immunmediált mechanizmussal hat. Úgy tűnik azonban, hogy néhány gyógyszer közvetlen toxikus hatást gyakorol a csontvelő őssejtjeire vagy a mitotikus kompartmentben lévő neutrofil prekurzorokra. Például az olyan gyógyszerek, mint az antipszichotikumok és antidepresszánsok, valamint a klóramfenikol az ilyen módon történő metabolizmus és érzékenység alapján egyes egyéneknél közvetlen toxinként hathatnak. Más gyógyszerek immun- és nem immunmechanizmusok kombinációjával vagy ismeretlen hatásmechanizmussal rendelkezhetnek.
Az antimikrobás szerek közé tartozik a penicillin, a cefalosporinok, a vancomycin, a klóramfenikol, a gentamicin, a klindamicin, a doxiciklin, a flucitozin, a nitrofurantoin, a novobiocin, a minociklin, a griseofulvin, a lincomycin, a metronidazol, a rifampin, az izoniazid, a streptomicin, tiacetazon, mebendazol, pirimetamin, levamisol, ristocetin, szulfonamidok, klorokvin, hidroxiklorokvin, kinakrin, etambutol, dapson, ciprofloxacin, trimetoprim, imipenem/cilastatin, zidovudin, fludarabin, acyclovir és terbinafin.
A fájdalomcsillapítók és gyulladáscsökkentők közé tartozik az aminopirin, dipiron, indometacin, ibuprofen, acetilszalicilsav, diflunisal, szulindak, tolmetin, benoxaprofen, barbiturátok, mezalazin és kinin.
Az antipszichotikumok, antidepresszánsok és neurofarmakológiai szerek közé tartoznak a fenotiazinok (klórpromazin, metilpromazin, mepazin, promazin, tioridazin, proklórperazin, trifluoperazin, trimeprazin), klozapin, riszperidon, imipramin, desipramin, diazepám, klórdiazepoxid, amoxapin, meprobamát, tiotixen és haloperidol.
A görcsoldók közé tartozik a valproinsav, a fenitoin, a trimetadion, a mefenitoin (mesantoin), az etoszuximid és a karbamazepin.
A pajzsmirigy elleni gyógyszerek közé tartozik a tiouracil, a propiltiuracil, a metimazol, a karbimazol, a káliumperklorát és a tiocianát.
A szív- és érrendszeri gyógyszerek közé tartozik a procainamid, a kaptopril, az aprindin, a propranolol, a hidralazin, a metildopa, a kinidin, a diazoxid, a nifedipin, a propafenon, a tiklopidin és a vesnarinon.
Az antihisztaminok közé tartozik a cimetidin, ranitidin, tripelennamin (piribenzamin), metafenilén, thenalidin, bromfeniramin és mianserin.
A diuretikumok közé tartozik az acetazolamid, bumetanid, klórtiazid, hidroklorotiazid, klórtalidon, metazolamid és spironolakton.
A hipoglikémiás szerek közé tartozik a klórpropamid és a tolbutamid.
A malária elleni gyógyszerek közé tartozik az amodiaquin, a dapson, a hidroxiklorokvin, a pirimetamin és a kinin.
A különféle gyógyszerek közé tartozik az allopurinol, kolhicin, aminoglutetimid, famotidin, bezafibrát, flutamid, tamoxifen, penicillamin, retinsav, metoklopramid, fenindion, dinitrofenol, etakrinsav, diklór-difenil-triklór-etán (DDT), cinchophen, antimon, pirithyldion, rauwolfia, etanol, klórpropamid, tolbutamid, tiazidok, spironolakton, metazolamid, acetazolamid, IVIG és levodopa.
A nehézfémek közé tartozik az arany, az arzén és a higany.
A gyógyszerek vagy vegyi anyagok expozíciója az agranulocitózis leggyakoribb oka: a betegek körülbelül felénél előfordult gyógyszer- vagy vegyi expozíció. Bármilyen vegyi anyag vagy gyógyszer, amely képes a csontvelő depressziójára és hipopláziát vagy apláziát okozhat, képes agranulocitózist okozni. Egyes gyógyszerek mindenkinél ezt teszik, ha elég nagy dózisban adják be őket. Úgy tűnik, hogy más szerek idioszinkrikus reakciókat okoznak, amelyek csak bizonyos fogékony egyéneket érintenek.
Egyes szerek (pl. a valproinsav, a karbamazepin és a béta-laktám antibiotikumok) a myelopoiesis közvetlen gátlásával hatnak. Csontvelőkultúrákban ezek a szerek dózisfüggő módon gátolják a granulocita kolóniaképződést. A csontvelő mikrokörnyezetének vagy a myeloid prekurzoroknak a közvetlen károsodása a legtöbb más esetben szerepet játszik.
Az agranulocitózissal összefüggésbe hozható gyógyszerek közül sokat jelentettek az amerikai Élelmiszer- és Gyógyszerügyi Hivatalnak (FDA) a mellékhatások jelentési kötelezettsége alapján. Számos hatóanyagot az Amerikai Orvosi Szövetség (AMA) által vezetett nyilvántartásba is jelentenek. A bejelentett gyógyszereket önmagukban, egy másik potenciálisan toxikusnak ismert gyógyszerrel kombinálva vagy egy másik, ismert toxicitással nem rendelkező gyógyszerrel együtt alkalmazták. Több gyógyszer különösen figyelemre méltó, mivel nagy gyakorisággal fordul elő, hogy agranulocitózissal társulnak. Ezek közé tartoznak a következők:
-
Phenothiazine
-
Antithyroid drugs (thiouracil and propylthiouracil)
-
Aminopyrine
-
Chloramphenicol
-
Sulfonamides
Miscellaneous immunologic neutropenias
Immunologic neutropenias may occur after bone marrow transplantation and blood product transfusions.
Felty syndrome is a syndrome of rheumatoid arthritis, splenomegaly, and neutropenia. Splenectomy shows an initial response, but neutropenia may recur in 10-20% of patients. Treatment is directed toward rheumatoid arthritis.
In complement activation–mediated neutropenia, hemodialysis, cardiopulmonary bypass, and extracorporeal membrane oxygenation (ECMO) expose blood to artificial membranes and can cause complement activation with subsequent neutropenia.
In splenic sequestration, the degree of neutropenia resulting from this process is proportional to the severity of the splenomegaly and the bone marrow’s ability to compensate for the reduction in circulating bands and neutrophils.
Eosinopenia and basophilopenia
Eosinopenia may be associated with the following:
-
Acute bacterial infection
-
Glucocorticoid administration
-
Physical stress
-
Thymoma
Decreased circulating basophils may be associated with the following:
-
Anaphylaxis
-
Acute infection
-
Drug-induced hypersensitivity
-
Congenital absence of basophils
-
Hemorrhage
-
Hyperthyroidism
-
Ionizing radiation
-
Neoplasia
-
Ovulation
-
Urticaria
-
Drugs (eg, corticosteroid, adrenocorticotropic hormone therapy, chemotherapeutic agents, thyroid hormones)
Go to Pediatric Autoimmune and Chronic Benign Neutropenia for complete information on this topic.
-
 Bilateral interstitial infiltrates in a 31-year-old patient with influenza pneumonia.
Bilateral interstitial infiltrates in a 31-year-old patient with influenza pneumonia.  Anteroposterior chest radiograph in a young ED patient presenting with cough and malaise. The radiograph shows a classic posterior segment right upper lobe density consistent with active tuberculosis. Ezt a nőt elkülönítésre vették fel, és a sürgősségi osztályon empirikusan 4 gyógyszeres kezelést kezdtek el alkalmazni. A köpetvizsgálat megerősítette a tuberkulózist. A kép a Remote Medicine, remotemedicine.org jóvoltából.
Anteroposterior chest radiograph in a young ED patient presenting with cough and malaise. The radiograph shows a classic posterior segment right upper lobe density consistent with active tuberculosis. Ezt a nőt elkülönítésre vették fel, és a sürgősségi osztályon empirikusan 4 gyógyszeres kezelést kezdtek el alkalmazni. A köpetvizsgálat megerősítette a tuberkulózist. A kép a Remote Medicine, remotemedicine.org jóvoltából.  Laterális mellkasi röntgenfelvétel egy 31 éves betegnél influenzás tüdőgyulladással. A kép a Remote Medicine, remotemedicine.org jóvoltából.
Laterális mellkasi röntgenfelvétel egy 31 éves betegnél influenzás tüdőgyulladással. A kép a Remote Medicine, remotemedicine.org jóvoltából.