Projekty naukowe dla początkujących: Chemia
Chemia
Salt or Sugar: Which Dissolves Faster in Different Liquids
Rozwiązania to nic innego jak mieszaniny różnych związków lub elementów. Z roztworami spotykasz się codziennie, nawet o tym nie wiedząc.
Nawet powietrze, którym oddychasz, zawierające wodę, jest roztworem cieczy i gazu. Jeśli wypiłeś dziś napój gazowany, to tak naprawdę wypiłeś roztwór gazu rozpuszczonego w wodzie smakowej. Jeśli nosisz bransoletkę wykonaną ze srebra, to masz na sobie roztwór dwóch metali.
W tym eksperymencie będziesz pracował z roztworem cieczy, który jest jednym z trzech rodzajów roztworów. Pozostałe typy to roztwory gazowe i roztwory stałe.
Więc co wydaje się być problemem?
Rozpuszczalnik to substancja?ciało stałe, ciecz lub gaz, która ulega rozpuszczeniu. Rozpuszczalnik, który również może być ciałem stałym, cieczą lub gazem, to substancja, która dokonuje rozpuszczenia. Roztwór jest jednolitą mieszaniną solutu (zazwyczaj ciała stałego) rozpuszczonego w rozpuszczalniku (zazwyczaj cieczy).
Gdy mieszasz łyżkę cukru w szklance wody, tworzysz roztwór. Ten rodzaj roztworu ciekłego składa się ze stałego solutu, którym jest cukier, i ciekłego rozpuszczalnika, którym jest woda. Jak cząsteczki cukru rozprzestrzeniają się równomiernie w wodzie, cukier rozpuszcza się.
Mieszanie cieczy w gazie tworzy inny typ roztworu, zwany roztworem gazowym. Przykładem tego typu roztworu jest wilgoć. Wilgotność to woda (ciecz) rozpuszczona w powietrzu (gaz).
Pomyśl o tym jak kostka cukru rozpuszcza się w wodzie, w porównaniu do paczki sypkiego cukru. Kostka rozpuszcza się wolniej, ponieważ mniej cząsteczek cukru jest początkowo w kontakcie z wodą.
W roztworze stałym, takim jak srebro próby 925, miedź, która została podgrzana w wysokiej temperaturze jest mieszana ze srebrem, które również zostało podgrzane aż do stopienia. Miedź jest solutem, czyli substancją, która rozpuści się w rozpuszczalniku. Srebro jest rozpuszczalnikiem.
Rodzaj roztworu jest określany przez stan skupienia substancji rozpuszczającej. Jeżeli substancja dokonująca rozpuszczania jest cieczą, to roztwór nazywamy roztworem ciekłym. Jeśli rozpuszczalnik jest gazem, roztwór nazywamy gazowym. I dobrze zgadłeś: Rozpuszczalnik stały utworzy roztwór stały.
Możesz sprawdzić wielkość kryształów soli i cukru pod mikroskopem lub szkłem powiększającym, co pozwoli ci zobaczyć również ich kształty. Jeśli narysujesz to, co widzisz, używając ołówka, tak abyś mógł zilustrować cieniowanie, możesz dołączyć ilustrację jako część końcowej prezentacji swojego projektu science fair.
Istnieje kilka czynników, które generalnie zwiększają ilość rozpuszczalnika, który może być rozpuszczony. Jeśli chcesz rozpuścić więcej cukru w tej samej ilości wody, na przykład, możesz podgrzać wodę. Możesz również zmielić cukier na mniejsze cząstki, aby zwiększyć jego powierzchnię, lub możesz mieszać mieszaninę.
W latach, w których używałeś soli i cukru do swoich potraw, prawdopodobnie zauważyłeś, że każdy kawałek soli?który w rzeczywistości jest kryształem, jest trochę mniejszy niż każdy kawałek cukru, który również jest kryształem.
Cząsteczka to dwa lub więcej elementów, które są chemicznie połączone. Cząsteczka soli zawiera sód i chlor, które są chemicznie połączone, aby stworzyć chlorek sodu. Wzór chemiczny tej soli to NaCl. Cząsteczka cukru zawiera węgiel, wodór i tlen. Wzór chemiczny cukru to C12H22O11.
Problem, który będziesz próbował rozwiązać w tym eksperymencie dotyczy tego, czy cukier lub sól rozpuszcza się szybciej po zmieszaniu z różnymi cieczami. Czy wielkość kawałków wpływa na to, jak szybko mieszają się z cieczą?
Kiedy rozpuszczasz cukier lub sól w cieczy, na przykład w wodzie, to co się dzieje, to fakt, że cząsteczki cukru poruszają się, aby dopasować się pomiędzy cząsteczkami wody w szklance lub zlewce. Ilustracja poniżej pokazuje, jak różne cząsteczki są rozmieszczone w pojemniku.
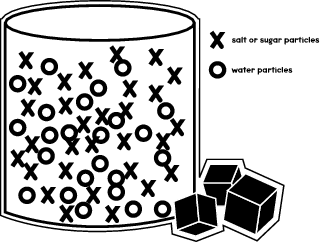
W doświadczeniu zobaczysz, jak cząsteczki soli i cukru poruszają się w różnych cieczach i rozpuszczają się w różnym tempie.
Tytuł tej sekcji, ?Salt or Sugar: Which Dissolves Faster in Different Liquids??? może służyć jako tytuł twojego projektu, jeśli chcesz. Możesz również rozważyć jeden z następujących tytułów dla swojego projektu:
- Wielki Konkurs Rozpuszczania Soli i Cukru
- Używanie Soli i Cukru do Badania Jak Substancje Rozpuszczają się
Cokolwiek wybierzesz, jest w porządku. Zastanówmy się teraz przez chwilę, dlaczego ten projekt jest wartościowym wykorzystaniem Twojego czasu.
What’s the Point?
Gdy pomiędzy cząsteczkami rozpuszczalnika jest dużo miejsca, mówi się, że rozpuszczalnik jest nienasycony. Gdy w rozpuszczalniku rozpuściła się duża ilość solutu, ale między cząsteczkami jest jeszcze trochę miejsca, roztwór jest stężony. Kiedy absolutnie żaden solute nie może być rozpuszczony w rozpuszczalniku, roztwór jest nasycony.
A kiedy nadmiar solute został rozpuszczony przez ogrzewanie roztworu, mówi się, że jest on przesycony.
Punktem tego eksperymentu, oprócz nauki, czy sól lub cukier rozpuszcza się szybciej w różnych cieczach, jest nauka, jak cząsteczki oddziałują ze sobą w roztworze.
Jak widzieliście na poprzedniej ilustracji, cząsteczki wody zajmują większość miejsca w pojemniku. Ale jest jeszcze trochę wolnego miejsca, w którym mogą się zmieścić cząsteczki cukru lub soli. Dzięki waszemu eksperymentowi dowiecie się, jak szybko cząsteczki cukru mieszczą się w tych przestrzeniach w porównaniu z cząsteczkami soli.
Wiedza o tym pomoże wam lepiej zrozumieć proces, który zachodzi podczas rozpuszczania substancji.
Kontrolą w waszym eksperymencie będzie woda. Pozostałe ciecze, w których rozpuścisz sól i cukier będą zmiennymi.
| Kontrola: | Rozpuszczalnik?woda |
| Rozpuszczalniki?cukier, sól | |
| Zmienne: | Pięć różnych przezroczystych cieczy (mogą być kolorowe) |
Pamiętaj, gdy będziesz przeprowadzać eksperyment, że bardzo ważne jest, aby wszystkie ciecze, których używasz, miały tę samą temperaturę. Nauczyłeś się już, że cukier rozpuszcza się szybciej w ciepłej cieczy niż w chłodnej, więc wiesz, że nie byłby to dokładny eksperyment, gdyby niektóre z cieczy, których używasz, były ciepłe, a niektóre zimne. Temperatura cieczy stałaby się zmienną.
Dlatego wszystkie ciecze, których używasz, włączając w to wodę, powinny mieć temperaturę pokojową. Jeśli zwykle trzymasz je w lodówce, upewnij się, że pozwolisz im siedzieć na blacie przez noc, aż wszystkie będą miały tę samą temperaturę.
Aby dać ci trochę więcej elastyczności podczas przeprowadzania eksperymentu, możesz wybrać płyny, w których będziesz rozpuszczać cukier i sól. Nie ma sensu wychodzić z domu i kupować dodatkowych płynów, jeśli już masz to, czego potrzebujesz.
Nie zakładaj, że płyny, które siedziały w różnych miejscach w twoim domu mają taką samą temperaturę. Na przykład butelka sody, która stoi w garażu, może być o kilka stopni chłodniejsza niż alkohol z szafki w łazience lub sok jabłkowy z kuchennej spiżarni. Upewnij się, że wszystkie płyny znajdują się w tym samym miejscu, aby mogły osiągnąć tę samą temperaturę pokojową. If you don’t, the results of your experiment won’t be valid.
Just make sure you choose liquids that are different from each other in taste, color, odor, and purpose. You’ll also need to select those that allow you to observe the salt and sugar as it dissolves. If you use milk or orange juice, for example, you won’t be able to watch the salt and sugar dissolve. Some suggestions for liquids to consider are:
- White vinegar
- Club soda
- Ginger ale
- Glass cleaner (such as Windex)
- Lemonade
- Tea or iced tea (each at room temperature)
- Apple juice
- Rubbing alcohol
All of these are commonly found around the house, perhaps saving you a trip to the store.
What Do You Think Will Happen?
Teraz, gdy wiesz jak tworzą się roztwory i znasz niektóre czynniki, które wpływają na szybkość rozpuszczania się cukru i soli, powinieneś być w stanie zgadnąć, który z nich rozpuści się szybciej.
Jeśli nie robiłeś tego eksperymentu wcześniej, nie będziesz wiedział, czy płyny, których użyjesz, będą czynnikiem wpływającym na rozpuszczanie soli i cukru. To sprawia, że trudniej jest postawić hipotezę, ale nie martw się. Czy twoja hipoteza okaże się poprawna, czy nie, nie ma wpływu na ważność lub wynik twojego eksperymentu.
Choć nie będziesz wiedział do czasu zakończenia eksperymentu, czy właściwości różnych cieczy, które wybierzesz, wpłyną na szybkość rozpuszczania soli i cukru, wiesz, że kryształy soli są na ogół mniejsze niż kryształy cukru. I wiesz, że temperatura płynów nie będzie czynnikiem w twoim eksperymencie.
Postaraj się wykorzystać swoje przeszłe doświadczenia, informacje, które przeczytałeś wcześniej w tym rozdziale, i zdrowy rozsądek, aby wymyślić solidną hipotezę.
Pamiętaj, że twoja hipoteza musi być podana jako obiektywne zdanie, a nie pytanie. Więc idź dalej i zgadnij czy sól lub cukier rozpuści się szybciej, i zacznijmy eksperyment.
Materiały, których będziesz potrzebował do tego projektu
Niektóre płyny sugerowane do użycia w tym eksperymencie to: biały ocet, soda klubowa, piwo imbirowe, płyn do mycia szyb, alkohol, sok jabłkowy, lemoniada i herbata. Jeśli chcesz zastąpić inny płyn dla jednego lub więcej z tych sugerowanych, to dobrze. Upewnij się tylko, że wszystkie płyny są czyste i mają temperaturę pokojową.
Ilości materiałów wymienionych poniżej są wystarczające do przeprowadzenia eksperymentu trzy razy z każdym płynem. You’ll need:
- 12 clear, plastic cups (10 ounce )
- One permanent marker
- One (1 teaspoon) (5.0 ml) measuring spoon
- One (12 teaspoon) (2.5 ml) measuring spoon
- One (1 cup) (240 ml) measuring cup
- 8 teaspoons (40 ml) salt, divided in 16 (12 teaspoon) portions
- 8 teaspoons (40 ml) sugar, divided in 16 (12 teaspoon) portions
- 48 ounces (1,440 ml) water at room temperature
- 24 ounces (720 ml) each of five different, clear liquids, all at room temperature
- One clock or watch with a second hand
- One clear plastic cup containing eight fluid ounces (240 ml) water at room temperature
Remember to make sure that all liquids are at room temperature.
Conducting Your Experiment
When you’ve gathered all your materials, you’ll be ready to begin your experiment. Wykonaj następujące kroki:
Zachowaj kubek zwykłej wody w zasięgu wzroku, abyś mógł porównać go z kubkami zawierającymi sól i cukier. Ciekawie będzie obserwować jak zmienia się wygląd płynów w miarę rozpuszczania się soli i cukru.
Trochę potrwa zanim cukier i sól się rozpuszczą. Aby uzyskać najlepsze wyniki, nie należy mieszać roztworów, ponieważ spowoduje to dodatkową zmienną. Jeśli musisz mieszać, to mieszaj każdy roztwór trzy razy i przestań. Mieszaj dopiero wtedy, gdy zauważysz, że na dnie każdego z dwóch pojemników znajduje się rozpuszczony roztwór. Nierównomierne mieszanie roztworów spowoduje, że twój eksperyment będzie nieważny.
- Używając markera permanentnego, napisz ?sól? na sześciu plastikowych kubeczkach, a ?cukier? na pozostałych sześciu.
- Umieść 1/2 łyżeczki (2.5 ml) soli w każdym z sześciu kubeczków oznaczonych jako ?sól.
- Umieść 1/2 łyżeczki (2.5 ml) cukru w każdym z sześciu kubków oznaczonych jako ?cukier?.
- Dodaj 8 uncji (240 ml) wody do jednej filiżanki zawierającej sól i jednej filiżanki zawierającej cukier. Natychmiast zapisz czas, w którym woda została dodana, na wykresie danych podobnym do tego, który jest pokazany w następnej części, ?
- Zaobserwuj, jak rozpuszczalniki (sól i cukier) rozpuszczają się w rozpuszczalniku (wodzie). Zapisz na wykresie danych czas, w którym wydaje ci się, że każdy solut całkowicie się rozpuścił. Czasy te prawdopodobnie nie będą takie same.
- Oblicz czas, jaki upłynął, w którym nastąpiło rozpuszczenie. Weź czas, w którym woda została dodana do kubków, a rozpuszczanie się rozpoczęło i odejmij go od czasu, w którym rozpuszczanie się zakończyło. To daje całkowitą liczbę minut, które zajęło soli i cukru, aby całkowicie rozpuścić się w płynie.
- Powtórz kroki od 4 do 6, używając każdego innego płynu zamiast wody.
- Umyj, opłucz i dokładnie wysusz każdy z 12 kubków.
- Powtórz kroki od 2 do 8 jeszcze dwa razy, w sumie trzy próby dla każdego z sześciu płynów.
- Oblicz średni czas rozpuszczania soli i cukru w każdym z sześciu płynów.
Pamiętaj, że aby znaleźć średni czas potrzebny do rozpuszczenia soli i cukru w każdym płynie, dodajesz trzy czasy zarejestrowane dla każdego z nich, a następnie dzielisz je przez trzy. Liczba, którą otrzymasz po podzieleniu czasów to średni czas.
Keeping Tracking of Your Experiment
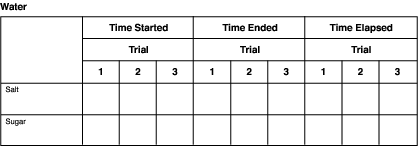
Wykresy takie jak poniższy mogą być użyte do zapisania informacji dla każdego rozpuszczalnika. Wystarczy zmienić nazwy rozpuszczalników w nagłówku.
Pamiętaj, aby zapisywać czasy w miarę postępu prac. Nie polegaj na swojej pamięci, aby zapisać je później. Do czasu zakończenia eksperymentu będziesz miał wiele liczb.
Podsumowując wszystko razem
Co zauważyłeś na temat szybkości rozpuszczania się soli i cukru? Czy udowodniłeś, że twoja hipoteza jest poprawna? Czy też błędną? Czy mogłeś wykryć jakiś wzór podczas dodawania soli i cukru do różnych płynów? Czy było oczywiste, że w niektórych cieczach sól rozpuszcza się lepiej i szybciej niż cukier? Czy możesz pomyśleć o jakichkolwiek powodach, dla których tak mogło się stać?
Czy myślisz, że natura chemiczna solutu i rozpuszczalnika wpłynęła na szybkość rozpuszczania? Użyj informacji, które zebrałeś podczas badania tematu, aby pomóc Ci odpowiedzieć na te pytania.
Im więcej wiesz o swoim projekcie, tym lepiej będziesz w stanie przeanalizować swoje dane poprawnie i dojść do rozsądnych wniosków.
Dalsze badania
Jak wspomniano wcześniej, czynnikami wpływającymi na rozpuszczalność stałych solutów są:
- Zwiększanie lub zmniejszanie temperatury rozpuszczalnika
- Zwiększanie powierzchni rozpuszczalnika
- Budzenie
Jeśli chciałbyś pójść o krok lub dwa dalej, mógłbyś zaprojektować eksperyment, który przetestowałby jedną?lub może wszystkie te zmienne.
Możesz łatwo porównać szybkość rozpuszczania się kostek cukru w cieczy z szybkością rozpuszczania się cukru granulowanego.
Możesz też użyć tego samego rozpuszczalnika, powiedzmy cukru, i sprawdzić, czy mieszanie roztworu spowodowało jego szybsze rozpuszczenie. Podgrzewanie i chłodzenie rozpuszczalnika w trakcie dodawania tego samego rozpuszczalnika również byłoby możliwe do dalszego eksperymentowania.
Jeśli jesteś ciekawy i chętny do eksperymentowania, prawdopodobnie możesz wymyślić wiele wariantów tego projektu. A ponieważ eksperyment wymaga tylko powszechnych, niedrogich materiałów, powinieneś być w stanie eksperymentować do woli.
Wstęp z The Complete Idiot’s Guide to Science Fair Projects 2003 autorstwa Nancy K. O’Leary i Susan Shelly. Wszystkie prawa zastrzeżone, łącznie z prawem reprodukcji w całości lub w części w jakiejkolwiek formie. Wykorzystano po uzgodnieniu z Alpha Books, członkiem Penguin Group (USA) Inc.
Aby zamówić tę książkę bezpośrednio od wydawcy, odwiedź stronę Penguin USA lub zadzwoń pod numer 1-800-253-6476. Możesz również kupić tę książkę na Amazon.com i Barnes & Noble.