Aplicar a geociência aos desafios mais importantes da Austrália
Introdução

Folha de alumínio. Fonte: Wikimedia Commons
Alumínio está à sua volta – desde itens do dia-a-dia, como uma lata de refrigerante, até à aeronave que voa sobrevoa. O alumínio é um dos materiais mais úteis conhecidos pelo homem. Ele pode ser ligado (misturado) com quase qualquer outro metal para criar materiais com propriedades úteis. Metais ligados com alumínio são todos muito fortes mas leves, e resistentes à oxidação.
Após oxigênio e silício, o alumínio é o terceiro elemento mais abundante na crosta terrestre (8,2%) e de longe o metal mais abundante. Ao contrário de metais como o cobre, ouro, chumbo, ferro e zinco, que são utilizados pelo homem há milhares de anos, o alumínio só tem sido usado em comum há pouco mais de 100 anos. Isto porque o alumínio nunca é encontrado no seu estado puro na natureza. Assim, embora os humanos soubessem dos compostos de alumínio, só descobriram como extrair metal de alumínio no final dos anos 1800.
Alumínio pode ser extraído (não economicamente) de algumas argilas, mas o minério de alumínio mais comum é um material chamado bauxita. Primeiro o minério de alumínio precisa ser extraído, depois a bauxita é refinada em alumina (óxido de alumínio). Grandes quantidades de electricidade são utilizadas para fundir a alumina em metal de alumínio.
Propriedades
Alumínio é um metal de cor prateada que nunca é encontrado por si só na natureza. É muito leve (cerca de um terço do peso do cobre) mas forte; algumas ligas são ainda mais fortes do que o aço. O alumínio é maleável (pode ser prensado em forma) e dúctil (pode ser batido e estirado num arame). O alumínio é um muito bom condutor de calor e eléctrico. Também é altamente resistente à ferrugem, e não é tóxico. O alumínio pode ser ligado a quase qualquer outro metal. O alumínio é inflamável, não magnético e não deixa marcas. These properties have made it an important metal in the modern world. As aluminium is such a reactive metal, you might think it would rust badly and therefore be useless. However, pure aluminium reacts very quickly with air or water to form a thin, almost invisible layer of aluminium oxide on its surface, which then acts as a protective coating preventing any further ‘rusting’.
|
The Properties of Aluminium |
|
|---|---|
|
Chemical symbol |
Al – from the Roman word Alumen – the word for the aluminium-potassium compound alum |
|
Ore |
Bauxite |
|
Relative density |
2.7 g/cm3 |
|
Hardness |
2.75 on Mohs scale |
|
Malleability |
High |
|
Ductility |
High |
|
Melting point |
660°C |
|
Boiling Point |
2470°C |
Uses

Aluminium-bodied Austin “A40 Sports” (c. 1951). Fonte: Wikimedia Commons
Aluminium is smelted from alumina which is refined from bauxite ore. All three products have a number of uses.
More than 90% of the world’s bauxite production is used to make alumina with most of the remaining 10% used by the abrasive, refractory and chemical industries. Bauxite is also used in the production of high-alumina cement, as an absorbent or catalyst by the oil industry, in welding rod coatings and as a flux in making steel and ferroalloys.
Alumina’s primary use is as feedstock for aluminium smelters, however it is also used for other industrial purposes. It is used in glass, porcelain and in metallic paints, such as those sprayed on cars. Também é utilizada na produção de isoladores de velas de ignição, como componente combustível para impulsionadores de foguetes sólidos, enchimento de plásticos, um abrasivo (é mais barato que o diamante industrial) e em refinarias de metal onde é utilizada para converter gases tóxicos de resíduos de sulfureto de hidrogénio em enxofre elementar.
Alumina que ocorre em estado natural e cristalino é referida como o corindo mineral. Às vezes, os cristais de coríndon estão contaminados com vestígios de cromo, ferro, titânio, cobre ou magnésio. Chamamos estes cristais de rubis e safiras.
Depois do ferro e do aço, o alumínio é o metal mais utilizado na Terra. É frequentemente ligado com cobre, zinco, magnésio, manganês ou silício e a adição de pequenas quantidades de zircónio, háfnio ou escândio a estas ligas melhora acentuadamente a sua resistência. O alumínio em si tem uma vasta gama de utilizações, desde a construção de aviões especializados até artigos do dia-a-dia, como facas e garfos. Alguns dos usos estão listados na tabela abaixo.
|
Use |
Description |
|---|---|
|
Building and construction |
Cladding, doors, window frames, awnings and bridge rails as aluminium is strong, light, easily shaped and resistant to rust. |
|
Transport |
Parts for cars, trucks, buses, aircraft, ships, rail and trams as aluminium is strong, light, easily shaped and resistant to rust. |
|
Appliances |
Fridges, washing machines, lawn mowers etc. due to its strength, malleability and rust resistance. |
|
Heating and ventilation |
Heating and cooling systems as aluminium is a good conductor of heat. |
|
Packaging |
Kitchen foil, packaging foil, cans and containers (worldwide, four out of every five drink cans are made of aluminium) as aluminium can be rolled into very thin sheets and is non-toxic. |
|
Electrical and communications |
Power transmission including towers, electrical conduits, superconductors, machinery and equipment, telephone cables and capacitors because of aluminium’s ability to conduct electricity. |
|
Other |
Utensils (cutlery, pans), industrial machinery, chemical industry, production of steel, antiperspirants, furniture, reflectors in telescopes, making high octane petrol, road signs, antacids and jewellery due to its many useful properties. |
History
Around 5300 BC: The Persians made extra strong pots from clay containing aluminium oxide.
Around 2000 BC: The ancient Egyptians and Babylonians used potassium aluminium sulphate KAl(SO4)2 as a medicine to reduce bleeding. It was sourced from naturally occurring deposits in Greece and Turkey. The ancient Romans called this medical compound “alum”, which is where we get the modern day word and symbol from. Ainda hoje é usado para parar a hemorragia.
Idade Média: A maioria do alúmen veio do território papal de Tolfa, mas o preço caiu dramaticamente quando um grande depósito de xisto de alúmen foi descoberto em Yorkshire, no início do século XVI. Durante os séculos seguintes, o alúmen foi usado em duas áreas principais: como conservante de papel e como agente fixador de tecidos para tingir.
1808: O inglês Sir Humphry Davy tentou extrair alumínio através de electrólise. Ele falhou mas estabeleceu sua existência e lhe deu seu nome.
1821: o geólogo francês Pierre Berthier descobriu um material rico em alumínio perto da vila de Les Baux, na Provença, França. Recebeu o nome de bauxita em homenagem à aldeia.
1825: Hans Christian Oersted na Dinamarca produziu alumínio impuro ao aquecer cloreto de alumínio com amálgama de potássio.
1827: o químico alemão Friedrich Wöhler extraiu alumínio em pó ao reagir ao potássio com cloreto de alumínio anidro melhorando o processo de Oersted.
1855: o químico alemão Friedrich Wöhler extraiu alumínio em pó ao reagir ao potássio com cloreto de alumínio anidro melhorando o processo de Oersted.
O químico francês Henri Saint-Claire Deville conseguiu obter uma barra sólida de alumínio usando sódio em vez do mais caro potássio. A barra de alumínio foi considerada tão preciosa que foi exposta nesse mesmo ano ao lado das jóias da coroa francesa.
1886: Dois cientistas em continentes separados (Charles Hall na América e Paul Heroult na França) descobriram independentemente um método económico para produzir alumínio através de electrólise em criolite fundida (fluoreto de alumínio sódico). A propósito, ambos nasceram em 1864 e ambos morreram em 1914.
1887: O químico austríaco Karl Josef Bayer a trabalhar na Rússia desenvolveu um método para extrair alumina da bauxite.
1888: Hall fundou a Pittsburgh Reduction Company (conhecida como Alcoa desde 1907).
1890: As descobertas Hall-Heroult e Bayer fizeram o preço do alumínio despencar 80%. Em 1888, o alumínio custou US$4,86 por libra. Em 1893, era de US$0,78 por libra e no final da década de 1930 custava apenas US$0,20 por libra e tinha mais de 2000 usos.
1900: Apenas 8000 toneladas de alumínio foram produzidas, mas 100 anos depois foram produzidas 24,5 milhões de toneladas e em 2016 foram produzidas cerca de 57,6 milhões de toneladas.

O avião de caça F-16 foi concebido para ser relativamente barato de construir e mais simples de manter do que os caças da geração anterior. A estrutura é construída com cerca de 80% de ligas de alumínio de qualidade aeronáutica, 8% de aço, 3% de compostos e 1,5% de titânio. Fonte: Wikimedia Commons, Mestre Sgt. Andy Dunaway
1911: O químico alemão Alfred Wilm desenvolveu importantes ligas de alumínio que eram sólidas o suficiente para a fabricação de itens como aeronaves. Houve grande demanda por alumínio durante a Segunda Guerra Mundial e a Guerra da Coréia, pois os aviões tinham sido feitos anteriormente de madeira e tecido.
1922: Foi fabricada folha de alumínio.
1955: A primeira fundição de alumínio na Austrália foi aberta em Bell Bay, Tasmânia.
1958: Foram produzidas latas de refrigerantes de alumínio pela primeira vez.
1961: A Alcoa forma a Alcoa da Austrália.
1963: A Alcoa da Austrália abre a primeira refinaria de alumina na Austrália em Kwinana, na Austrália Ocidental, seguida por Pinjarra em 1972 e Wagerup em 1984.
Today: Em 2016 foram produzidas cerca de 57,6 milhões de toneladas de alumínio. Isto é mais do que todos os outros metais não ferrosos combinados. A Austrália minera bauxita em Queensland, Oeste da Austrália, Território do Norte e Tasmânia e é o maior produtor mundial de bauxita. A Austrália é também um líder mundial na produção de alumina e alumínio. As três refinarias da Austrália Ocidental fornecem 45% da alumina da Austrália e 11% do total global, tornando-as a maior fonte única de alumina do mundo.
Formação

Bauxita Weipa, R30128. Fonte: Geoscience Australia.
Bauxite é o minério de alumínio mais comum. A bauxita ocorre como uma cobertura ou manta desgastada, conhecida como laterite ou duricrust, sobre uma variedade de rochas com alumina. Ela se forma quando grandes quantidades de chuva derramam os elementos mais móveis na rocha hospedeira, deixando o alumínio relativamente imóvel com algum silício, ferro e titânio. Devido à forma como se forma, os depósitos de bauxite podem ser muito extensos e são encontrados em quase todos os continentes.
Os principais minerais de alumínio na bauxite são gibbsite , boehmite e diáspora, que é um polimorfo (forma alternativa) de boehmite mas é mais denso e duro. A alumina pura (Al2O3) contém 52,9% de alumínio e 47,1% de oxigénio. A bauxita pode ser muito dura ou tão mole como a lama e pode ocorrer como terra compactada (tanto friável como re-cimentada), pequenas bolas (pisólitos), ou material oco, semelhante a galhos (túbulos). As suas cores podem ser polpa, rosa, amarelo, vermelho ou branco, ou qualquer combinação destas. O alumínio também está presente em muitas pedras preciosas como turquesa, rubis, safiras, esmeraldas, topázio, jade e água-marinha.
Recursos
O minério de bauxita contém níveis suficientemente altos de óxidos de alumínio e níveis adequadamente baixos de óxido de ferro (Fe2O3) e sílica (SiO2) para ser economicamente extraível. A quantidade de sílica reativa é particularmente importante, pois esta forma de sílica consome a soda cáustica necessária para produzir alumina, portanto, é desejável uma sílica reativa baixa. Outras fontes potenciais de alumínio incluem uma variedade de rochas e minerais como xisto aluminoso e ardósia, rocha fosfática de alumínio e argilas de alta alcatrão.
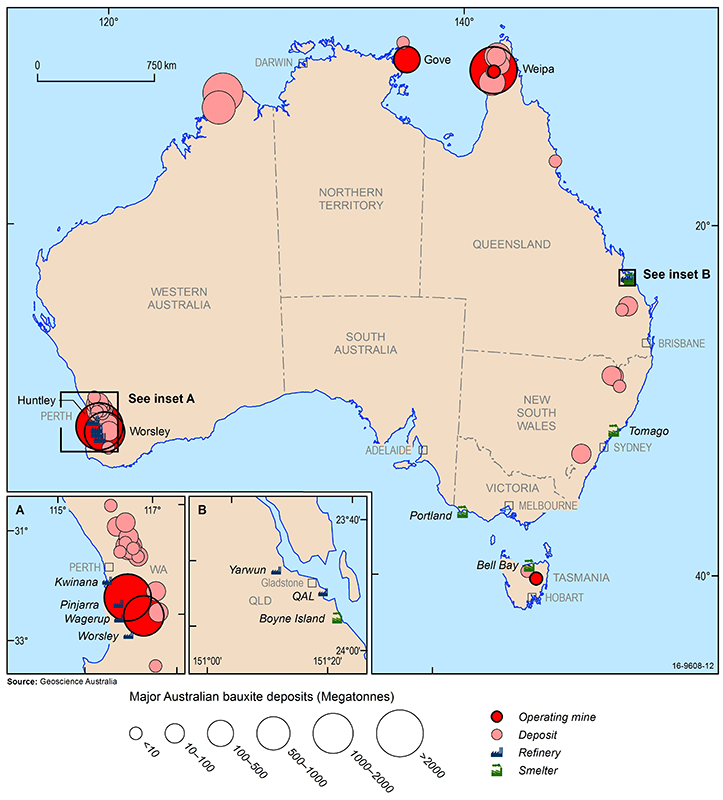
Os principais depósitos de bauxita da Austrália, minas, refinarias de alumina e fundições de alumínio (2016). Source: Geoscience Australia.
Os maiores recursos econômicos de bauxita do mundo ocorrem na Guiné, Austrália, Brasil, Vietnã e Jamaica. Na Austrália, a bauxita é extraída de operações a céu aberto estabelecidas em Weipa em Queensland, Gove no Território do Norte e Darling Range no Oeste da Austrália. Além disso, novas minas começaram recentemente a operar na região de Cape York em Queensland e no centro da Tasmânia. Outros depósitos de bauxita ocorrem no norte oeste da Austrália, Nova Gales do Sul e leste de Queensland, mas atualmente não são econômicos para se extrair.
As refinarias de alumina da Austrália estão localizadas no oeste da Austrália (Kwinana, Wagerup, Pinjarra e Worsely) e Queensland (QAL e Yarwun) e suas fundições de alumínio estão localizadas na Tasmânia (Bell Bay), Queensland (Boyne Island), Victoria (Portland) e Nova Gales do Sul (Tomago). A China é o maior consumidor mundial de alumínio e, apesar da forte produção interna, importa grandes quantidades de alumina e bauxita bruta, representando mais de 40% do consumo global. Outros grandes mercados de alumínio são os Estados Unidos da América, Japão e Europa, mas estas regiões possuem poucos depósitos econômicos de bauxita e também dependem das importações de bauxita e alumina para suas refinarias de alumina e fundições de alumínio.
Outras informações sobre recursos e produção.
Mineração
Extração de metal de alumínio ocorre em três etapas principais¿mina de minério de bauxita, refinando o minério para recuperar alumina e fundindo alumina para produzir alumínio. A bauxita é extraída por métodos de superfície (mineração a céu aberto) nos quais o solo superficial e a sobrecarga são removidos por bulldozers e raspadores. A camada superficial do solo é então armazenada e posteriormente utilizada para revegetar e restaurar a área após a conclusão da mineração. A bauxita subjacente é minerada por carregadeiras frontais, pás elétricas ou escavadeiras hidráulicas. Alguns minérios de bauxita são simplesmente triturados, secos e enviados. Outra bauxita é tratada após a britagem por lavagem para remover alguma da argila, sílica reativa e resíduos de areia; e depois é seca em fornos rotativos. O minério é carregado em caminhões, vagões ferroviários ou em correias transportadoras e transportado para navios ou refinarias.
Uma série de factores no ciclo de produção do alumínio estão relacionados com o ambiente e são atribuídos recursos consideráveis para minimizar o impacto da exploração mineira, da refinação e da fundição no ambiente circundante. A reabilitação da mina é realizada, fazendo todo o esforço para devolver a área, pelo menos, ao seu estado original. É tomado cuidado com o manuseamento e eliminação da lama vermelha das refinarias. Esta lama é normalmente bombeada para represas que são seladas com material impermeável para evitar a poluição do meio rural circundante.
Processamento
Em quase todas as operações comerciais, a alumina é extraída da bauxita pelo processo de refinação da Bayer. O processo, descoberto por Karl Josef Bayer em 1888, consiste em quatro etapas.
Digestão: a bauxita finamente moída é introduzida numa unidade aquecida por vapor chamada digestor. Aqui ela é misturada, sob pressão, com uma solução quente de soda cáustica. O óxido de alumínio da bauxita (e a sílica reativa) reage com a soda cáustica formando uma solução de aluminato de sódio ou licor verde e um precipitado de silicato de sódio e alumínio.
Clarificação: o licor verde ou solução de alumina é separado dos resíduos¿ os óxidos de ferro e sílica não dissolvidos que faziam parte da bauxita original e agora compõem os resíduos de areia e lama vermelha. Esta etapa envolve três etapas: em primeiro lugar, os resíduos do tamanho da areia grossa são removidos e lavados para recuperar a soda cáustica; em segundo lugar, a lama vermelha é separada; e, finalmente, o licor verde restante é bombeado através de filtros para remover quaisquer impurezas residuais. A areia e a lama são bombeadas juntas para lagos de resíduos e o licor verde é bombeado para trocadores de calor onde é resfriado de 1000°C a cerca de 650-790°C.
Precipitação: a alumina é precipitada do licor como cristais de hidrato de alumina. Para isto, a solução de licor verde é misturada em vasos de precipitação altos com pequenas quantidades de alumina cristalina fina, o que estimula a precipitação de hidrato de alumina sólido à medida que a solução esfria. Quando concluído, o hidrato de alumina sólido é passado para a etapa seguinte e o licor remanescente, que contém soda cáustica e alguma alumina, volta para os digestores.
Calcinação: o hidrato de alumina é lavado para remover qualquer licor remanescente e, em seguida, seco. Finalmente, ele é aquecido a cerca de 1000°C para remover a água de cristalização, deixando a alumina – um material branco puro, seco e arenoso. Uma parte da alumina pode ser deixada na forma de hidrato ou processada posteriormente para a indústria química.
Alumina é transformada em alumínio através de um processo de fundição. Toda a produção comercial de alumínio é baseada no processo de fundição Hall-Héroult, no qual o alumínio e o oxigênio na alumina são separados por eletrólise. A eletrólise envolve a passagem de uma corrente elétrica através de uma solução fundida de alumina e criolita natural ou sintética (fluoreto de alumínio sódico). A solução derretida está contida em células de redução ou potes que são revestidos no fundo com carbono (o cátodo) e são conectados em uma série elétrica chamada potline. Inseridos na parte superior de cada vaso estão os ânodos de carbono, cujos fundos estão imersos na solução fundida.
A passagem de uma corrente elétrica faz com que o oxigênio da alumina se combine com o carbono do ânodo formando o gás dióxido de carbono. O restante alumínio metálico fundido acumula-se no cátodo no fundo do pote. Periodicamente, ele é sifonado e transferido para grandes fornos de espera. As impurezas são removidas, os elementos de liga são adicionados e o alumínio fundido é fundido em lingotes.
O processo de fundição é contínuo. Como o teor de alumina do banho de criolita é reduzido, mais é adicionado. O calor gerado pela passagem da corrente elétrica mantém o banho de criolita em seu estado fundido, de modo que ele dissolva a alumina. Uma grande quantidade de energia é consumida durante o processo de fundição; de 14.000 – 16.000 quilowatts-hora de energia elétrica é necessária para produzir uma tonelada de alumínio a partir de cerca de duas toneladas de alumina. O alumínio é por vezes referido como “electricidade sólida” devido à grande quantidade de energia utilizada na sua produção. A disponibilidade de eletricidade barata é, portanto, essencial para a produção econômica.
Os lingotes de alumínio são produzidos em várias formas e tamanhos, dependendo do seu uso final. Eles podem ser enrolados em chapa, folha, folha, barras ou varetas. Eles podem ser estirados em fios que são encalhados em cabos para linhas de transmissão elétrica. As prensas extrudam os lingotes em centenas de diferentes formas úteis e decorativas ou plantas de fabricação podem convertê-los em grandes formas estruturais.