Como funciona a bateria de um carro e como é construída?
A função tradicional da bateria no compartimento do motor é bem conhecida: Sem a bateria, o veículo não pode arrancar. Para além do motor de arranque, as velas, velas de incandescência, luzes e aplicações electrónicas requerem, todas elas, energia eléctrica. Mas como é construída uma bateria e como funciona?
h2>Bateria de chumbo-ácido: Componentes e estrutura
Muitos condutores tomam consciência do peso pesado das baterias de automóveis quando compram uma nova. Pesos de cerca de 10,5 kg, até 30 kg são possíveis. A razão para isso são as placas de chumbo nas células da bateria.
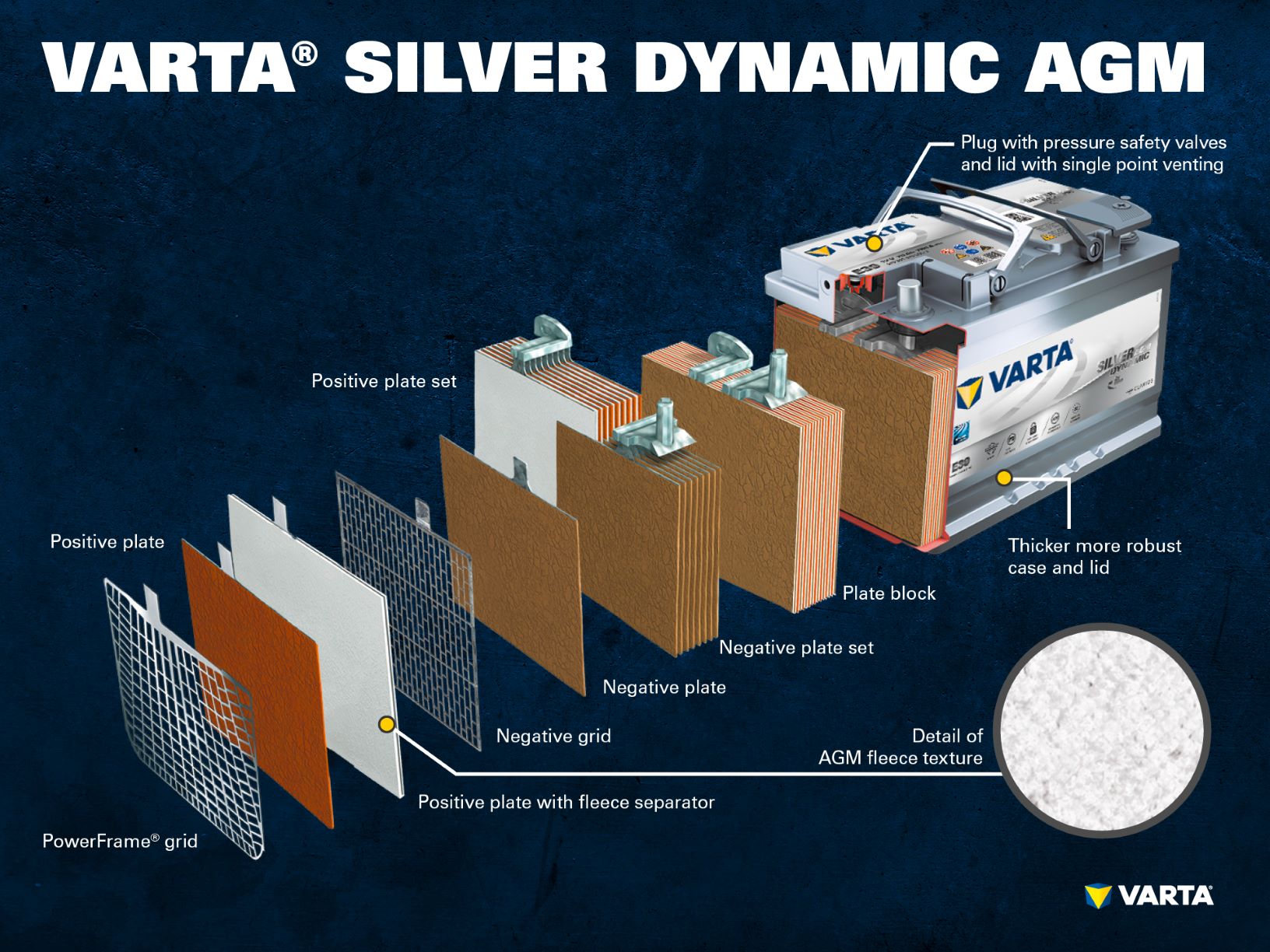
Componentes e estrutura de uma célula de bateria
eletrodo positivo:
- Placa positiva: Em uma bateria de chumbo-ácido, a placa com carga positiva (material ativo) consiste de óxido de chumbo (PbO2) que está imerso em um eletrólito.
- Grelha Positiva: A grelha positiva consiste numa liga de chumbo e é utilizada para manter o material activo e como colector de corrente.
Eléctrodo negativo:
- Placa negativa: A placa com carga negativa (material activo) consiste em chumbo puro (Pb), que também está imerso num electrólito.
- Placa negativa: Tal como a placa positiva, esta também consiste numa liga de chumbo e serve a mesma finalidade.
Os eléctrodos com cargas diferentes são separados por um saco separador.
O electrólito é uma mistura de ácido sulfúrico (H2SO4) e água destilada. Este eletrólito pode ser na forma líquida (como em baterias úmidas convencionais ou na tecnologia EFB aprimorada), na forma de gel, ou encadernado em um tapete de vidro (como na tecnologia AGM para novas aplicações start-stop).
Eléctrodos transversais positivos formam um conjunto de placas positivas e vários eletrodos negativos formam um conjunto de placas negativas. Juntos, um conjunto de placas negativas e um conjunto de placas positivas formam um bloco de placas. Um bloco de placas é uma célula de bateria.
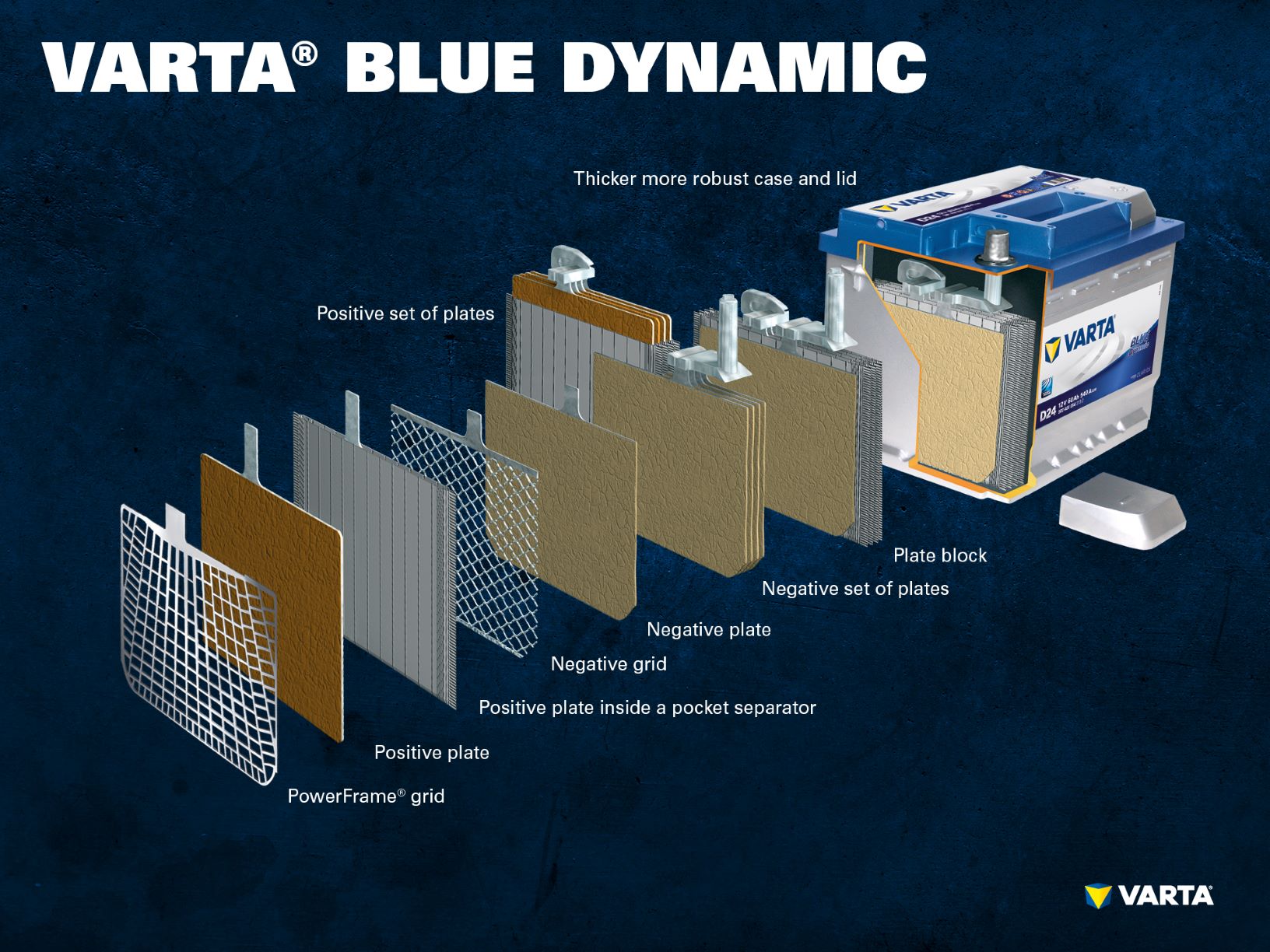
Uma bateria de arranque convencional consiste em 6 células ligadas em série, cada uma com uma tensão nominal de 2 V, o que resulta numa tensão de exactamente 12,72 V quando a bateria está totalmente carregada. A capacidade e a capacidade de arranque a frio da bateria resulta do número de placas por célula.
P>Regra de polegar: Quanto mais placas uma célula contém, e portanto forma uma superfície maior, maior é a potência de arranque a frio (CCA) que a bateria pode fornecer. No entanto, se o espaço na célula for utilizado para menos placas, mas mais espessas, a estabilidade do ciclo é aumentada. Isto significa que a bateria é projetada para um maior rendimento de carga (processo contínuo de carga e descarga).
As células estão contidas em um invólucro que é feito de plástico resistente a ácidos (polipropileno). Numa bateria SLI convencional, esta é fechada com uma tampa com um sistema de labirinto que impede a fuga do líquido da bateria e separa o líquido do gás.
As baterias eléctricas tinham tampas de rosca que permitiam a sua recarga com água destilada. As baterias modernas são completamente isentas de manutenção. A água não precisa de ser, nem deve ser reabastecida. Embora as baterias AGM ainda tenham “fichas de um só sentido”, estas não devem ser abertas em circunstância alguma.
Função da bateria do automóvel: A energia química torna-se energia eléctrica
Uma bateria de automóvel armazena energia na forma química e converte-a em energia eléctrica. Neste processo electroquímico, quatro materiais reagem entre si:
- Hidrogénio (H)
- Oxigénio (O2)
- Lead (Pb)
- Sulfur (S)
A ligação de um consumidor externo inicia a reacção química na bateria:
- O electrólito, uma mistura de ácido sulfúrico (H2SO4) e água destilada decompõe-se em iões de hidrogénio com carga positiva (H+) e iões de sulfato com carga negativa (SO42-).
- Ao mesmo tempo, os elétrons (2e-) viajam do negativo para o positivo através do consumidor externo.
- Para compensar este fluxo de elétrons, os íons sulfato viajam do eletrólito para o negativo, onde reagem com o chumbo (PbSO4) para produzir sulfato de chumbo (PbSO4).
- Sulfato de chumbo também é produzido no eletrodo positivo: A ligação do oxigênio (O2) no óxido de chumbo (PbO2) é quebrada pela transferência de elétrons e o oxigênio passa para o eletrólito. O chumbo restante (Pb) liga-se com o sulfato (SO4) do eletrólito.
li>There, o oxigênio liga-se com o hidrogênio para formar água (H2O). Como o ácido sulfúrico é utilizado pela formação do sulfato de chumbo, a concentração da solução electrolítica diminui. Quando a concentração do ácido sulfúrico cai abaixo de um certo nível, a bateria tem que ser recarregada.li>Durante a carga, os processos químicos acontecem na sequência inversa. No final, os elementos originais podem ser encontrados: O eletrodo positivo consiste de sulfato de chumbo (PbSO4), o negativo consiste de chumbo puro (Pb) e o eletrólito consiste de ácido sulfúrico diluído (H2SO4). Como este processo de conversão está associado a perdas, uma bateria só pode resistir a um número limitado de ciclos de carga. A sua vida útil é portanto limitada. 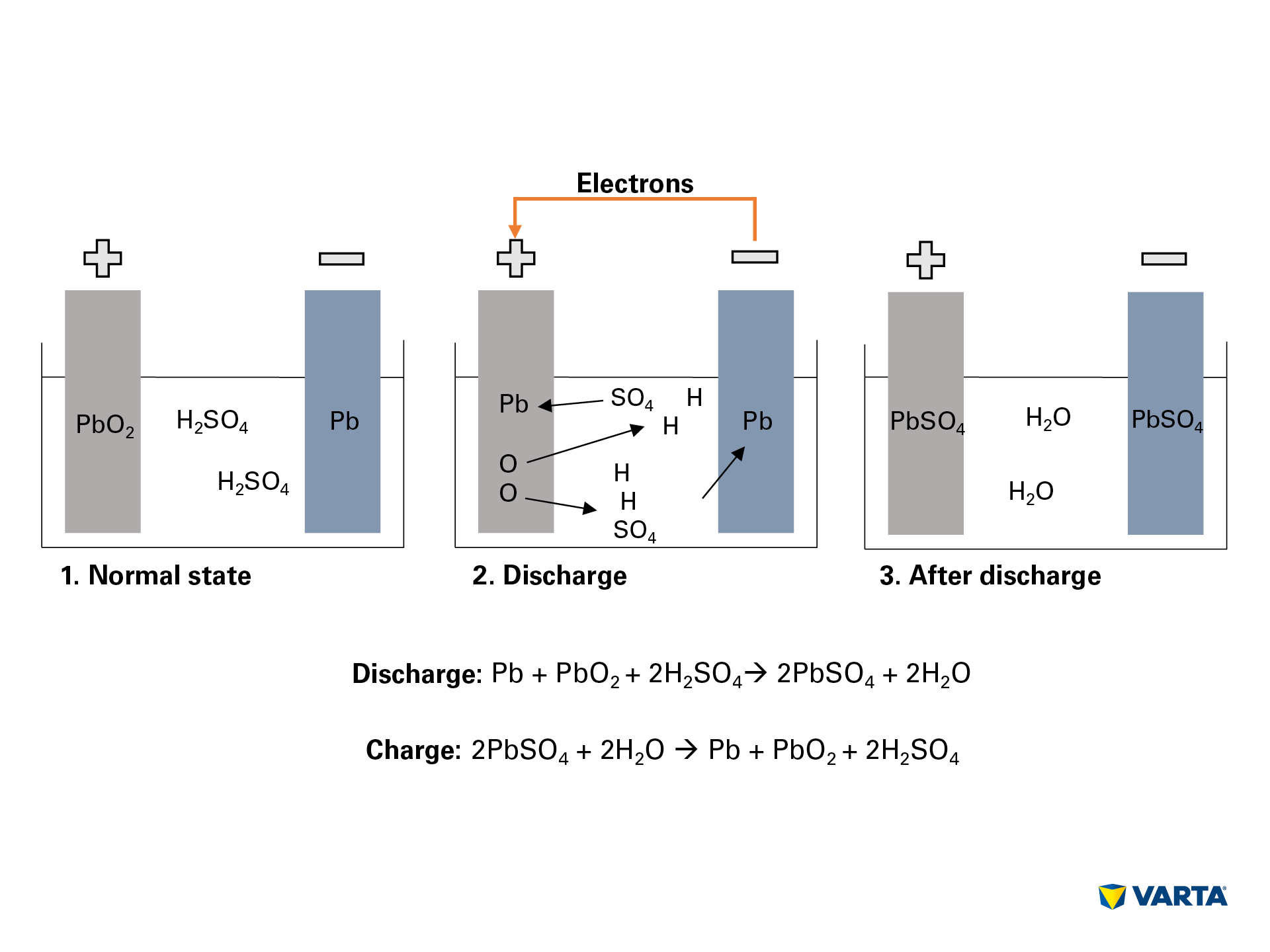
Problemas com baterias de chumbo-ácido: Sulfation and acid layering
Se uma bateria for carregada com uma tensão demasiado baixa, ou se funcionar sempre com uma tensão demasiado baixa (abaixo de 80%), também referida como estratificação, ocorre uma estratificação. O ácido no electrólito estratifica devido a uma má mistura. Várias densidades causam estratificação do ácido sulfúrico na parte inferior e da água na área superior da bateria. Devido a isso, apenas a seção do meio do eletrólito, ou seja, apenas um terço, pode ser utilizado para o processo de descarga e carga.
Uma possível causa da estratificação do ácido é principalmente viagens curtas com o uso simultâneo de um grande número de consumidores elétricos. Neste caso, o alternador não dispõe de tempo suficiente para recarregar a bateria. 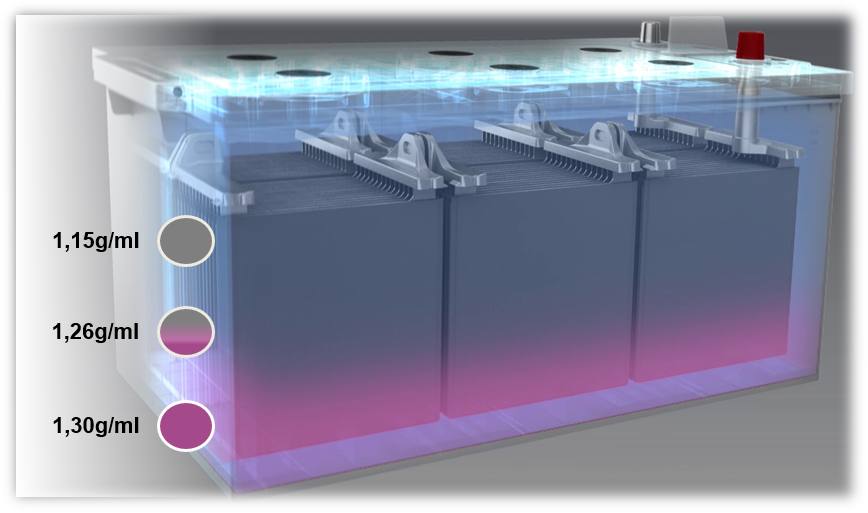
Um resultado de sobreposição ácida é a sulfatação. Se isto ocorrer na bateria, ou se não estiver constantemente carregada a um nível adequado, o sulfato de chumbo (PbSO4) cristaliza nos eléctrodos, para formar estruturas cristalinas maiores ao longo do tempo. Este processo é conhecido como “sulfatação”. A cristalização evita a reconversão do sulfato de chumbo nos componentes originais chumbo ou óxido de chumbo, o que resulta na prevenção da aceitação da carga e redução da potência de arranque a frio.
Cristais de chumbo também podem danificar os separadores ou causar curto-circuitos nas células.
Para contrariar este efeito e evitar a falha prematura da bateria, uma bateria nunca deve ser sujeita a um nível de carga baixo durante um longo período. Para isso, é aconselhável testar a bateria regularmente e carregá-la completamente se necessário.
Deseja saber mais sobre este tópico? Como carregar correctamente uma bateria.
Novas tecnologias de bateria: AGM e íon de lítio
Até agora, as baterias convencionais de chumbo-ácido têm tido uma elevada quota de mercado. No entanto, o mercado está a mudar rapidamente: Tecnologias inovadoras de baterias para veículos start-stop como o AGM utilizam ácido que é ligado num tapete para proporcionar maior estabilidade de ciclo e garantir um desempenho fiável em veículos com maiores necessidades energéticas. Uma outra vantagem do AGM: A camada de ácido não é mais possível devido ao ácido ligado.
Uma nova geração de baterias para veículos micro-híbridos funciona a 48V e utiliza células com tecnologia de iões de lítio.