Doença de Lyme
Visão geral
O primeiro caso de anaplasmose humana foi descrito em 1990, quando um paciente de Wisconsin desenvolveu uma doença febril grave após uma picada de carraça e morreu duas semanas depois. Esfregaços de sangue revelaram grupos de bactérias dentro dos neutrófilos do paciente, semelhantes às mórulas observadas em monócitos com infecção por E. chaffeensis. Contudo, as culturas e testes serológicos para E. chaffeensis foram negativos. Entretanto, o curso clínico do paciente sugeriu algum tipo de ehrlichiosis, e quando vários casos adicionais da doença foram relatados no Midwest do norte nos anos seguintes, foi postulado que uma nova espécie de Ehrlichia poderia estar emergindo. A nova doença recebeu provisoriamente o nome de “ehrlichiosis granulocytic humana”, ou HGE.
Em 1994, estudos de sequenciamento de DNA revelaram que o agente HGE era claramente distinto de E. chaffeensis mas essencialmente idêntico a dois patógenos veterinários ehrlichial previamente conhecidos, E. equi e E. (Cytoecetes) phagocytophila. Sob um novo esquema taxonômico implementado desde então, estes três organismos foram unidos como uma única espécie dentro de um novo gênero, Anaplasma. A nova espécie é referida como Anaplasma phagocytophilum, e a doença que ela causa é agora conhecida como anaplasmose granulocítica humana, ou HGA.
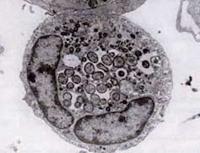
Ehrlichia species, Anaplasma organisms are small, gram-negative, and intracellular. A. phagocytophilum visa os neutrófilos, altera sua função no hospedeiro e forma mórulos dentro dos vacúolos. A maioria dos danos que causa parece estar relacionada aos processos inflamatórios do hospedeiro, pois há pouca evidência de correlação entre o número de organismos e a gravidade da doença do hospedeiro.
Anaplasmose é uma infecção global, ocorrendo na América do Norte, na maior parte da Europa e no leste da Ásia. Os carrapatos dos Ixodes persulcatus-complexos são os vetores: I. escapularis nas regiões nordeste e centro-oeste superior dos Estados Unidos; I. pacificus no Noroeste Pacífico; I. ricinus na Europa; e I. persulcatus na Ásia. A. phagocytophilum é mantido na natureza pelo ciclismo entre estes carrapatos e vários pequenos mamíferos, principalmente camundongos e outros pequenos roedores. Como os carrapatos Ixodes também são os vetores da doença de Lyme, babesiose e encefalite transmitida por carrapatos, a coinfecção por Anaplasma com essas outras doenças pode e ocorre em humanos.
Nos Estados Unidos, os casos de HGA superaram em número os da Ehrlichiosis Monocytic Human Monocytic Ehrlichiosis (HME) Semelhante à HME e ewingii ehrlichiosis humana, a idade média dos pacientes com HGA é de cerca de 50 anos.
Sinais e Sintomas
O curso clínico da HGA varia de infecção assintomática a doença fatal. Os sintomas iniciais, ocorrendo cerca de cinco a dez dias após a picada da carraça, são em grande parte inespecíficos: febre, calafrios, cefaléia severa e mialgias; j náuseas, tosse e artralgia também podem ocorrer. A erupção cutânea é incomum, mas tem sido relatada.
Comparado com a HME, a HGA parece menos provável de envolver o sistema nervoso central, mas as neuropatias periféricas (por exemplo, dormência e formigamento) são mais comuns e podem durar semanas a meses. Entre os achados neurológicos relatados na literatura médica estão a paralisia facial, a polineuropatia desmielinizante e a plexopatia braquial. A síndrome do desconforto respiratório e uma síndrome séptica ou tóxica, mas parecem ser menos comuns do que na HME. A taxa global de mortalidade por HGA é muito baixa (menos de 1%), com a maioria das mortes resultantes de infecções oportunistas (por exemplo, esofagite por herpes simples, pneumonia por Candida e aspergilose pulmonar) em pacientes imunocomprometidos.
Diagnóstico
Exames sanguíneos padrão em HGA geralmente revelam achados similares aos observados em HME: leucopenia, trombocitopenia e anormalidades da função hepática (transaminases elevadas). Entretanto, as anormalidades hematológicas freqüentemente se resolvem até a segunda semana de sintomas, portanto sua ausência deve ser interpretada nesse contexto se os pacientes estiverem se apresentando mais tarde durante o curso da doença. Em geral, o tratamento antibiótico empírico deve ser considerado para pacientes em áreas endêmicas que apresentam uma doença febril aguda sugestiva de HGA.
Para diagnóstico específico, os esfregaços de sangue de Wright ou Giemsa têm um rendimento ligeiramente maior do que com a HME, mas ainda não são ideais para utilidade clínica geral, já que parece haver uma grande variação (25-75%) na sensibilidade desses testes na visualização de mórulas nos neutrófilos do hospedeiro. Mais úteis, mas nem sempre disponíveis, são os testes de reacção em cadeia da polimerase (PCR), que se estima terem uma sensibilidade de 67-90%. A antibioticoterapia prévia reduz drasticamente a sensibilidade de ambos os métodos de diagnóstico.
Testes serológicos são úteis para confirmar o diagnóstico de anaplasmose. O método mais utilizado é a imunofluorescência indirecta (IFA) de anticorpos IgM e IgG anti-A. fagocytophilum. A seroconversão é talvez a evidência laboratorial mais sensível da infecção por A. phagocytophilum, mas nem sempre é obtida de forma suficientemente atempada para fornecer informação útil nas decisões clínicas (i.e., de tratamento).