2.3: Familiile și perioadele tabelului periodic
Familiile tabelului periodic
Amintiți-vă că Mendeleev a aranjat tabelul periodic astfel încât elementele cu cele mai asemănătoare proprietăți să fie plasate în aceeași grupă. O grupă este o coloană verticală a tabelului periodic. Toate elementele 1A au câte un electron de valență. Acesta este cel care face ca aceste elemente să reacționeze în aceleași moduri ca și ceilalți membri ai familiei. Elementele din 1A sunt toate foarte reactive și formează compuși în aceleași proporții și cu proprietăți similare cu alte elemente. Datorită similitudinilor în ceea ce privește proprietățile lor chimice, Mendeleev a pus aceste elemente în același grup. Grupul 1A este cunoscut și sub numele de metale alcaline. Deși majoritatea metalelor tind să fie foarte dure, aceste metale sunt de fapt moi și pot fi tăiate cu ușurință.
Grupa 2A se mai numește și metale alcalino-pământoase. Încă o dată, din cauza asemănărilor în configurațiile electronice, aceste elemente au proprietăți similare între ele. Același model este valabil și pentru alte grupe din tabelul periodic. Amintiți-vă, Mendeleev a aranjat tabelul astfel încât elementele cu cele mai asemănătoare proprietăți să se afle în aceeași grupă din tabelul periodic.
Este important să recunoaștem câteva alte grupe importante din tabelul periodic după numele lor de grup. Elementele din grupa 7A (sau 17) sunt, de asemenea, numite halogeni. Această grupă conține elemente nemetalice foarte reactive.
Gazele nobile se află în grupa 8A. Aceste elemente au, de asemenea, proprietăți similare între ele, cea mai semnificativă proprietate fiind aceea că sunt extrem de puțin reactive, formând rareori compuși. Vom afla motivul pentru acest lucru mai târziu, când vom discuta despre cum se formează compușii. Elementele din această grupă sunt, de asemenea, gaze la temperatura camerei.
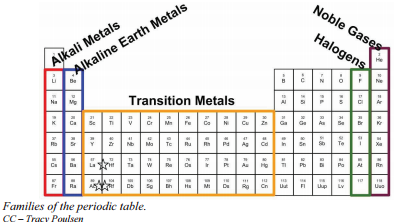
Un sistem alternativ de numerotare numerotează toate elementele din blocurile \(s\), \(p\) și \(d\) de la 1 la 18. În acest sistem de numerotare, grupul 1A este grupul 1; grupul 2A este grupul 2; halogenii (7A) sunt grupul 17; iar gazele nobile (8A) sunt grupul 18. Veți întâlni tabele periodice cu ambele sisteme de numerotare. Este important să recunoașteți care sistem de numerotare este utilizat și să puteți găsi numărul de electroni de valență în elementele din blocul principal, indiferent de sistemul de numerotare utilizat.
.