Adipocitele
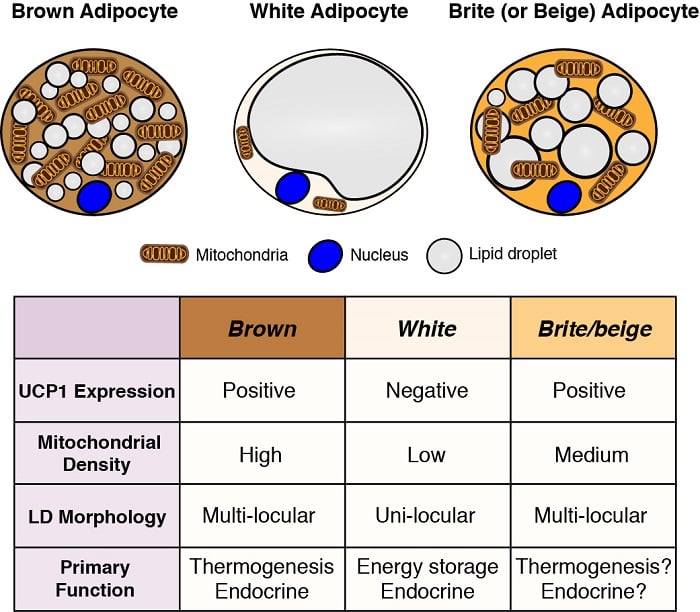
Adipocitele sunt principalele locuri de stocare a energiei din organism și au, de asemenea, funcții endocrine esențiale. Prin urmare, înțelegerea dezvoltării și funcției adipocitelor – în special în lumina pandemiei de obezitate – este esențială pentru a înțelege homeostazia metabolică. Există două clase generale de adipocite: adipocitele albe – care stochează energia sub forma unei singure picături mari de lipide și au funcții endocrine importante, și adipocitele brune – care stochează energia în mai multe picături mici de lipide, dar în mod special pentru a fi utilizate drept combustibil pentru a genera căldură corporală (adică termogeneză). Producerea de căldură de către adipocitele brune este posibilă datorită expresiei unice a proteinei de decuplare 1 (Ucp1) localizată la nivel mitocondrial. Cu toate acestea, aceste clasificări sunt prea simplificate, deoarece unele adipocite albe pot adopta caracteristici de adipocite brune (denumite adipocite brite sau bej) și viceversa, în funcție de temperatură și de regimul alimentar. Suntem interesați să înțelegem originile diferitelor adipocite și să definim căile de semnalizare și metabolice care controlează dezvoltarea, distribuția și funcția acestora.
Originea adipocitelor
Centrală pentru înțelegerea rolului țesutului adipos în sănătate și boală este înțelegerea modului în care acesta crește și, în acest sens, unul dintre cele mai puțin înțelese domenii ale biologiei țesutului adipos este originea de dezvoltare a diferitelor tipuri de adipocite. Definirea originii adipocitelor ar putea ajuta la explicarea modelelor de distribuție a grăsimii corporale umane, în special la persoanele obeze sau lipodistrofice, și ar putea oferi indicii cu privire la diferențele metabolice observate între anumite depozite de grăsime. Identificarea celulelor precursoare ale adipocitelor și a mecanismelor care le reglează expansiunea este, de asemenea, esențială pentru înțelegerea și gestionarea funcției sănătoase a țesutului adipos. De asemenea, ar putea fi posibilă dezvoltarea inginerească a adipocitelor „sănătoase” (cum ar fi adipocitele brune sau brite/beige) din precursori pentru terapiile pe bază de celule care vizează, în esență, combaterea grăsimii cu grăsime. Cu ajutorul unei combinații de strategii genetice și de urmărire a liniei, am cartografiat anterior originile adipocitelor care rezidă în diferite depozite. Rezultatele noastre relevă un nivel neașteptat de eterogenitate în concordanță cu faptul că adipocitele au origini multiple de dezvoltare și susțin un model în care soarta adipocitelor depinde probabil atât de factori extrinseci, cât și de factori intrinseci.
Adipocitele au origini multiple de dezvoltare
(jos, stânga) Distribuția anatomică a depozitelor de țesut adipos la un șoarece. Sunt reprezentați depozitele de țesut adipos brun (BAT) și de țesut adipos alb (WAT). (dedesubt, la dreapta) Un exemplu de experiment de urmărire a liniei de dezvoltare în timpul căruia celulele precursoare de dezvoltare și toți descendenții lor au fost marcați în mod indelebil cu un marcaj fluorescent legat de expresia Myf5 (panoul a) sau Pax3 (panoul b). Adipocitele marcate în verde (mGFP) provin dintr-o celulă precursoare diferită de adipocitele marcate în roșu (mTFP).
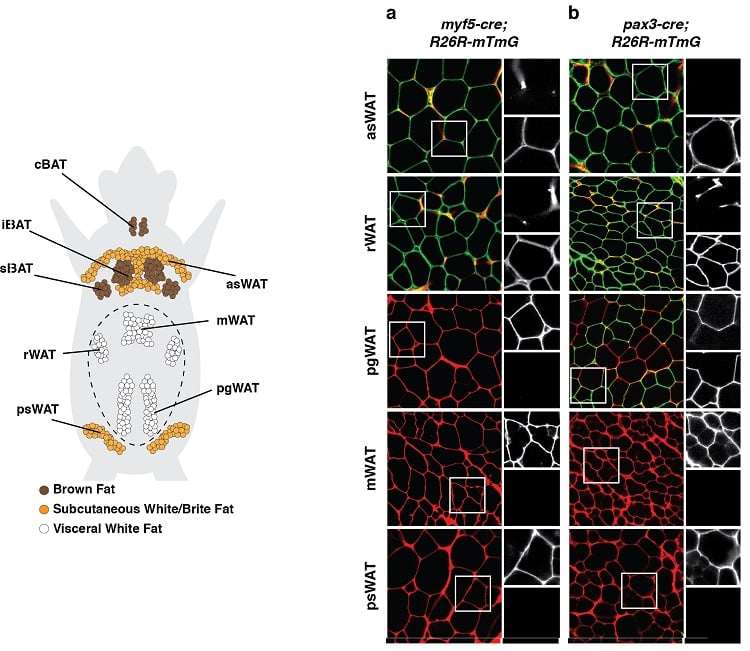
Rezultate precum acestea sugerează că adipocitele au origini multiple de dezvoltare.
(adaptat după Sanchez-Gurmaches & Guertin, Nature Communications 2014; Sanchez-Gurmaches et al., Trends in Cell Biology 2016)
Adipocitele brune
Adipocitele brune sunt celule fascinante. Ele există doar la mamifere, iar principala lor funcție este aceea de a genera căldură endogenă într-un proces numit termogeneză. Acest lucru este posibil datorită expresiei lor unice a unei proteine de membrană mitocondrială numită proteină de decuplare 1 (UCP1). Proprietățile de consum de energie ale grăsimii brune și constatarea recentă a faptului că oamenii adulți au grăsime brună au făcut din acestea o țintă pentru terapiile menite să combată supraalimentarea. Adipocitele brune active au, de asemenea, unul dintre cele mai intrigante programe metabolice: ele absorb și consumă simultan cantități mari de nutrienți diverși (de exemplu, glucoză, lipide, aminoacizi) și pot angaja simultan atât metabolismul anabolic, cât și cel catabolic. De exemplu, noi și alții am arătat anterior că BAT stimulată la rece stimulează pe scară largă un program genetic care susține căile de sinteză de novo a lipidelor în plus față de căile de oxidare a acizilor grași . Am dori să înțelegem mai multe despre acest metabolism remarcabil și paradoxal.
Învățați mai multe despre dezvoltarea și metabolismul țesutului adipos brun
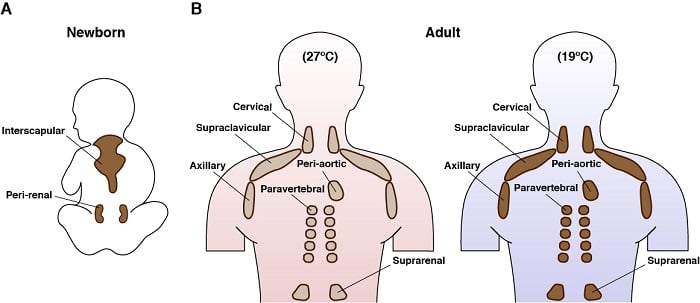
Localizarea anatomică a grăsimii brune la om
De asemenea, folosim modele genetice pentru a investiga modul în care căile de semnalizare controlează metabolismul BAT. De exemplu, folosind șoareci, am eliminat genetic Rictor – care codifică o componentă unică și esențială a mTORC2 – numai în țesutul adipos brun. Aflați mai multe despre mTORC2. În mod remarcabil, acești șoareci sunt protejați de o dietă bogată în grăsimi. Mai precis, șoarecii lipsiți de BAT Rictor nu au acumulat lipide excesive în ficat sau în depozitele de țesut adipos visceral atunci când au consumat dieta bogată în grăsimi . Aceasta este o constatare interesantă, deoarece depozitarea excesivă a lipidelor în aceste locuri este periculos de nesănătoasă. Folosind o combinație de genetică, genomică, metabolomică și biochimie, încercăm să înțelegem de ce acești șoareci sunt protejați de dieta bogată în grăsimi.
Adipocitele albe
Adipocitele albe sunt cele mai abundente adipocite la om. Depozitele de țesut adipos alb au, de asemenea, o capacitate remarcabilă de a se extinde și de a stoca energie și transmit semnale către creier și alte țesuturi pentru a influența puternic comportamentul alimentar și homeostazia metabolică. Cu toate acestea, în timp ce adipocitele albe sunt adaptate în mod specific pentru a bloca în siguranță excesul de nutrienți, acestea au un punct de basculare (de exemplu, în cazul obezității) în care funcțiile lor benefice eșuează, iar acest lucru favorizează puternic apariția bolilor metabolice și a diabetului de tip 2. Ce definește punctul de basculare? Cum semnalează adipocitele albe către alte țesuturi? Cât de eterogene sunt depozitele de țesut adipos alb? De ce un exces de grăsime viscerală este mai dăunător pentru sănătate decât un exces de grăsime subcutanată? Toate acestea sunt întrebări nerezolvate care ne interesează.
Studiem, de asemenea, semnalizarea mTOR în adipocitele albe. mTOR este o țintă majoră în aval a semnalizării insulinei, care este principalul hormon la care răspund adipocitele. Folosind modele genetice de șoareci, am inhibat selectiv fie mTORC1, fie mTORC2 în toate adipocitele. Inhibarea mTORC1 în țesutul adipos alb provoacă un sindrom asemănător lipodistrofiei, asociat cu rezistența la insulină și cu boala ficatului gras. Inhibarea mTORC2 în țesutul adipos alb provoacă, de asemenea, rezistență la insulină, dar independent de modificările masei țesutului adipos. În acest din urmă model, mTORC2 pare să reglementeze un semnal derivat din adipocite care comunică cu ficatul pentru a controla producția hepatică de glucoză. Înțelegerea bazei mecaniciste a acestor fenotipuri va oferi informații critice despre modul în care căile de transducție a semnalului de detectare a nutrienților contribuie la patogeneza bolilor legate de țesutul adipos.
Model de semnalizare mTORC2 într-un adipocit alb
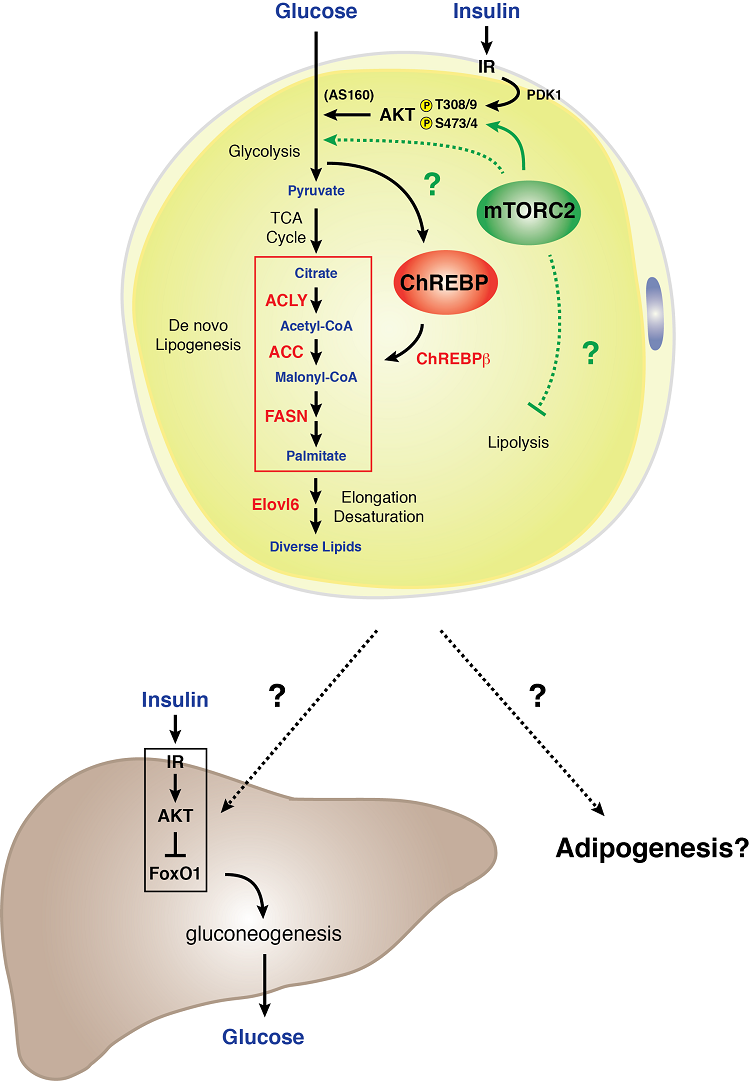 Adipocitele albe necesită mTORC2 pentru metabolismul normal al carbohidraților și lipidelor. Am constatat că pierderea genetică a Rictor (mTORC2) în mod specific în adipocitele albe reduce absorbția de glucoză și atenuează expresia factorului de transcripție ChREBP-beta și a țintelor sale din aval – care include enzimele care funcționează în calea lipogenezei de novo. În plus, o deficiență de mTORC2 în celulele adipoase albe duce la o rezistență hepatică severă la insulină. Aceste date indică faptul că mTORC2 din adipocitele albe este un regulator esențial al metabolismului carbohidraților și al lipidelor și este o componentă cheie a unui mecanism de comunicare organică extra-hepatică de detectare a nutrienților care controlează homeostazia sistemică a glucozei . Înțelegerea biologiei semnalizării mTORC2 în grăsimea albă poate deține indicii importante despre modul în care țesutul adipos alb funcționează ca un organ de detectare a glucozei și mediator al fitness-ului metabolic sistemic.
Adipocitele albe necesită mTORC2 pentru metabolismul normal al carbohidraților și lipidelor. Am constatat că pierderea genetică a Rictor (mTORC2) în mod specific în adipocitele albe reduce absorbția de glucoză și atenuează expresia factorului de transcripție ChREBP-beta și a țintelor sale din aval – care include enzimele care funcționează în calea lipogenezei de novo. În plus, o deficiență de mTORC2 în celulele adipoase albe duce la o rezistență hepatică severă la insulină. Aceste date indică faptul că mTORC2 din adipocitele albe este un regulator esențial al metabolismului carbohidraților și al lipidelor și este o componentă cheie a unui mecanism de comunicare organică extra-hepatică de detectare a nutrienților care controlează homeostazia sistemică a glucozei . Înțelegerea biologiei semnalizării mTORC2 în grăsimea albă poate deține indicii importante despre modul în care țesutul adipos alb funcționează ca un organ de detectare a glucozei și mediator al fitness-ului metabolic sistemic.