Proiecte științifice pentru începători: Chimie
Chimie
Sare sau zahăr: Care se dizolvă mai repede în diferite lichide
Soluțiile nu sunt altceva decât amestecuri de diferiți compuși sau elemente. Întâlnești soluții în fiecare zi, fără să-ți dai seama.
Chiar și aerul pe care îl respiri?care conține apă?este o soluție formată dintr-un lichid și un gaz. Dacă ați băut astăzi un suc, ați băut de fapt soluția unui gaz dizolvat în apă aromatizată. Dacă purtați o brățară făcută din argint, purtați o soluție din două metale.
În acest experiment, veți lucra cu o soluție lichidă, care este unul dintre cele trei tipuri de soluții. Celelalte tipuri sunt soluțiile gazoase și soluțiile solide.
Care pare să fie problema?
Un solut este substanța?fie solidă, lichidă sau gazoasă?care se dizolvă. Un solvent?care poate fi, de asemenea, un solid, un lichid sau un gaz?este substanța care face dizolvarea. O soluție este un amestec uniform de un solut (de obicei un solid) dizolvat într-un solvent (de obicei un lichid).
Când amestecați o lingură de zahăr într-un pahar cu apă, formați o soluție. Acest tip de soluție lichidă este compusă dintr-un solut solid, care este zahărul, și un solvent lichid, care este apa. Pe măsură ce moleculele de zahăr se răspândesc uniform în apă, zahărul se dizolvă.
Mixarea unui lichid într-un gaz formează un alt tip de soluție, numită soluție gazoasă. Un exemplu de acest tip de soluție este umiditatea. Umiditatea este apă (un lichid) dizolvată în aer (un gaz).
Gândiți-vă la modul în care un cub de zahăr se dizolvă în apă, în comparație cu un pachet de zahăr vrac. Cubul se dizolvă mai încet deoarece mai puține molecule de zahăr sunt inițial în contact cu apa.
Într-o soluție solidă, cum ar fi argintul, cuprul care a fost încălzit la temperaturi ridicate este amestecat cu argintul care, de asemenea, a fost încălzit până când se topește. Cuprul este solutul, adică substanța care se va dizolva în solvent. Argintul este solventul.
Tipul de soluție este determinat de starea de materie a solventului. Dacă substanța care face dizolvarea este un lichid, soluția se numește soluție lichidă. Dacă solventul este un gaz, soluția se numește soluție gazoasă. Și ați ghicit bine: Un solvent solid va forma o soluție solidă.
Puteți verifica dimensiunea cristalelor de sare și de zahăr la microscop sau la lupă, ceea ce vă va permite să le vedeți și formele. Dacă desenați ceea ce vedeți, folosind un creion, astfel încât să puteți ilustra umbrirea, ați putea include ilustrația ca parte a expunerii finale a proiectului dvs. de la concursul de științe.
Există câțiva factori care, în general, cresc cantitatea de solut care poate fi dizolvată. Dacă doriți să dizolvați mai mult zahăr în aceeași cantitate de apă, de exemplu, ați putea încălzi apa. De asemenea, ați putea măcina zahărul în particule mai mici pentru a-i mări suprafața sau ați putea amesteca amestecul.
În anii în care ați folosit sare și zahăr la alimente, ați observat, probabil, că fiecare bucată de sare?care este de fapt un cristal?este puțin mai mică decât fiecare bucată de zahăr, care este de asemenea un cristal.
O moleculă este formată din două sau mai multe elemente care sunt combinate chimic. O moleculă de sare conține sodiu și clor, care se combină chimic pentru a obține clorura de sodiu. Formula chimică pentru această sare este NaCl. O moleculă de zahăr conține carbon, hidrogen și oxigen. Formula chimică a zahărului este C12H22O11.
Problema pe care veți încerca să o rezolvați în acest experiment este dacă zahărul sau sarea se dizolvă mai repede atunci când sunt amestecate în diverse lichide. Afectează mărimea bucăților cât de repede se amestecă cu lichidul?
Când dizolvi zahărul sau sarea într-un lichid?să zicem, apă?ceea ce se întâmplă este că moleculele de zahăr se deplasează pentru a se potrivi între moleculele de apă din pahar sau pahar. Ilustrația de mai jos arată cum sunt aranjate diferitele molecule în recipient.
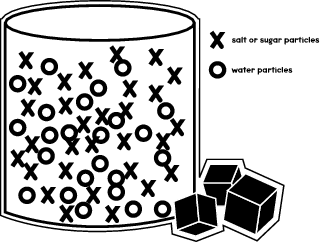
În experimentul tău, vei vedea cum moleculele de sare și de zahăr se deplasează în diferite lichide și se dizolvă cu viteze diferite.
Titlul acestei secțiuni, ?Sare sau Zahăr: Care dintre ele se dizolvă mai repede în diferite lichide?” ar putea servi ca titlu al proiectului dumneavoastră, dacă doriți. De asemenea, ați putea lua în considerare unul dintre următoarele titluri pentru proiectul dvs.:
- The Great Salt vs. Sugar Dissolving Contest
- Using Salt and Sugar to Explore How Substances Dissolve
Care nume pe care îl alegeți este bun. Haideți să luăm acum un minut pentru a considera de ce acest proiect este o utilizare valoroasă a timpului dumneavoastră.
Ce rost are?
Când există un spațiu amplu între moleculele unui solvent, se spune că solventul este nesaturat. Atunci când o cantitate mare de solut a fost dizolvată în solvent, dar există încă spațiu între molecule, soluția este concentrată. Atunci când absolut niciun solut nu mai poate fi dizolvat în cadrul unui solvent, soluția este saturată.
Și atunci când solutul în exces a fost dizolvat prin încălzirea soluției, se spune că aceasta este suprasaturată.
Scopul acestui experiment, pe lângă faptul de a învăța dacă sarea sau zahărul se dizolvă mai repede în diferite lichide, este de a învăța cum interacționează moleculele într-o soluție.
După cum ați văzut în ilustrația anterioară, moleculele de apă ocupă cea mai mare parte a spațiului din recipient. Dar mai există încă ceva spațiu disponibil în care pot încăpea moleculele de zahăr sau de sare. Prin experimentul dumneavoastră, veți afla cât de repede se potrivesc moleculele de zahăr în acele spații, în comparație cu particulele de sare.
Cunoscând acest lucru vă va ajuta să înțelegeți mai bine procesul care are loc atunci când o substanță se dizolvă.
Controlul din experimentul dumneavoastră va fi apa. Celelalte lichide în care veți dizolva sarea și zahărul vor fi variabilele.
| Controale: | Solvent?apă |
| Solvenți?zahăr, sare | |
| Variabile: | Cinci lichide limpezi diferite (pot fi colorate) |
Amintește-ți când realizezi experimentul că este foarte important ca lichidele pe care le folosești să aibă toate aceeași temperatură. Ai învățat deja că zahărul se dizolvă mai repede într-un lichid cald decât într-unul rece, așa că știi că nu ar fi un experiment corect dacă unele dintre lichidele pe care le folosești sunt calde, iar altele sunt reci. Temperatura lichidului ar deveni o variabilă.
De aceea, toate lichidele pe care le folosiți?inclusiv apa?ar trebui să fie la temperatura camerei. Dacă în mod normal le păstrați în frigider, asigurați-vă că le lăsați să stea pe tejghea peste noapte până când toate au aceeași temperatură.
Pentru a vă oferi un pic mai multă flexibilitate atunci când realizați experimentul, puteți alege lichidele în care veți dizolva zahărul și sarea. Nu are rost să trebuiască să ieșiți și să cumpărați lichide suplimentare dacă aveți deja ceea ce vă trebuie.
Nu presupuneți că lichidele care au stat în diferite zone ale casei dumneavoastră au aceeași temperatură. O sticlă de sifon care a stat în garaj, de exemplu, poate fi cu câteva grade mai rece decât alcoolul de frecat din dulapul din baie sau sucul de mere din cămara din bucătărie. Asigurați-vă că toate lichidele se află în aceeași locație pentru ca acestea să atingă aceeași temperatură ambiantă. If you don’t, the results of your experiment won’t be valid.
Just make sure you choose liquids that are different from each other in taste, color, odor, and purpose. You’ll also need to select those that allow you to observe the salt and sugar as it dissolves. If you use milk or orange juice, for example, you won’t be able to watch the salt and sugar dissolve. Some suggestions for liquids to consider are:
- White vinegar
- Club soda
- Ginger ale
- Glass cleaner (such as Windex)
- Lemonade
- Tea or iced tea (each at room temperature)
- Apple juice
- Rubbing alcohol
All of these are commonly found around the house, perhaps saving you a trip to the store.
What Do You Think Will Happen?
Acum știți cum se formează soluțiile și câțiva dintre factorii care vor afecta viteza cu care se vor dizolva zahărul și sarea pe care le veți folosi, ar trebui să puteți ghici care dintre ele se va dizolva mai repede.
Dacă nu ați mai făcut acest experiment înainte, nu veți ști dacă lichidele pe care le folosiți vor fi un factor în dizolvarea sării și a zahărului. Acest lucru face mai dificilă formularea unei ipoteze, dar nu vă faceți griji. Faptul că ipoteza dumneavoastră se dovedește a fi corectă sau nu, nu afectează validitatea sau rezultatul experimentului dumneavoastră.
În timp ce nu veți ști până după experiment dacă proprietățile diferitelor lichide pe care le alegeți vor afecta viteza cu care sarea și zahărul se dizolvă, știți că cristalele de sare sunt, în general, mai mici decât cristalele de zahăr. Și știți că temperatura lichidelor nu va fi un factor în experimentul dumneavoastră.
Încercați să vă folosiți experiențele anterioare, informațiile pe care le-ați citit mai devreme în această secțiune și bunul simț pentru a formula o ipoteză solidă.
Rețineți că ipoteza dumneavoastră trebuie să fie enunțată ca o propoziție obiectivă, nu ca o întrebare. Așa că dați-i drumul și -faceți-vă o presupunere dacă sarea sau zahărul se va dizolva mai repede și haideți să începem experimentul.
Materiale de care veți avea nevoie pentru acest proiect
Câteva lichide sugerate pentru a fi folosite în acest experiment sunt oțetul alb, sifonul, ginger ale, detergentul de sticlă, alcoolul de frecat, sucul de mere, limonada și ceaiul. Dacă doriți să înlocuiți cu un alt lichid unul sau mai multe dintre cele sugerate, este în regulă. Doar asigurați-vă că toate lichidele sunt limpezi și la temperatura camerei.
Cantitățile de materiale enumerate mai jos sunt suficiente pentru a realiza experimentul de trei ori cu fiecare lichid. You’ll need:
- 12 clear, plastic cups (10 ounce )
- One permanent marker
- One (1 teaspoon) (5.0 ml) measuring spoon
- One (12 teaspoon) (2.5 ml) measuring spoon
- One (1 cup) (240 ml) measuring cup
- 8 teaspoons (40 ml) salt, divided in 16 (12 teaspoon) portions
- 8 teaspoons (40 ml) sugar, divided in 16 (12 teaspoon) portions
- 48 ounces (1,440 ml) water at room temperature
- 24 ounces (720 ml) each of five different, clear liquids, all at room temperature
- One clock or watch with a second hand
- One clear plastic cup containing eight fluid ounces (240 ml) water at room temperature
Remember to make sure that all liquids are at room temperature.
Conducting Your Experiment
When you’ve gathered all your materials, you’ll be ready to begin your experiment. Urmați doar acești pași:
Păstrați la vedere o ceașcă cu apă plată, astfel încât să o puteți compara cu ceaștile care conțin sare și zahăr. Va fi interesant să urmăriți cum se schimbă aspectul lichidelor pe măsură ce sarea și zahărul se dizolvă.
Va dura puțin timp până când zahărul și sarea se vor dizolva. Pentru cele mai bune rezultate, nu amestecați soluțiile, deoarece acest lucru va prezenta o variabilă suplimentară. Dacă trebuie să amestecați, atunci amestecați fiecare soluție de trei ori, apoi opriți-vă. Amestecați numai după ce observați că există solut pe fundul fiecăruia dintre cele două recipiente. Agitarea inegală a soluțiilor va face ca experimentul dumneavoastră să nu fie valid.
- Folosind markerul permanent, scrieți „sare” pe șase dintre paharele de plastic și „zahăr” pe celelalte șase.
- Puneți 1/2 linguriță (2,5 ml) de sare în fiecare dintre cele șase pahare etichetate ?sare?
- Puneți 1/2 linguriță (2,5 ml) de zahăr în fiecare dintre cele șase pahare etichetate ?zahăr?
- Adăugați 8 uncii (240 ml) de apă într-o ceașcă ce conține sare și una ce conține zahăr. Înregistrați imediat ora la care a fost adăugată apa pe o diagramă de date similară cu cea prezentată în secțiunea următoare, ?Păstrarea evidenței experimentului dumneavoastră?
- Observați solvenții (sarea și zahărul) care se dizolvă în solvent (apă). Înregistrați pe graficul de date momentul în care vi se pare că fiecare solut s-a dizolvat complet. Aceste timpi nu vor fi, probabil, aceiași.
- Calculați timpul scurs în timpul căruia a avut loc dizolvarea. Luați momentul în care apa a fost adăugată în cupe și a început dizolvarea și scădeți-l din momentul în care s-a încheiat dizolvarea. Astfel veți obține numărul total de minute necesare pentru ca sarea și zahărul să se dizolve complet în lichid.
- Repetați pașii de la 4 la 6, folosind fiecare lichid diferit în loc de apă.
- Spălați, clătiți și uscați bine fiecare dintre cele 12 căni.
- Repetați pașii de la 2 la 8 de încă două ori, pentru un total de trei încercări pentru fiecare dintre cele șase lichide.
- Calculați un timp mediu de dizolvare pentru sare și zahăr în fiecare dintre cele șase lichide.
Amintiți-vă că pentru a afla timpul mediu de dizolvare a sării și a zahărului în fiecare lichid, adunați cele trei timpi înregistrați pentru fiecare, apoi împărțiți-i la trei. Numărul pe care îl obțineți atunci când împărțiți timpii este timpul mediu.
Să țineți evidența experimentului dumneavoastră
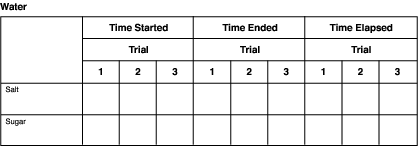
Graficele precum cel de mai jos pot fi folosite pentru a înregistra informații pentru fiecare solvent. Pur și simplu schimbați numele solvenților din titlu.
Asigurați-vă că înregistrați timpii pe măsură ce înaintați. Nu vă bazați pe memoria dumneavoastră pentru a le scrie mai târziu. Veți avea o mulțime de numere în momentul în care veți termina experimentul.
Punând totul cap la cap
Ce ați observat în legătură cu vitezele cu care sarea și zahărul s-au dizolvat? Ați dovedit că ipoteza dumneavoastră este corectă? Sau incorectă? Ați putut detecta vreun tip de model pe măsură ce ați adăugat sarea și zahărul în diferitele lichide? A fost evident că sarea s-a dizolvat mai bine și mai repede în unele lichide în comparație cu zahărul? Vă puteți gândi la vreun motiv pentru care s-ar fi putut întâmpla acest lucru?
Credeți că natura chimică a solutului și a solventului a afectat vitezele de dizolvare? Folosiți informațiile pe care le-ați adunat atunci când v-ați cercetat subiectul pentru a vă ajuta să răspundeți la aceste întrebări.
Cu cât știți mai multe despre proiectul dvs., cu atât veți fi mai capabili să vă analizați corect datele și să ajungeți la o concluzie solidă.
Investigații suplimentare
După cum am menționat mai devreme, factorii care influențează solubilitatea soluanților solizi sunt:
- Creșterea sau descreșterea temperaturii solventului
- Creșterea suprafeței solutului
- Agitarea
Dacă doriți să duceți acest proiect cu un pas sau doi mai departe, ați putea concepe un experiment care să testeze o?sau poate toate?aceste variabile.
Ați putea compara cu ușurință viteza cu care cuburile de zahăr se dizolvă în lichid cu viteza de dizolvare a zahărului granulat.
Sau ați putea folosi același solut?să zicem, zahăr?și să testați dacă agitarea soluției face ca aceasta să se dizolve mai repede. Încălzirea și răcirea solventului pe măsură ce adăugați același solut ar fi, de asemenea, o posibilitate pentru experimente ulterioare.
Dacă sunteți curioși și dispuși să experimentați, probabil că vă puteți gândi la multe variante pentru acest proiect. Și, deoarece experimentul necesită doar materiale comune și ieftine, ar trebui să puteți experimenta până la refuz.
Extras din The Complete Idiot’s Guide to Science Fair Projects 2003 de Nancy K. O’Leary și Susan Shelly. Toate drepturile sunt rezervate, inclusiv dreptul de reproducere integrală sau parțială sub orice formă. Folosit prin acord cu Alpha Books, un membru al Penguin Group (USA) Inc.
Pentru a comanda această carte direct de la editură, vizitați site-ul Penguin USA sau sunați la 1-800-253-6476. De asemenea, puteți achiziționa această carte de pe Amazon.com și Barnes & Noble.
.