Fakten über Fluor
Das reaktionsfreudigste Element im Periodensystem hat eine bewegte Geschichte bei der Suche nach seiner Entdeckung. Trotz der schwierigen und manchmal explosiven Eigenschaften von Fluor ist es ein lebenswichtiges Element für Menschen und Tiere, weshalb es häufig in Trinkwasser und Zahnpasta enthalten ist.
Die Fakten
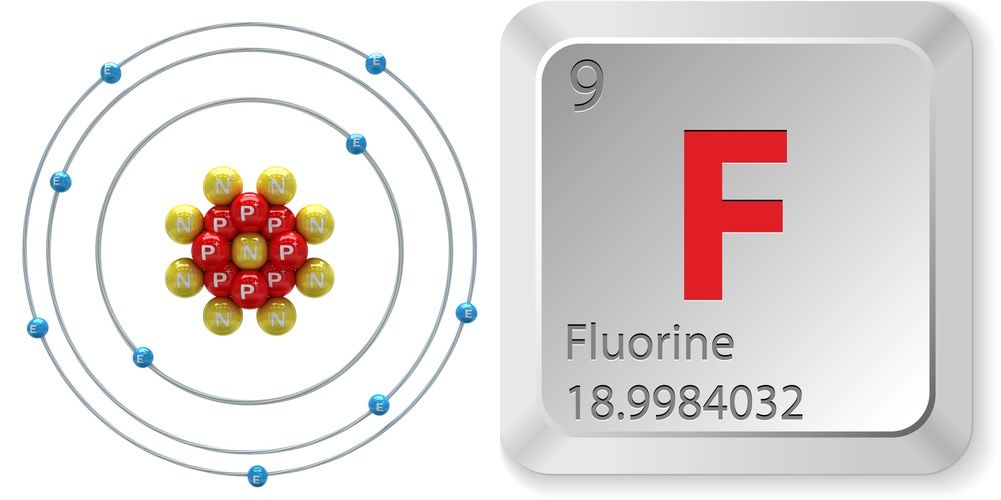
- Atomzahl (Anzahl der Protonen im Kern): 9
- Atomsymbol (im Periodensystem der Elemente): F
- Atomgewicht (durchschnittliche Masse des Atoms): 18,998
- Dichte: 0,001696 Gramm pro Kubikzentimeter
- Phase bei Raumtemperatur: Gas
- Schmelzpunkt: minus 363,32 Grad Fahrenheit (minus 219,62 Grad Celsius)
- Siedepunkt: minus 306,62 Grad Fahrenheit (minus 188,12 Grad Celsius)
- Anzahl der Isotope (Atome desselben Elements mit einer unterschiedlichen Anzahl von Neutronen): 18
- Häufigste Isotope: F-19 (100 Prozent natürliche Häufigkeit)
Geschichte
Frühe Chemiker versuchten jahrelang, das Element aus verschiedenen Fluoriden zu isolieren. Erst 1986 gelang es dem deutschen Chemiker Karl O. Christie, Fluor zu synthetisieren, und er berichtete über seine Ergebnisse in der Zeitschrift Anorganische Chemie. Fluor kommt in der Natur nicht frei vor, aber 2012 fanden Forscher kleine Mengen Fluor in Antozonit, einer Art radioaktivem Fluorit, eingeschlossen.
Jahrhundertelang wurde das Mineral Flussspat in der Metallveredelung verwendet. Das heute als Calciumfluorid (CaF2) bekannte Mineral wurde als Flussmittel verwendet, um reines Metall von unerwünschten Mineralien im Erz zu trennen, so Chemicool. Das „Fluor“ kommt vom lateinischen Wort „fluere“, was so viel wie „fließen“ bedeutet, denn genau das konnte der Flussspat bei Metallen bewirken. Das Mineral wurde auch als böhmischer Smaragd bezeichnet und nach Angaben des Jefferson Laboratory zum Ätzen von Glas verwendet.
Viele Wissenschaftler haben im Laufe der Jahrzehnte versucht, mit Flussspat zu experimentieren, um seine Eigenschaften und seine Zusammensetzung besser zu verstehen. Bei ihren Experimenten stellten die Chemiker oft Flusssäure (heute bekannt als Flusssäure, HF) her, eine unglaublich reaktive und gefährliche Säure. Schon kleine Spritzer dieser Säure auf der Haut können laut Chemicool tödlich sein. Mehrere Wissenschaftler wurden bei einigen Experimenten verletzt, geblendet oder getötet.
Anfang des 19. Jahrhunderts korrespondierten die Wissenschaftler Andre-Marie Ampere in Frankreich und Humphry Davy in England über die Möglichkeit eines neuen Elements in der Säure. Im Jahr 1813 gab Davy die Entdeckung des neuen Elements bekannt und nannte es auf Anregung von Ampere Fluor.
Henri Moissan, ein französischer Chemiker, isolierte Fluor schließlich 1886 – nachdem er bei seinen Nachforschungen mehrmals vergiftet worden war. Für die Isolierung von Fluor durch Elektrolyse von trockenem Kaliumhydrogenfluorid (KHF2) und trockener Flusssäure erhielt er 1906 den Nobelpreis.
Verwendung von Fluor
Seit vielen Jahren werden Fluorsalze oder Fluoride zum Schweißen und zum Mattieren von Glas verwendet, so die Royal Society. Fluorwasserstoffsäure wird beispielsweise zum Ätzen des Glases von Glühbirnen verwendet.
Fluor ist nach Angaben der Royal Society ein wichtiges Element in der Kernenergieindustrie. Es wird zur Herstellung von Uranhexafluorid verwendet, das zur Trennung von Uranisotopen benötigt wird. Schwefelhexafluorid ist ein Gas, das zur Isolierung von Hochleistungstransformatoren verwendet wird.
Fluorchlorkohlenwasserstoffe (FCKW) wurden früher in Aerosolen, Kühlschränken, Klimaanlagen, Schaumstoffverpackungen für Lebensmittel und Feuerlöschern verwendet. Diese Verwendungszwecke sind seit 1996 verboten, weil sie zum Abbau der Ozonschicht beitragen, so die National Institutes of Health. Vor 2009 wurden FCKW in Inhalatoren zur Asthmakontrolle verwendet, aber diese Art von Inhalatoren wurde 2013 aus dem Verkehr gezogen.
Fluor wird in vielen Fluorchemikalien verwendet, darunter Lösungsmittel und Hochtemperaturkunststoffe wie Teflon (Poly(tetrafluorethen), PTFE). Teflon ist für seine Antihafteigenschaften bekannt und wird in Bratpfannen verwendet. Es wird auch für die Isolierung von Kabeln, für Klempnerband und als Grundlage von Gore-Tex® (für wasserdichte Schuhe und Kleidung) verwendet.
Fluor wird der städtischen Wasserversorgung in einem Verhältnis von etwa einem Teil pro Million zugesetzt, um Karies vorzubeugen, so das Jefferson Lab. Verschiedene Fluoridverbindungen werden auch Zahnpasta zugesetzt, um Karies vorzubeugen.
Gesundheits- und Umweltauswirkungen von Fluor
Obwohl alle Menschen und Tiere winzigen Mengen von Fluor ausgesetzt sind und diese benötigen, ist das Element in einer ausreichend hohen Dosis extrem giftig und gefährlich. Nach Angaben von Lenntech kommt Fluor in geringen Mengen in Wasser, Luft und pflanzlichen und tierischen Lebensmitteln vor. Größere Mengen Fluor finden sich in einigen wenigen Lebensmitteln wie Tee und Schalentieren.
Während kleine Mengen Fluor für die Erhaltung der Festigkeit unserer Knochen und Zähne unerlässlich sind, kann ein Zuviel den gegenteiligen Effekt haben und Osteoporose oder Zahnverfall verursachen sowie Nieren, Nerven und Muskeln schädigen.
In seiner gasförmigen Form ist Fluor unglaublich gefährlich. Kleine Mengen von Fluorgas können zu Augen- und Nasenreizungen führen, während größere Mengen tödlich sein können, so Lenntech. Auch Flusssäure, ein weiteres Beispiel, kann laut Chemicool schon bei einem kleinen Spritzer auf die Haut tödlich sein.
In der Umwelt lagert sich Fluor, das dreizehnthäufigste Element in der Erdkruste, typischerweise im Boden ab und verbindet sich leicht mit Erde, Gestein, Kohle und Ton, so Lenntech. Pflanzen können das Fluor aus dem Boden aufnehmen, wobei hohe Konzentrationen zu Schäden führen können. Mais und Aprikosen zum Beispiel gehören zu den Pflanzen, die am anfälligsten für Schäden und Wachstumseinbußen sind, wenn sie erhöhten Fluorwerten ausgesetzt sind.
Wer hätte das gedacht?
- Da Fluor das chemisch reaktivste Element ist, muss es mit äußerster Vorsicht gehandhabt werden, da es laut Chemicool bei Kontakt mit allen anderen Elementen außer Sauerstoff, Helium, Neon und Krypton manchmal explodieren kann.
- Stahlwolle geht laut der Royal Society of Chemistry in Flammen auf, wenn sie Fluor ausgesetzt wird.
- Fluor ist auch das elektronegativste Element. Fluor zieht Elektronen leichter an als jedes andere Element.
- Im Durchschnitt enthält der menschliche Körper drei Milligramm Fluor.
- Fluor wird laut der Minerals Education Coalition vor allem in China, der Mongolei, Russland, Mexiko und Südafrika abgebaut.
- Fluor entsteht in sonnenähnlichen Sternen gegen Ende ihrer Lebensdauer, so ein 2014 in der Zeitschrift Astrophysical Journal Letters veröffentlichter Artikel. Das Element entsteht unter den höheren Drücken und Temperaturen im Inneren des Sterns, wenn er sich zu einem Roten Riesen ausdehnt. Wenn die äußeren Schichten des Sterns weggedrückt werden und ein planetarischer Nebel entsteht, wandert das Fluor zusammen mit den anderen Gasen in das interstellare Medium und bildet schließlich neue Sterne und Planeten.
- Nach Angaben des Journal of Chemistry enthalten etwa 25 Prozent der Arzneimittel und Medikamente, darunter solche für Krebs, das zentrale Nervensystem und das Herz-Kreislauf-System, eine Form von Fluor.
Aktuelle Forschung
Obwohl Fluor giftig sein kann, wenn die Konzentration im Körper zu hoch ist, kann es auch ein vorteilhaftes Element sein, das in Krebsmedikamenten enthalten ist, so ein 2018 im Journal of Fluorine Chemistry veröffentlichter Artikel. Der Forschung zufolge führt das Ersetzen von Kohlenstoff-Wasserstoff- oder Kohlenstoff-Sauerstoff-Bindungen durch eine Kohlenstoff-Fluor-Bindung in den aktiven Komponenten des Medikaments in der Regel zu einer Verbesserung der Wirksamkeit des Medikaments, einschließlich einer höheren Stoffwechselstabilität, einer verstärkten Bindung an Zielmoleküle und einer verbesserten Membrandurchlässigkeit. Man hofft, dass die erhöhte Wirksamkeit der Medikamente in Verbindung mit tumorspezifischen Zielmolekülen oder zielgerichteten Medikamentenverabreichungssystemen die Lebensqualität von Krebspatienten im Vergleich zu herkömmlichen Methoden wie der Chemotherapie, bei der sowohl Krebszellen als auch gesunde Zellen von den Medikamenten angegriffen werden, erheblich verbessern kann.
Diese neue Generation von Krebsbekämpfungsmedikamenten sowie Fluorsonden zur Verabreichung der Medikamente wurde gegen Krebsstammzellen getestet und hat sich als vielversprechend erwiesen, wenn es darum geht, die Krebsstammzellen anzuvisieren und zu bekämpfen, heißt es in der Studie. Die Forscher fanden heraus, dass die Medikamente, die Fluor enthielten, um ein Vielfaches aktiver gegen verschiedene Krebsstammzellen waren und eine bessere Stabilität aufwiesen als herkömmliche Krebsbekämpfungsmittel.